Clear Sky Science · sv
Duktal adenokarcinom i pankreas: integrering av molekylära insikter för riktade interventioner
Varför denna cancer angår oss alla
Duktalt adenokarcinom i pankreas är en av de vanligaste och dödligaste cancerformerna: de flesta patienter lever mindre än två år efter diagnos. Standardbehandlingar som cytostatika och strålning har bara gett måttliga förbättringar, och många av de immunoterapigenombrott som förändrat melanom och lungcancer har i stort sett misslyckats här. Denna översikt sammanför vad forskare nyligen lärt sig om biologin hos pankreastumörer och deras omgivning, och hur den kunskapen kanske till slut kan öppna dörren för mer effektiva, skräddarsydda behandlingar.
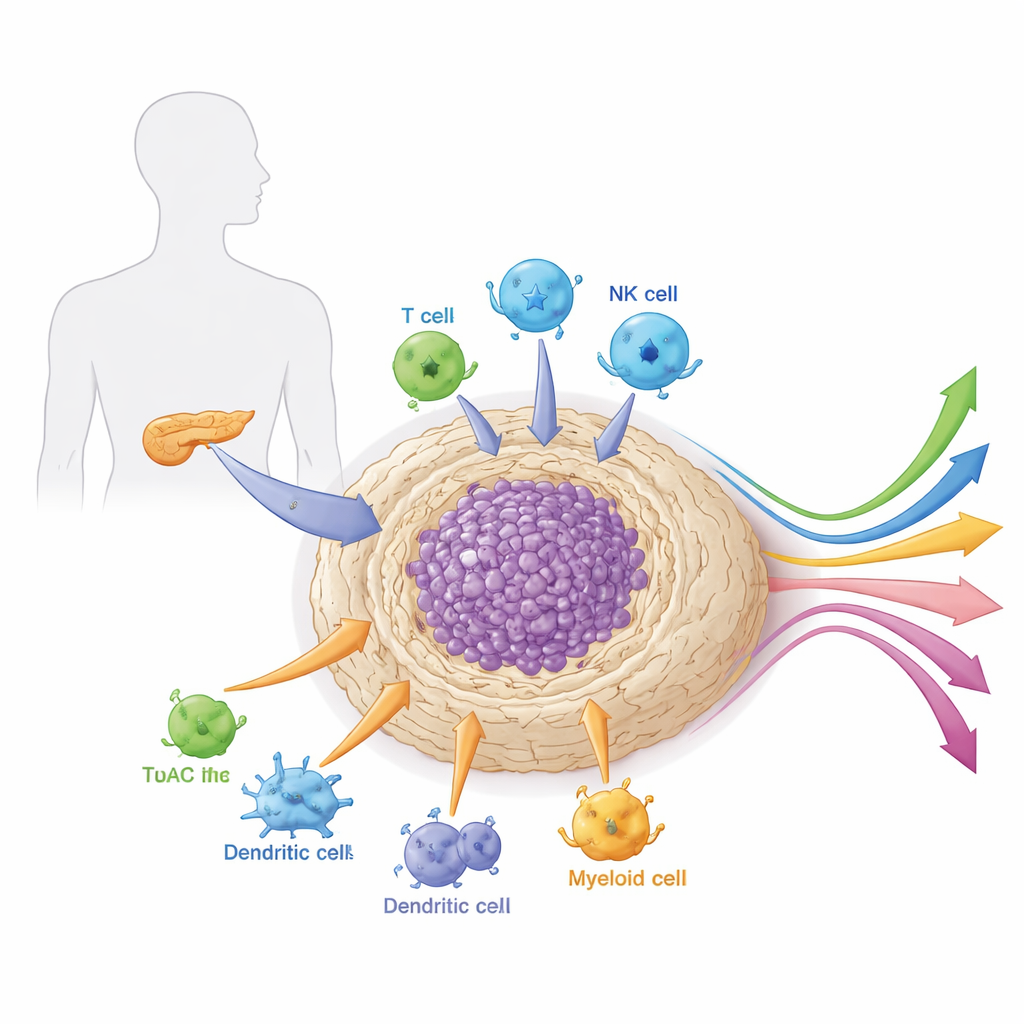
Omgivningen runt tumören
Pankreastumörer växer inte isolerat. De är inbäddade i en tät, ärrliknande vävnad kallad stroma som är fylld med stödjeceller, immunceller, blodkärl och bindvävsmaterial. Detta lokala ”kvarter”, eller mikromiljö, är ovanligt hårt och immunsuppressivt. Det fungerar både som rustning och livsstöd för cancern — fysiskt blockerar det läkemedel och immunceller samtidigt som det tillför tillväxtsignaler och näring. Artikeln förklarar hur olika celltyper i denna mikromiljö — särskilt cancerassocierade fibroblaster, myeloida celler och specialiserade lymfocyter — samarbetar för att skydda tumören från angrepp och formar hur den svarar på behandling.
Supportcellernas många ansikten
Ett centralt fokus i översikten är en mångfaldig familj av celler som kallas cancerassocierade fibroblaster. Tidigare betraktade som en enhetlig typ av strukturell ”hjälparcell”, erkänns dessa fibroblaster nu som flera undergrupper med olika roller. Vissa prolifererar snabbt och bygger det fibrösa skal som stelnar tumören och hindrar läkemedel från att tränga igenom. Andra drar ihop sig och avsätter kollagen, vilket ytterligare förtätar barriären. Inflammatoriska fibroblaster utsöndrar moln av signalsubstanser som attraherar och omprogrammerar immunceller, ofta mot tolerans istället för angrepp. Ytterligare fibroblaster förändrar sin egen ämnesomsättning för att mata tumören eller presenterar till och med fragment av tumörproteiner för T‑celler, ibland till stöd för immunitet och ibland för att driva immunundertryck. Denna rika blandning innebär att en alltför grov avlägsnande av alla fibroblaster kan slå tillbaka; framtida behandlingar behöver selektivt desarmera de skadliga undertyperna samtidigt som skyddande typer bevaras eller förstärks.
Immunceller som blir ovetande allierade
Immunsystemet inne i pankreastumörer är lika komplext. Myeloid‑hereledda suppressorceller och tumörassocierade makrofager dras in i tumören av fibroblast‑ och cancer‑härledda signaler. Väl på plats berövar de mördande T‑celler näringsämnen, släpper ut faktorer som dämpar immunaktivitet och hjälper till att bygga nya blodkärl som göder cancern. Viktiga lymfocytpopulationer omformas också. Regulatoriska T‑celler klustrar sig nära cytotoxiska T‑celler och dämpar deras funktion via checkpoints och metabola knep. Dendritiska celler, som borde primingera antitumörimmunitet, blockeras av den hårda stroman och omprogrammeras av uppbyggnad av fettsyror, så att de presenterar tumörmaterial dåligt. Natural killer‑celler, som normalt är skickliga på att känna igen stressade celler, tystas av tumör‑ och stromasignaler. Tillsammans omvandlar dessa förändringar en potentiellt fientlig immuninfiltrat till ett tolerant sådant, vilket förklarar varför vanliga checkpoint‑läkemedel sällan fungerar ensamma vid pankreascancer.
Gener, signaler och varför terapier misslyckas
På genetisk och molekylär nivå drivs pankreastumörer av en karakteristisk uppsättning förändringar, särskilt mutationer i KRAS, TP53, CDKN2A och SMAD4. Kopieringsnummerförändringar och epigenetiska förändringar omskriver ytterligare tillväxtvägar, cellcykelkontroll och DNA‑reparation. Dessa förändringar matas in i större signalvägar — såsom MAPK och PI3K–AKT–mTOR — som driver proliferationen och hjälper tumörer att anpassa sig när en väg blockeras. De påverkar också hur cancerceller reparerar skadat DNA, vilket öppnar för läkemedel som PARP‑hämmare i tumörer med specifika reparationsdefekter. Samtidigt gör tät stroma, onormal ämnesomsättning och cancerstam‑lika celler tumörerna intrinsikalt resistenta mot cytostatika och riktade läkemedel, och gör att de snabbt utvecklar förvärvad resistens.
Nya strategier och vad som kommer härnäst
I stället för att förlita sig på en ensam ”mirakelkur” argumenterar översikten för rationella kombinationer som angriper både cancercellerna och deras skyddande miljö. Dessa inkluderar att para ihop checkpoint‑hämmare med läkemedel som omstrukturerar fibroblaster eller utarmar suppressiva myeloida celler, att konstruera T‑celler eller natural killer‑celler så att de söker sig in i fibrösa tumörer, att använda vacciner och mRNA‑baserade metoder för att öka igenkänningen av tumörspecifika mål, och att utnyttja svagheter i DNA‑reparation eller KRAS‑signalering. Tidiga kliniska prövningar av sådana kombinationer, tillsammans med sofistikerad genetisk och immunologisk profilering, börjar identifiera vilka patienter som kan dra nytta av vilken strategi. För en lekmannaläsare är huvudbudskapet försiktigt hoppfullt: genom att förstå pankreascancer som ett komplext ekosystem — snarare än bara en massa maligna celler — sätter forskarna äntligen ihop mångfacetterade behandlingsplaner som kan göra denna historiskt svårbehandlade cancer mer mottaglig för terapi.
Citering: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Nyckelord: bukspottkörtelcancer, tumörmikromiljö, immunoterapi, cancerassocierade fibroblaster, KRAS-mutationer