Clear Sky Science · ar
سرطان غدّي القناة البنكرياسية: دمج الرؤى الجزيئية لتدخلات مستهدفة
لماذا يهمنا هذا السرطان جميعًا
سرطان غدّي القناة البنكرياسية من أخطر الأورام الشائعة، حيث يعيش معظم المرضى أقل من عامين بعد التشخيص. العلاجات القياسية مثل العلاج الكيميائي والإشعاعي حققت تقدمًا طفيفًا فقط، والاختراقات في العلاج المناعي التي غيّرت نتائج مرضى الميلانوما وسرطان الرئة فشلت إلى حد كبير هنا. تستعرض هذه المراجعة ما تعلّمه العلماء مؤخرًا عن بيولوجيا أورام البنكرياس ومحيطها، وكيف قد يفتح هذا الفهم أخيرًا الباب أمام علاجات أكثر فعالية ومصممة بدقة.
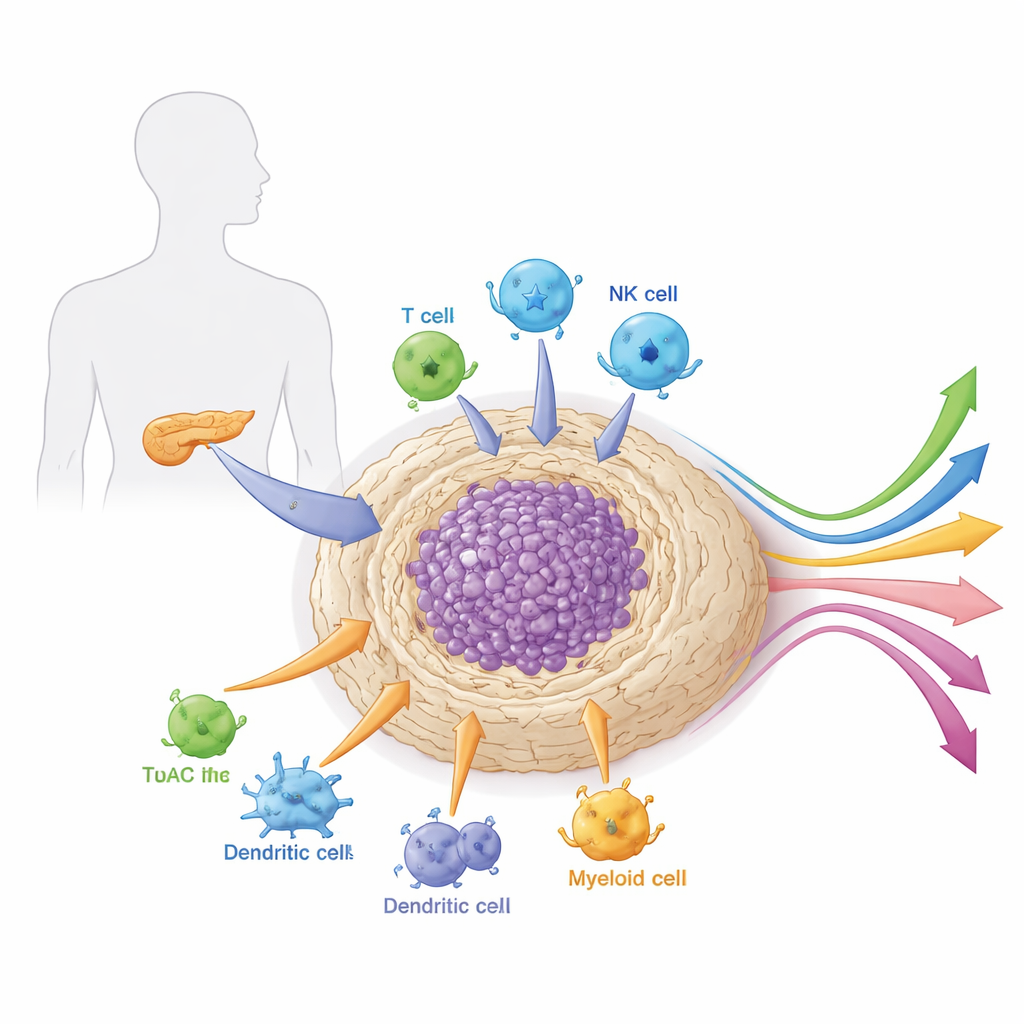
الحي المحيط بالورم
الأورام البنكرياسية لا تنمو بمعزل. إنها مغمورة في نسيج كثيف يشبه الندبة يُسمى السدى، وهو مليء بخلايا داعمة وخلايا مناعية وأوعية دموية ومادة ضامة. هذا "الحي" المحلي، أو البيئة الدقيقة، صعب وغير مهيّئ للمناعة بشكل غير عادي. يعمل كدرع ونظام دعم للحالة السرطانية في آن واحد: يمنع وصول الأدوية والخلايا المناعية من الناحية الفيزيائية بينما يزود الورم بإشارات ونحو غذائية. يوضح المقال كيف تتعاون أنواع خلايا مختلفة داخل هذه البيئة — لا سيما الخلايا الليفية المرتبطة بالسرطان والخلايا النخاعية والخلايا اللمفاوية المتخصصة — لحماية الورم من الهجوم وتشكيل استجابته للعلاج.
الوجوه المتعددة للخلايا الداعمة
محور المراجعة هو عائلة متنوعة من الخلايا تُسمى الخلايا الليفية المرتبطة بالسرطان. كان يُعتقد سابقًا أنها نوع واحد من خلايا الـ"مساعدة" البنيوية، لكنها تُعرف الآن كمجموعات فرعية متعددة ذات أدوار مميزة. البعض يتكاثر بسرعة ويبني القشرة الليفية التي تصلّب الورم وتعيق اختراق الدواء. أخرى تنقبض وتفرز الكولاجين، مما يزيد من إحكام هذا الحاجز. الخلايا الليفية الالتهابية تفرز سُحُبًا من البروتينات الإشارية التي تجذب وتعيد برمجة الخلايا المناعية، وغالبًا ما تدفعها نحو التسامح بدل الهجوم. خلايا ليفية أخرى تغير أيضها لتغذي الورم أو حتى تعرض مقتطفات من بروتينات الورم للخلايا التائية، أحيانًا داعمة للمناعة وأحيانًا مسهمة في كبتها. هذا الخليط الغني يعني أن القضاء الإجمالي على كل الخلايا الليفية قد يأتي بنتيجة عكسية؛ ستحتاج العلاجات المستقبلية إلى تعطيل الأنواع الضارة انتقائيًا مع الحفاظ على الأنواع الواقية أو حتى تعزيزها.
الخلايا المناعية التي تحولت إلى حلفاء غير مقصودين
نظام المناعة داخل أورام البنكرياس معقّد أيضًا. الخلايا المعطلة المشتقة من النخاع والبلعميات المرتبطة بالورم تجذبها إشارات من الخلايا الليفية والسرطانية إلى الورم. وبمجرد وصولها، تجرد المغذيات اللازمة للخلايا التائية القاتلة، وتطلق عوامل تقلل الفعالية المناعية، وتساعد في بناء أوعية دموية جديدة تغذي السرطان. كما تُعاد تشكيل مجموعات اللمفاويات الرئيسية؛ تتجمع الخلايا التائية المنظمة بالقرب من الخلايا التائية السامة للخلايا وتُخمد وظائفها عبر جزيئات نقاط التفتيش وحيل أيضية. الخلايا التغصُّنية، التي يفترض أن تُهيّئ المناعة المضادة للورم، تُعرقل بواسطة السدى الصلب وتعاد برمجتها بتراكم الأحماض الدهنية، فتقدم مادة الورم بشكل سيئ. خلايا القتل الطبيعي، التي تكون عادة بارعة في التعرف على الخلايا المضطربة، تُسكت بإشارات من الورم والسدى. معًا، تحول هذه التغيرات اختراقًا مناعيًا كان من الممكن أن يكون معاديًا إلى اختراق متسامح، مما يشرح لماذا نادراً ما تؤدي أدوية نقاط التفتيش وحدها إلى نجاح في سرطان البنكرياس.
الجينات والإشارات ولماذا تفشل العلاجات
على المستوى الجيني والجزيئي، تقود الأورام البنكرياسية مجموعة مميزة من التغييرات، لا سيما طفرات في KRAS وTP53 وCDKN2A وSMAD4. تغييرات في عدد النسخ والتعديلات اللاجينية تعيد توصيل مسارات النمو، وضبط دورة الخلية، وإصلاح الحمض النووي. تغذي هذه التغيرات شلالات إشارية رئيسية — مثل مسارات MAPK وPI3K–AKT–mTOR — التي تحفز التكاثر وتساعد الأورام على التكيف عندما يُسد طريق واحد. كما تؤثر على كيفية إصلاح خلايا السرطان للحمض النووي التالف، مما يفتح الباب أمام أدوية مثل مثبطات PARP في الأورام التي تعاني من عيوب إصلاح محددة. في الوقت نفسه، يجعل السدى الكثيف والأيض الشاذ وخلايا شبيهة بالجذور السرطانية الأورام مقاومة جوهريًا للعلاج الكيميائي والأدوية المستهدفة، وسريعة في تطوير مقاومة مكتسبة.
استراتيجيات جديدة وما هو آتٍ
بدلاً من الاعتماد على "طلقة سحرية" واحدة، تجادل المراجعة بوجوب اعتماد تراكيب منطقية تعالج كلًا من خلايا السرطان وبيئتها الواقية. تشمل هذه مزج مثبطات نقاط التفتيش مع أدوية تعيد تشكيل الخلايا الليفية أو تستنزف الخلايا النخاعية الكابحة، هندسة الخلايا التائية أو خلايا القتل الطبيعي لتتوجه نحو الأورام الليفية، استخدام اللقاحات والنهج المعتمدة على mRNA لتعزيز التعرف على الأهداف الخاصة بالورم، واستغلال ثغرات في إصلاح الحمض النووي أو إشارات KRAS. بدأت التجارب السريرية المبكرة لمثل هذه التراكيب، إلى جانب التحليل الوراثي والمناعي المتقدم، بتحديد أي المرضى قد يستفيدون من أي استراتيجية. للقرّاء العامين، الرسالة الأساسية متفائلة بحذر: من خلال فهم سرطان البنكرياس كنظام بيئي معقّد — وليس مجرد كتلة من خلايا خبيثة — يجمع الباحثون أخيرًا خطط علاج متعددة الجوانب قد تحول هذا السرطان الذي كان تاريخيًا عصيًا إلى واحد أكثر استجابة للعلاج.
الاستشهاد: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
الكلمات المفتاحية: سرطان البنكرياس, البيئة الدقيقة للورم, العلاج المناعي, الخلايا الليفية المرتبطة بالسرطان, طفرات KRAS