Clear Sky Science · he
אדנוקרצינומה דוקטלית של הלבלב: שילוב תובנות מולקולריות להתערבויות ממוקדות
מדוע הסרטן הזה חשוב לכולנו
אדנוקרצינומה דוקטלית של הלבלב היא אחד מהסרטנים הנפוצים הקטלניים ביותר, כאשר רוב החולים חיים פחות משנתיים לאחר האבחנה. טיפולים סטנדרטיים כמו כימותרפיה וקרינה השיגו רק שיפורים צנועים, והרבה מההישגים בתחום האימונותרפיה ששינו את הטיפול במלנומה וסרטן הריאה נכשלו ברובם כאן. סקירה זו אוספת את מה שחוקרים גילו לאחרונה על הביולוגיה של גידולי הלבלב ושל סביבתם, וכיצד ידע זה עשוי סוף סוף לפתוח דלת לטיפולים יעילים ומותאמים יותר.
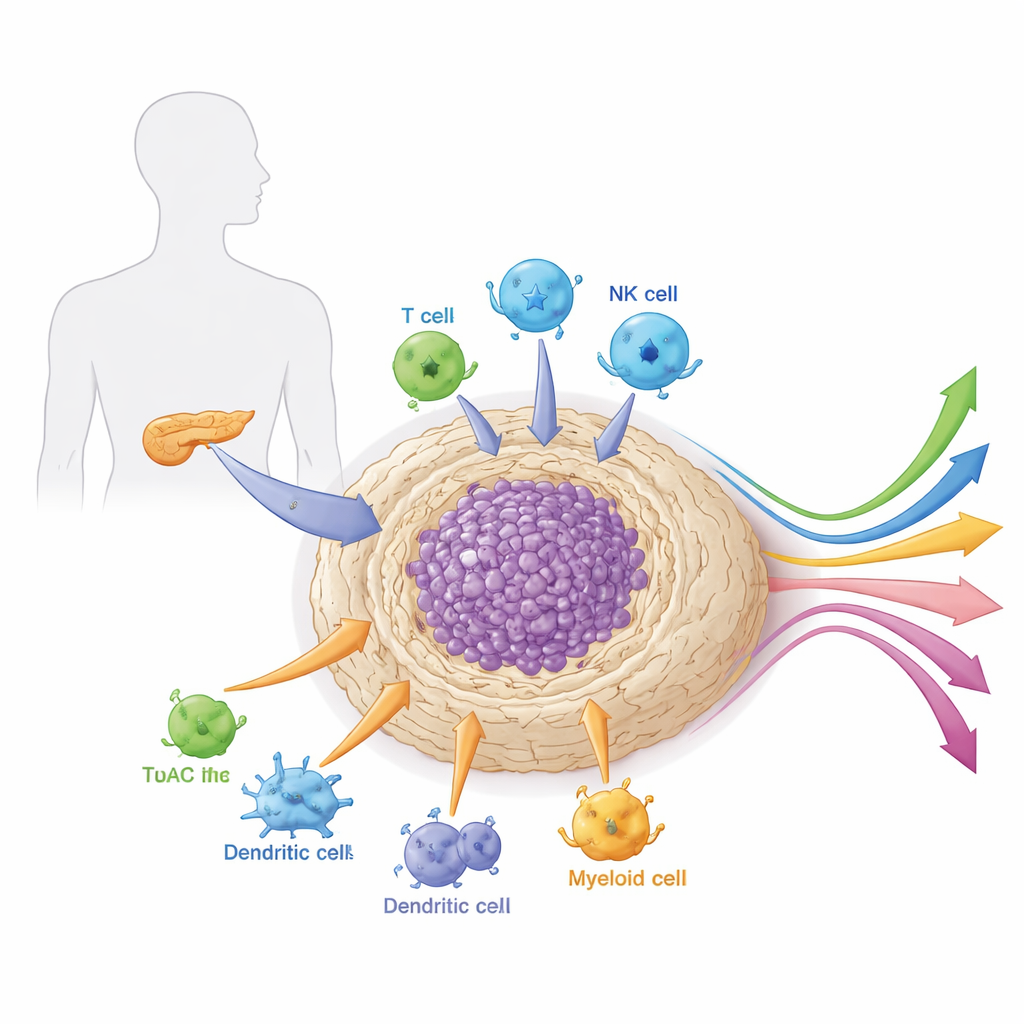
השכונה סביב הגידול
גידולי הלבלב אינם צומחים בבידוד. הם מוטמעים ברקמה צפופה הדומה לצלקת הקרויה סטרומה, המלאה בתאי תמיכה, תאי חיסון, כלי דם וחומר מחבר. ה"שכונה" המקומית הזו, או המיקרו-סביבה, קשה באופן בלתי רגיל ומדכאת חיסון. היא פועלת גם כהשריון וגם כמערכת תמיכה לחיים של הסרטן — חוסמת פיזית תרופות ותאי חיסון ובו בזמן מספקת אותות גדילה ומזון. המאמר מסביר כיצד סוגי תאים שונים בתוך מיקרו- הסביבה הזו — במיוחד פיברובלסטים קשורים לסרטן, תאים מיילואידים ותאי לימפוציטים מותאמים — משתפים פעולה כדי להגן על הגידול מפני התקפה ולעצב את תגובתו לטיפול.
פניהן הרבות של תאי התמיכה
מוקד מרכזי בסקירה הוא משפחה מגוונת של תאים המכונים פיברובלסטים קשורים לסרטן. שהתייחסו אליהם בעבר כסוג בודד של תאי "עזרה" מבניים, הפיברובלסטים האלה מזוהים היום כתת-קבוצות מרובות עם תפקידים מובחנים. חלקם מתרבים במהירות ובונים את מעטפת הסיבים שמקשיחה את הגידול וחוסמת חדירת תרופות. אחרים מתכווצים ומפרישים קולגן, מה שמחזק עוד יותר את המחסום. פיברובלסטים דלקתיים מייצרים ענני חלבוני איתות שמושכים ומנתבים מחדש תאי חיסון, לעתים קרובות לדחוף אותם לעבר סובלנות במקום התקפה. פיברובלסטים אחרים משנים את המטבוליזם שלהם כדי להזין את הגידול או אפילו מציגים שברי חלבוני גידול לתאי T, לעיתים תומכים בחיסון ולעיתים מקדמים דיכוי חיסוני. התערובת העשירה הזו אומרת שמחיקה גסה של כל הפיברובלסטים עלולה לחזור כבומרנג; טיפולים עתידיים יצטרכו לנטרל באופן סלקטיבי את התת-סוגים המזיקים תוך שמירה או אפילו חיזוק של אלה המגנים.
תאי חיסון שהופכים לבעלי ברית בלתי מכוונים
מערכת החיסון בתוך גידולי הלבלב מורכבת באותה מידה. תאים מדכאים מסטמקית מקור מיילואיד ומקרופגים קשורים לגידול נמשכים אל תוך הגידול על ידי אותות שמקורם בפיברובלסטים ובתאי הסרטן. כשהם שם, הם מסירים מזונות שהדרושים לתאי T קטלניים, משחררים גורמים שמטשטשים פעילות חיסונית ועוזרים לבנות כלי דם חדשים המעניקים מזון לסרטן. אוכלוסיות לימפוציטים מרכזיות מעוצבות אף הן מחדש. תאי T רגולטוריים נמצאים בקבוצות סמוכות לתאי T ציטוטוקסיים ומאטות את תפקודם דרך מולקולות בדיקה וטריקים מטבוליים. תאי דנדריטיים, שאמורים להפעיל תגובה חיסונית נגד הגידול, נחסמים על ידי הסטומה הקשיחה ומושתתים על ידי הצטברות חומצות שומן, ולכן הם מציגים חומר גידולי בצורה לקויה. תאי הרוצח הטבעיים, שלרוב מזהים תאים בסטרס, מושתקים על ידי אותות מהגידול ומהסטרומה. יחד, השינויים האלה הופכים חדירת חיסון פוטנציאלית לאויבת לסובלנית, מה שמסביר מדוע תרופות צ'קפוינט סטנדרטיות בלבד בדרך כלל אינן עובדות בסרטן הלבלב.
גנים, אותות ומדוע טיפולים נכשלו
ברמה הגנטית והמולקולרית, גידולי הלבלב מונעים על ידי סט אופייני של שינויים, במיוחד מוטציות ב-KRAS, TP53, CDKN2A ו-SMAD4. שינויים במספר העותקים ושינויים אפיגנטיים משנים עוד יותר מסלולי גדילה, בקרה על מחזור התא ותיקון DNA. שינויים אלה מזינים קסצטות איתות מרכזיות — כגון מסלולי MAPK ו-PI3K–AKT–mTOR — שמניעות התרבות ועוזרות לגידולים להסתגל כשהנתיב האחד נחסם. הם גם משפיעים על אופן תיקון ה-DNA בתאי הסרטן, מה שפותח דלת לשימוש בתרופות כמו מעכבי PARP בגידולים עם ליקויים ספציפיים בתיקון. במקביל, סטרומה צפופה, מטבוליזם לא תקין ותאי גזע בסגנון סרטני עושים את הגידולים בעל-טבעיות עמידים לכימותרפיה ולתרופות ממוקדות, ומהירים בפיתוח עמידות נרכשת.
אסטרטגיות חדשות ומה הלאה
במקום להסתמך על "כדור הקסם" יחיד, הסקירה קוראת לשילובים רציונליים שמתמודדים הן עם תאי הסרטן והן עם סביבת ההגנה שלהם. אלה כוללים צימוד של מעכבי צ'קפוינט עם תרופות שמעצבנות פיברובלסטים או מפחיתות תאי מיילואיד מדכאים, הנדסת תאי T או תאי הרוצח הטבעיים כדי לשכון בגידולים פיברוטיים, שימוש בחיסונים ובגישות מבוססות mRNA להעצמת הזיהוי של מטרות ספציפיות לגידול, וניצול חולשות בתיקון DNA או באיתות KRAS. ניסויים קליניים מוקדמים של שילובים כאלה, יחד עם פרופילינג גנטי וחיסוני משוכלל, מתחילים לזהות אילו חולים עשויים להרוויח מאיזו אסטרטגיה. עבור הקורא הכללי, המסר המרכזי הוא תקווה זהירה: על ידי הבנת סרטן הלבלב כאקוסיסטם מורכב — ולא רק כמסה של תאים ממאירים — החוקרים סוף סוף מרכיבים תוכניות טיפול רב-כיווניות שעשויות להפוך סרטן זה, שהיה עד כה קשה לטיפול, לרגיש יותר לטיפולים.
ציטוט: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
מילות מפתח: סרטן הלבלב, מיקרו-סביבת הגידול, אימונותרפיה, פיברובלסטים קשורים לסרטן, מוטציות KRAS