Clear Sky Science · de
Pankreatisches duktales Adenokarzinom: Integration molekularer Erkenntnisse für gezielte Interventionen
Warum dieser Krebs uns alle betrifft
Das pankreatische duktale Adenokarzinom gehört zu den tödlichsten häufigen Krebserkrankungen: Die meisten Patienten überleben nach der Diagnose weniger als zwei Jahre. Standardbehandlungen wie Chemotherapie und Strahlentherapie haben nur begrenzte Fortschritte gebracht, und viele der Immuntherapie‑Durchbrüche, die Melanom und Lungenkrebs transformierten, versagen weitgehend bei dieser Krankheit. Dieses Review fasst zusammen, was Forschende kürzlich über die Biologie von Pankreastumoren und deren Umfeld gelernt haben und wie dieses Wissen schließlich den Weg zu wirksameren, individuelleren Therapien öffnen könnte.
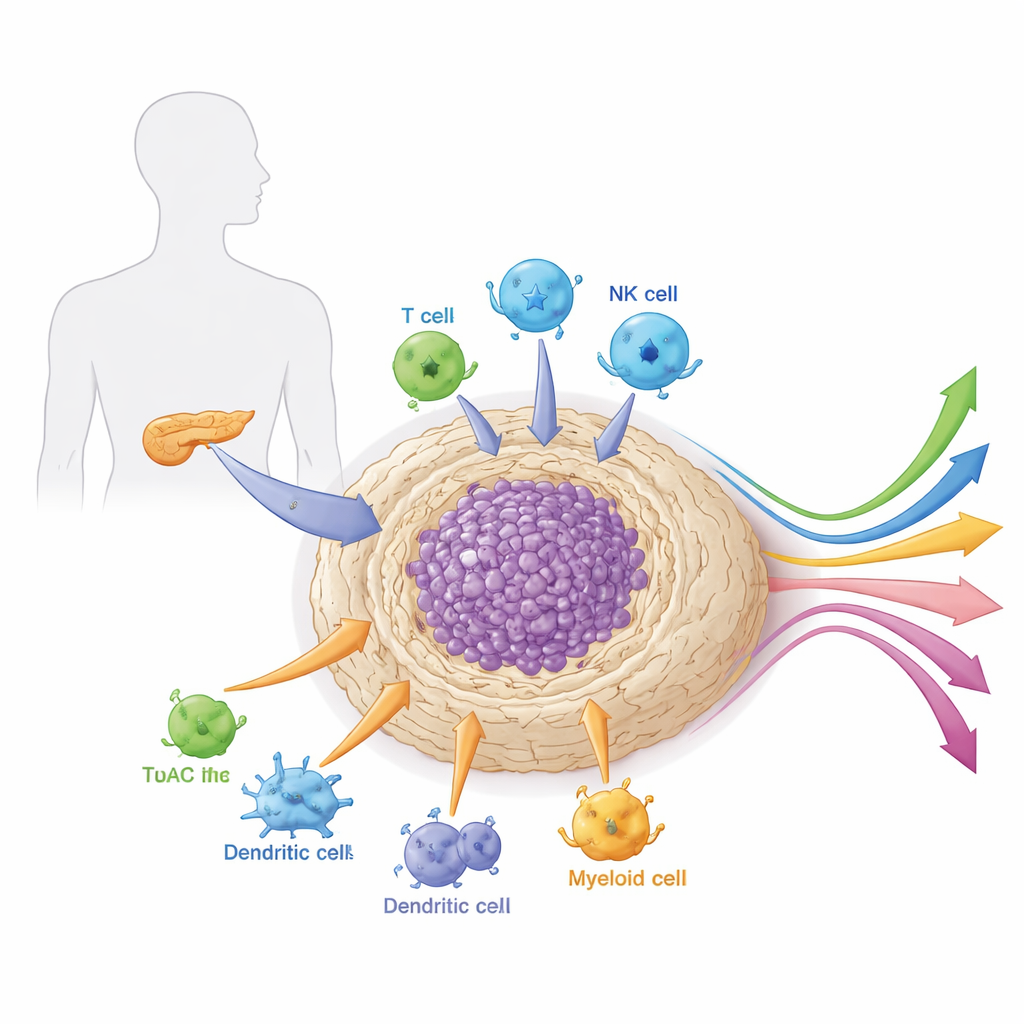
Die Nachbarschaft rund um den Tumor
Pankreastumoren wachsen nicht isoliert. Sie sind eingebettet in ein dichtes, narbenartiges Gewebe, das Stroma genannt wird und voller Stütz‑ und Immunzellen, Blutgefäße und Bindegewebsmaterial ist. Dieses lokale „Viertel“ oder die Mikroumgebung ist ungewöhnlich hart und immununterdrückend. Es wirkt sowohl als Rüstung wie auch als Lebenserhaltungssystem für den Tumor: Es blockiert physisch Medikamente und Immunzellen und liefert zugleich Wachstumssignale und Nährstoffe. Der Artikel erklärt, wie verschiedene Zelltypen innerhalb dieser Mikroumgebung — insbesondere tumorassoziierte Fibroblasten, myeloide Zellen und spezialisierte Lymphozyten — zusammenarbeiten, um den Tumor vor Angriffen zu schützen und seine Therapieantwort zu formen.
Die vielen Gesichter der Stütz‑ und Helferzellen
Im Mittelpunkt der Übersicht steht eine vielfältige Zellfamilie, die als tumorassoziierte Fibroblasten bezeichnet wird. Einst als einheitlicher strukturgebender „Hilfs“typ betrachtet, werden diese Fibroblasten heute als mehrere Subgruppen mit unterschiedlichen Funktionen erkannt. Manche proliferieren schnell und bilden die faserige Hülle, die den Tumor versteift und die Medikamentendurchdringung blockiert. Andere kontrahieren und lagern Kollagen ab, wodurch die Barriere weiter verdichtet wird. Entzündliche Fibroblasten sezernieren Wolken von Signalmolekülen, die Immunzellen anziehen und umprogrammieren, oft hin zu Toleranz statt Angriff. Wieder andere verändern ihren Stoffwechsel, um den Tumor zu ernähren, oder präsentieren Fragmente von Tumorproteinen an T‑Zellen — manchmal die Immunität unterstützend, manchmal immunsuppressiv wirkend. Diese komplexe Mischung bedeutet, dass ein pauschales Entfernen aller Fibroblasten nach hinten losgehen kann; künftige Therapien müssen schädliche Subtypen gezielt entwaffnen und zugleich protektive Subpopulationen erhalten oder sogar stärken.
Immunzellen als ungewollte Verbündete
Auch das Immunsystem innerhalb pankreatischer Tumoren ist höchst komplex. Myeloid‑abgeleitete Suppressorzellen und tumorassoziierte Makrophagen werden durch Signale von Fibroblasten und Tumorzellen angezogen. Einmal vorhanden, entziehen sie Killer‑T‑Zellen notwendige Nährstoffe, setzen Faktoren frei, die die Immunaktivität dämpfen, und helfen beim Aufbau neuer Blutgefäße, die den Tumor versorgen. Wichtige Lymphozytenpopulationen werden ebenfalls umgeformt. Regulatorische T‑Zellen sammeln sich nahe zytotoxischer T‑Zellen und dämpfen deren Funktion über Checkpoint‑Moleküle und metabolische Tricks. Dendritische Zellen, die eigentlich Anti‑Tumor‑Immunität initiieren sollten, werden durch das steife Stroma blockiert und durch Fettansammlungen umprogrammiert, sodass sie Tumormaterial nur schlecht präsentieren. Natürliche Killerzellen, normalerweise geübt darin, gestresste Zellen zu erkennen, werden durch tumorale und stromale Signale stillgelegt. Zusammengenommen verwandeln diese Veränderungen ein potenziell feindliches Immuninfiltrat in eines, das Toleranz fördert — ein Grund, weshalb alleinige Checkpoint‑Therapien bei Pankreaskrebs selten erfolgreich sind.
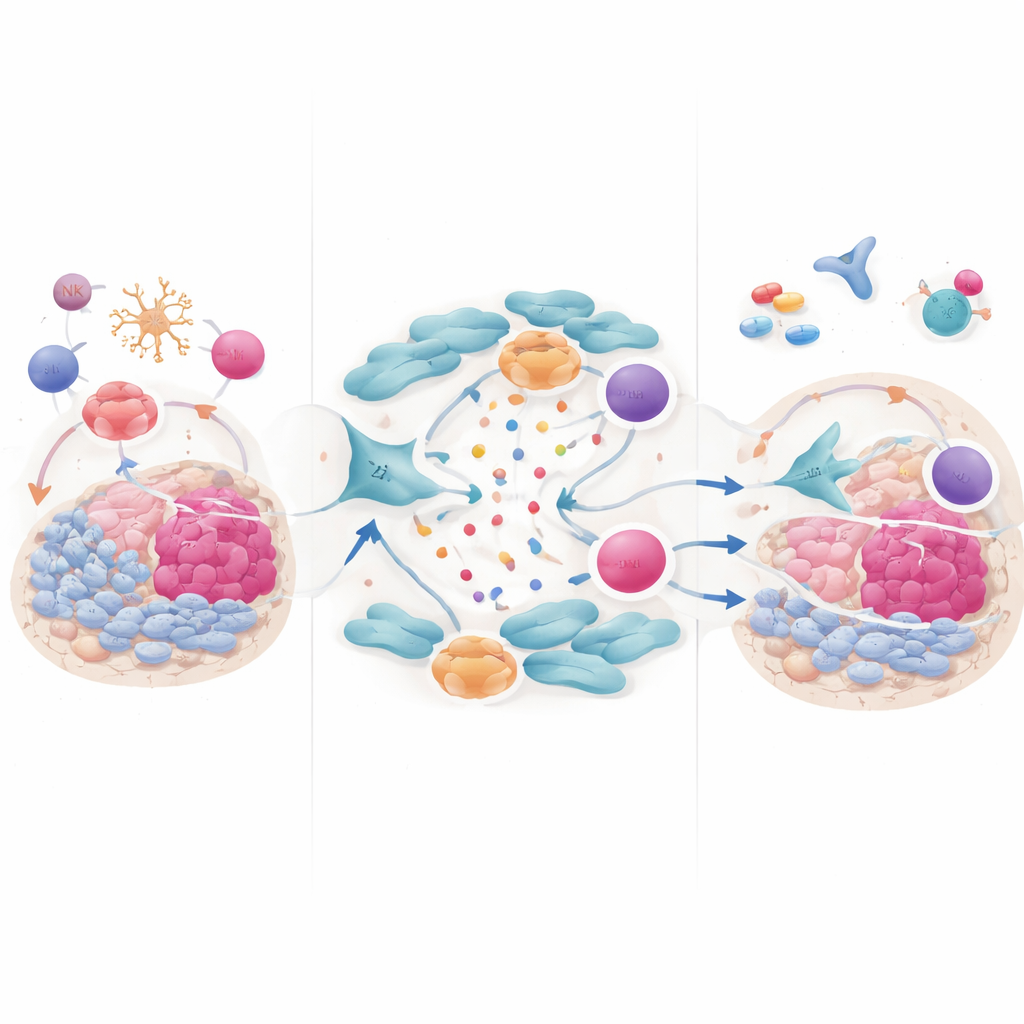
Gene, Signale und warum Therapien versagen
Auf genetischer und molekularer Ebene werden pankreatische Tumoren von einem charakteristischen Satz von Veränderungen angetrieben, insbesondere Mutationen in KRAS, TP53, CDKN2A und SMAD4. Kopienzahlanomalien und epigenetische Modifikationen verdrahten Wachstumswege, Zellzykluskontrolle und DNA‑Reparatur weiter um. Diese Veränderungen speisen sich in wesentliche Signalwege — etwa MAPK und PI3K–AKT–mTOR — die Proliferation antreiben und Tumoren helfen, wenn ein Weg blockiert wird, auf andere Ausweichrouten umzuschalten. Sie beeinflussen auch, wie Krebszellen beschädigte DNA reparieren, was den Einsatz von Medikamenten wie PARP‑Inhibitoren bei Tumoren mit spezifischen Reparaturdefekten ermöglicht. Gleichzeitig machen dichtes Stroma, anomaler Stoffwechsel und tumorstammzellähnliche Zellen Tumoren intrinsisch resistent gegen Chemotherapie und zielgerichtete Wirkstoffe und begünstigen die rasche Entwicklung erworbener Resistenzen.
Neue Strategien und wie es weitergeht
Statt auf eine einzelne „Wunderwaffe“ zu setzen, plädiert das Review für rationale Kombinationen, die sowohl die Krebszellen als auch ihr schützendes Umfeld angreifen. Dazu gehören die Kombination von Checkpoint‑Inhibitoren mit Wirkstoffen, die Fibroblasten umgestalten oder suppressive myeloide Zellen reduzieren, das gentechnische Engineering von T‑Zellen oder natürlichen Killerzellen, damit sie fibrotische Tumoren erreichen, der Einsatz von Impfstoffen und mRNA‑basierten Ansätzen zur Stärkung der Erkennung tumorspezifischer Ziele sowie die Ausnutzung von Schwachstellen in der DNA‑Reparatur oder KRAS‑Signalgebung. Frühe klinische Studien solcher Kombinationen zusammen mit ausgefeiltem genetischem und immunologischem Profiling beginnen zu zeigen, welche Patienten von welcher Strategie profitieren könnten. Für Laien lautet die Kernbotschaft vorsichtiger Optimismus: Indem man Pankreaskrebs als komplexes Ökosystem begreift — nicht nur als Masse bösartiger Zellen — stellen Forschende endlich mehrgleisige Behandlungspläne zusammen, die diese historisch schwer zugängliche Krankheit möglicherweise therapieempfindlicher machen.
Zitation: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Schlüsselwörter: pankreaskrebs, tumormikroumgebung, Immuntherapie, tumorassoziierte Fibroblasten, KRAS‑Mutationen