Clear Sky Science · fr
Adénocarcinome canalaire pancréatique : intégrer les connaissances moléculaires pour des interventions ciblées
Pourquoi ce cancer nous concerne tous
L’adénocarcinome canalaire du pancréas est l’un des cancers parmi les plus meurtriers : la majorité des patients vivent moins de deux ans après le diagnostic. Les traitements standards, comme la chimiothérapie et la radiothérapie, n’ont apporté que des gains modestes, et bon nombre des percées en immunothérapie qui ont transformé la prise en charge du mélanome et du cancer du poumon ont largement échoué ici. Cette revue rassemble les découvertes récentes sur la biologie des tumeurs pancréatiques et de leur environnement, et explique comment ces connaissances pourraient enfin ouvrir la voie à des traitements plus efficaces et mieux ciblés.
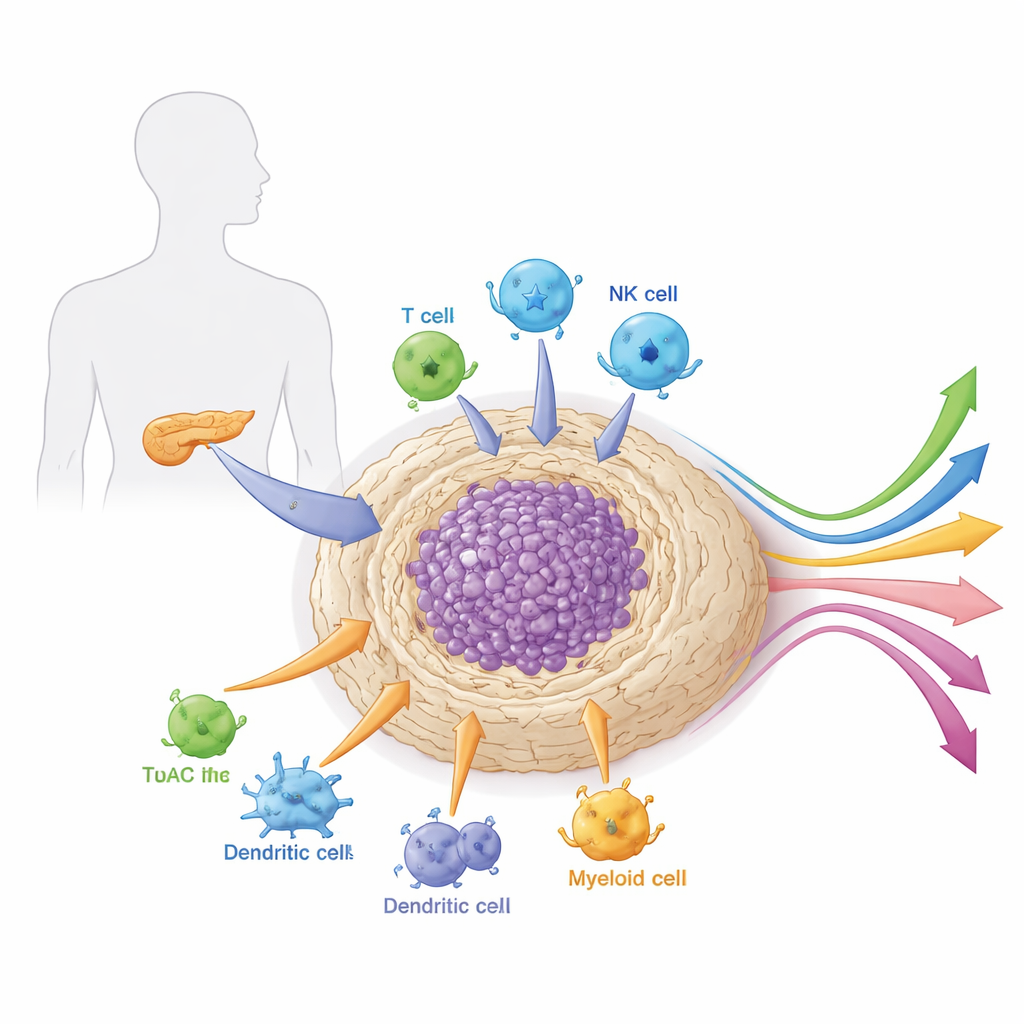
Le voisinage autour de la tumeur
Les tumeurs pancréatiques ne se développent pas en isolation. Elles sont enchâssées dans un tissu dense, de type cicatriciel, appelé stroma, qui regorge de cellules de soutien, de cellules immunitaires, de vaisseaux sanguins et de matière conjonctive. Ce « voisinage » local, ou microenvironnement, est particulièrement robuste et immunosuppresseur. Il joue à la fois le rôle d’armure et de système de survie pour le cancer : il bloque physiquement les médicaments et les cellules immunitaires tout en fournissant des signaux de croissance et des nutriments. L’article détaille comment différents types cellulaires au sein de ce microenvironnement — notamment les fibroblastes associés au cancer, les cellules myéloïdes et des lymphocytes spécialisés — coopèrent pour protéger la tumeur des attaques et influencer sa réponse aux thérapies.
Les multiples visages des cellules de soutien
Un des axes centraux de la revue concerne une famille hétérogène de cellules appelées fibroblastes associés au cancer. Autrefois considérés comme un seul type de cellules « auxiliaires » structurelles, ces fibroblastes sont désormais reconnus comme plusieurs sous-groupes aux rôles distincts. Certains prolifèrent rapidement et construisent une coque fibreuse qui rigidifie la tumeur et empêche la pénétration des médicaments. D’autres se contractent et déposent du collagène, renforçant encore cette barrière. Les fibroblastes inflammatoires sécrètent des nuages de protéines de signalisation qui attirent et reprogramment les cellules immunitaires, les orientant souvent vers la tolérance plutôt que l’attaque. D’autres fibroblastes modifient leur propre métabolisme pour nourrir la tumeur ou présentent des fragments de protéines tumorales aux lymphocytes T, soutenant parfois l’immunité et parfois favorisant l’immunosuppression. Cette diversité signifie qu’éliminer brutalement tous les fibroblastes peut se révéler contre-productif ; les traitements futurs devront désarmer sélectivement les sous-types délétères tout en préservant, voire en renforçant, les sous-types protecteurs.
Des cellules immunitaires devenues alliées involontaires
Le système immunitaire au sein des tumeurs pancréatiques est tout aussi complexe. Les cellules suppressives d’origine myéloïde et les macrophages associés à la tumeur sont attirés par des signaux provenant des fibroblastes et des cellules cancéreuses. Une fois présents, ils épuisent les nutriments nécessaires aux lymphocytes T cytotoxiques, libèrent des facteurs qui atténuent l’activité immune et contribuent à la formation de nouveaux vaisseaux qui nourrissent le cancer. Les populations de lymphocytes sont également remodelées. Les cellules T régulatrices se regroupent à proximité des lymphocytes T cytotoxiques et réduisent leur fonction via des molécules de point de contrôle et des détours métaboliques. Les cellules dendritiques, qui devraient amorcer une réponse anti-tumorale, sont entravées par le stroma rigide et reprogrammées par l’accumulation d’acides gras, si bien qu’elles présentent mal le matériel tumoral. Les cellules NK, normalement efficaces pour reconnaître les cellules stressées, sont silencées par des signaux tumoraux et stromaux. Ensemble, ces modifications transforment un infiltrat immunitaire potentiellement hostile en un infiltrat tolérant, ce qui explique en grande partie pourquoi les inhibiteurs de points de contrôle seuls sont rarement efficaces contre le cancer du pancréas.
Gènes, signaux et raisons des échecs thérapeutiques
Au niveau génétique et moléculaire, les tumeurs pancréatiques sont animées par un ensemble caractéristique d’altérations, en particulier des mutations de KRAS, TP53, CDKN2A et SMAD4. Des altérations du nombre de copies et des modifications épigénétiques reconfigurent en outre les voies de croissance, le contrôle du cycle cellulaire et la réparation de l’ADN. Ces altérations alimentent d’importantes cascades de signalisation — comme les voies MAPK et PI3K–AKT–mTOR — qui stimulent la prolifération et permettent à la tumeur de s’adapter lorsqu’une voie est bloquée. Elles influencent aussi la manière dont les cellules cancéreuses réparent l’ADN endommagé, ouvrant la possibilité d’utiliser des médicaments comme les inhibiteurs de PARP dans les tumeurs présentant des défauts spécifiques de réparation. Parallèlement, la stroma dense, le métabolisme anormal et les cellules souches tumorales rendent les tumeurs intrinsèquement résistantes à la chimiothérapie et aux thérapies ciblées, et prédisposent à l’apparition rapide de résistances acquises.
Nouvelles stratégies et perspectives
Plutôt que de compter sur une « balle magique » unique, la revue plaide pour des combinaisons rationnelles qui s’attaquent à la fois aux cellules cancéreuses et à leur environnement protecteur. Cela inclut l’association d’inhibiteurs de points de contrôle avec des médicaments qui remodelent les fibroblastes ou épuisent les cellules myéloïdes suppressives, l’ingénierie de lymphocytes T ou de cellules NK pour qu’ils ciblent les tumeurs fibreuses, l’utilisation de vaccins et d’approches à base d’ARNm pour renforcer la reconnaissance de cibles tumorales spécifiques, et l’exploitation des vulnérabilités en réparation de l’ADN ou dans la signalisation KRAS. Des essais cliniques précoces de telles combinaisons, associés à un profilage génétique et immunitaire sophistiqué, commencent à identifier quels patients pourraient bénéficier de quelle stratégie. Pour le lecteur non spécialiste, le message principal est prudemment optimiste : en comprenant le cancer du pancréas comme un écosystème complexe — plutôt que comme une simple masse de cellules malignes — les chercheurs assemblent enfin des plans thérapeutiques multi‑volets qui pourraient rendre ce cancer historiquement difficile davantage réceptif aux traitements.
Citation: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Mots-clés: cancer du pancréas, microenvironnement tumoral, immunothérapie, fibroblastes associés au cancer, mutations KRAS