Clear Sky Science · tr
Pankreas duktal adenomakarsinomu: hedefe yönelik müdahaleler için moleküler içgörüleri bütünleştirmek
Bu kanserin hepimiz için neden önemli olduğu
Pankreas duktal adenomakarsinom, yaygın kanserler arasında en ölümcüllerden biridir; tanı konan hastaların çoğu iki yıldan kısa süre yaşar. Kemoterapi ve radyasyon gibi standart tedaviler yalnızca sınırlı ilerleme sağlamış, melanom ve akciğer kanserinde devrim yaratan birçok immünoterapi buluşu burada büyük ölçüde başarısız olmuştur. Bu derleme, bilim insanlarının pankreas tümörlerinin biyolojisi ve çevresi hakkında son zamanlarda öğrendiklerini bir araya getiriyor ve bu bilgilerin nihayet daha etkili, kişiye özel tedavilere kapı açabileceğini tartışıyor.
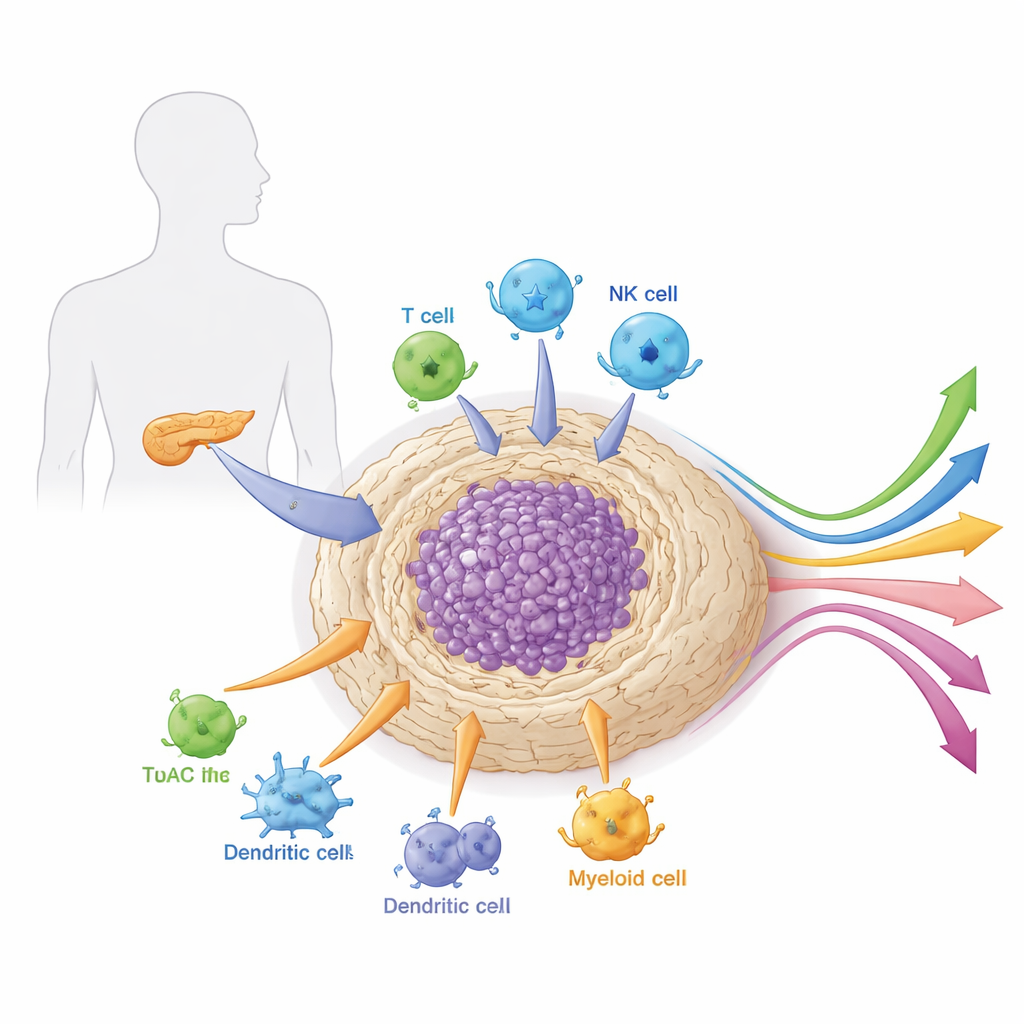
Tümörün çevresindeki mahalle
Pankreas tümörleri izole büyümez. Destek hücreleri, bağışıklık hücreleri, kan damarları ve bağ doku maddesiyle dolu, yoğun, yara izi benzeri bir doku olan stromaya gömülüdürler. Bu yerel “mahalle” veya mikroçevre alışılmadık derecede sert ve immünsüpresif özellik taşır. Hem kanser için zırh hem de yaşam desteği görevi görür; ilaçları ve bağışıklık hücrelerini fiziksel olarak engellerken büyüme sinyalleri ve besin sağlar. Makale, özellikle kansere bağlı fibroblastlar, miyeloid hücreler ve uzmanlaşmış lenfositler olmak üzere bu mikroçevredeki farklı hücre tiplerinin tümörü saldırılardan nasıl koruduğunu ve tedaviye yanıtını nasıl şekillendirdiğini açıklıyor.
Destek hücrelerinin çok yüzlülüğü
Derlemenin merkezi odağı, kansere bağlı fibroblastlar olarak adlandırılan çeşitli hücre ailesidir. Bir zamanlar tek tip yapısal “yardımcı” hücre olarak düşünülen bu fibroblastların artık farklı rollere sahip birden çok alt grup olarak tanındığı anlaşılmıştır. Bazıları hızla çoğalır ve tümörü sertleştirip ilaç penetrasyonunu engelleyen fibröz kabuğu oluşturur. Başkaları kasılarak kollajen döşer ve bu bariyeri daha da sıkılaştırır. İnflamatuar fibroblastlar, bağışıklık hücrelerini çeken ve yeniden programlayan sinyal proteinleri salgılar; sıklıkla bu hücreleri saldırmak yerine toleransa ittirirler. Diğer fibroblastlar metabolizmalarını değiştirerek tümörü besler veya bazen tümör protein parçalarını T hücrelerine sunarak ya immüniteyi destekler ya da immün baskıyı tetikler. Bu zengin karışım, tüm fibroblastları körlemesine ortadan kaldırmanın ters etki yapabileceği anlamına gelir; gelecekteki tedaviler zararlı alt tipleri seçici olarak etkisiz hale getirirken koruyucu olanları korumalı veya hatta güçlendirmelidir.
Bağışıklık hücrelerinin istemeden müttefike dönüşmesi
Pankreas tümörleri içindeki bağışıklık sistemi de eşit derecede karmaşıktır. Miyeloid kaynaklı baskılayıcı hücreler ve tümöre bağlı makrofajlar, fibroblast ve kanser kaynaklı sinyallerle tümöre çekilir. Oraya ulaştıklarında, katil T hücrelerinin ihtiyacı olan besinleri tüketir, bağışıklık aktivitesini azaltan faktörler salgılar ve kanseri besleyen yeni kan damarlarının oluşmasına yardımcı olurlar. Önemli lenfosit popülasyonları da yeniden şekillenir. Düzenleyici T hücreleri sitotoksik T hücrelerinin yakınında kümelenir ve kontrol noktası molekülleri ile metabolik mekanizmalar aracılığıyla onların işlevini azaltır. Anti-tümör bağışıklığını hazırlaması gereken dendritik hücreler, sert stroma tarafından engellenir ve yağ asidi birikimiyle yeniden programlandıkları için tümör materyalini kötü sunarlar. Normalde stres altındaki hücreleri tanımada yetkin olan doğal katil hücreler de tümör ve stromal sinyallerle susturulur. Bu değişiklikler bir araya gelerek potansiyel olarak düşmanca bir bağışıklık infiltratını toleranslı bir hale çevirir ve bu da standart kontrol noktası ilaçlarının pankreas kanserinde tek başına nadiren etkili olmasını açıklar.
Genler, sinyaller ve neden tedaviler başarısız oluyor
Genetik ve moleküler düzeyde pankreas tümörleri, özellikle KRAS, TP53, CDKN2A ve SMAD4 mutasyonları gibi karakteristik değişikliklerle yönlendirilir. Kopya sayısı değişiklikleri ve epigenetik değişimler, büyüme yollarını, hücre döngüsü kontrolünü ve DNA onarımını yeniden kablolayarak ilave uyum sağlar. Bu değişiklikler MAPK ve PI3K–AKT–mTOR gibi ana sinyal kaskadlarına beslenir; bu yollar proliferasyonu sürdürür ve bir yol bloke edildiğinde tümörlerin uyum sağlamasına yardım eder. Ayrıca kanser hücrelerinin hasarlı DNA’yı nasıl onardığını etkileyerek belirli onarım kusurları olan tümörlerde PARP inhibitörleri gibi ilaçlara kapı açar. Aynı zamanda yoğun stroma, anormal metabolizma ve kanser kök hücresi benzeri hücreler, tümörleri kemoterapi ve hedefe yönelik ilaçlara karşı içsel olarak dirençli kılar ve kazanılmış direnci hızla geliştirir.
Yeni stratejiler ve gelecek ne getirir
Tek bir “mucize kurşuna” güvenmek yerine derleme, kanser hücreleri ile onların koruyucu ortamını aynı anda hedefleyen rasyonel kombinasyonları savunuyor. Bunlar arasında kontrol noktası inhibitörlerini fibroblastları yeniden şekillendiren veya baskılayıcı miyeloid hücreleri azaltan ilaçlarla eşleştirmek, fibrotik tümörlere yönelen T hücreleri veya doğal katil hücreleri tasarlamak, tümör-spesifik hedeflerin tanınmasını artırmak için aşılar ve mRNA tabanlı yaklaşımlar kullanmak ve DNA onarımı veya KRAS sinyalleşmesindeki zayıflıkları sömürmek yer alır. Bu tür kombinasyonların erken klinik denemeleri ile sofistike genetik ve bağışıklık profillemesi, hangi hastanın hangi stratejiden yararlanabileceğini belirlemeye başlıyor. Halk için ana mesaj temkinli bir umut: pankreas kanserini yalnızca kötü huylu hücrelerin bir kütlesi olarak değil, karmaşık bir ekosistem olarak anlamak sayesinde araştırmacılar nihayet bu tarihsel olarak güç çözülen kanseri terapilere daha duyarlı hale getirebilecek çok yönlü tedavi planları bir araya getiriyorlar.
Atıf: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Anahtar kelimeler: pankreas kanseri, tümör mikroçevresi, immünoterapi, kansere bağlı fibroblastlar, KRAS mutasyonları