Clear Sky Science · pl
Gruczolakorak przewodów trzustkowych: integrowanie wiedzy molekularnej dla ukierunkowanych interwencji
Dlaczego ten nowotwór ma znaczenie dla nas wszystkich
Gruczolakorak przewodów trzustkowych należy do najgroźniejszych powszechnych nowotworów — większość pacjentów przeżywa mniej niż dwa lata od rozpoznania. Standardowe terapie, takie jak chemioterapia i radioterapia, przyniosły jedynie skromne postępy, a wiele przełomów immunoterapeutycznych, które zrewolucjonizowały leczenie czerniaka i raka płuca, w tym wypadku zawiodło. Niniejszy przegląd zestawia najnowsze odkrycia dotyczące biologii guzów trzustki i ich otoczenia oraz wyjaśnia, jak ta wiedza może wreszcie otworzyć drogę do skuteczniejszych, spersonalizowanych terapii.
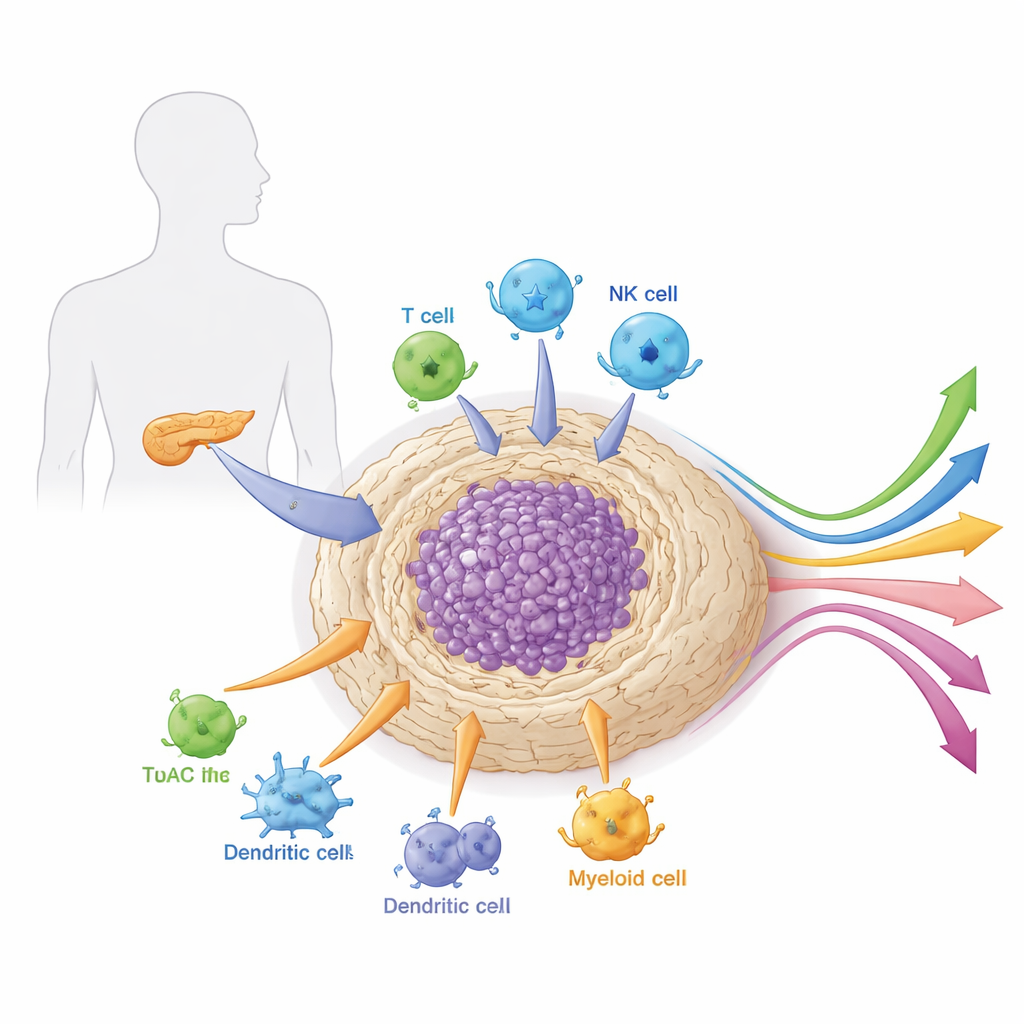
Sąsiedztwo wokół guza
Guzy trzustki nie rosną w izolacji. Są osadzone w gęstej, bliznowatej tkance zwanej zrębem, wypełnionej komórkami podporowymi, komórkami układu odpornościowego, naczyniami krwionośnymi i materiałem łączącym. To lokalne „sąsiedztwo”, czyli mikrośrodowisko, jest wyjątkowo twarde i immunosupresyjne. Działa zarówno jak pancerz, jak i system podtrzymania życia dla nowotworu — fizycznie blokuje leki i komórki odpornościowe, a jednocześnie dostarcza sygnałów wzrostowych i składników odżywczych. Artykuł opisuje, jak różne typy komórek w tym mikrośrodowisku — w szczególności fibroblasty związane z nowotworem, komórki mieloidalne i wyspecjalizowane limfocyty — współpracują, by osłaniać guz przed atakiem i kształtować jego odpowiedź na terapię.
Wiele twarzy komórek podporowych
Centralnym punktem przeglądu jest różnorodna rodzina komórek zwanych fibroblastami związanymi z nowotworem. Kiedyś uważane za jeden typ strukturalnych „pomocników”, fibroblasty te są dziś rozpoznawane jako wiele podgrup o odmiennych rolach. Niektóre szybko proliferują i tworzą włóknistą powłokę, która usztywnia guz i blokuje przenikanie leków. Inne kurczą się i deponują kolagen, dodatkowo wzmacniając tę barierę. Fibroblasty prozapalne wydzielają chmury białek sygnalizacyjnych, które przyciągają i przeprogramowują komórki odpornościowe, często skłaniając je ku tolerancji zamiast ataku. Kolejne podtypy zmieniają własny metabolizm, by odżywiać guz, a nawet prezentują fragmenty białek nowotworowych limfocytom T — czasem wspierając odporność, a czasem ją tłumiąc. Ta bogata mieszanka oznacza, że brutalne eliminowanie wszystkich fibroblastów może przynieść skutek odwrotny do zamierzonego; przyszłe terapie będą musiały selektywnie unieszkodliwiać szkodliwe podtypy przy zachowaniu lub nawet wzmocnieniu ochronnych.
Komórki odpornościowe zmienione w nieświadomych sojuszników
Układ odpornościowy w guzach trzustki jest równie złożony. Komórki mieloidalne o właściwościach supresyjnych oraz makrofagi związane z guzem są przyciągane przez sygnały pochodzące od fibroblastów i komórek nowotworowych. Po przybyciu odbierają składniki odżywcze niezbędne cytotoksycznym limfocytom T, uwalniają czynniki tłumiące aktywność immunologiczną i pomagają budować nowe naczynia krwionośne, które odżywiają nowotwór. Kluczowe populacje limfocytów także ulegają przekształceniu. Limfocyty T regulatorowe gromadzą się blisko komórek cytotoksycznych i osłabiają ich funkcję poprzez cząsteczki kontrolne oraz sztuczki metaboliczne. Komórki dendrytyczne, które powinny inicjować odpowiedź przeciwko nowotworowi, są blokowane przez sztywny zrąb i przeprogramowywane wskutek nagromadzenia kwasów tłuszczowych, przez co słabo prezentują materiał nowotworowy. Komórki natural killer, zwykle skuteczne w rozpoznawaniu zestresowanych komórek, są uciszane przez sygnały guza i zrębu. Wspólnie te zmiany przekształcają potencjalnie wrogą infiltrację immunologiczną w tolerancyjną, co tłumaczy, dlaczego standardowe inhibitory punktów kontrolnych rzadko działają solo w raku trzustki.
Geny, sygnały i dlaczego terapie zawodzą
Na poziomie genetycznym i molekularnym guzy trzustki napędzane są charakterystycznym zestawem zmian, w szczególności mutacjami w genach KRAS, TP53, CDKN2A i SMAD4. Zmiany liczby kopii i modyfikacje epigenetyczne dodatkowo przestawiają szlaki wzrostu, kontrolę cyklu komórkowego i naprawę DNA. Te modyfikacje wpływają na główne kaskady sygnałowe — takie jak szlak MAPK i PI3K–AKT–mTOR — które napędzają proliferację i pomagają guzom adaptować się, gdy jedna droga zostaje zablokowana. Mają też znaczenie dla naprawy uszkodzonego DNA, otwierając możliwości leków typu inhibitory PARP w guzach z określonymi defektami naprawy. Równocześnie gęsty zrąb, nieprawidłowy metabolizm i komórki przypominające komórki macierzyste nowotworu czynią guzy inherentnie opornymi na chemioterapię i leki celowane oraz szybciej rozwijającymi oporność nabytą.
Nowe strategie i co dalej
Zamiast polegać na pojedynczej „magicznej kuli”, przegląd opowiada się za racjonalnymi kombinacjami, które atakują zarówno komórki nowotworowe, jak i ich ochronne otoczenie. Należą do nich łączenia inhibitorów punktów kontrolnych z lekami przebudowującymi fibroblasty lub usuwającymi supresyjne komórki mieloidalne, modyfikowanie genetyczne limfocytów T lub komórek natural killer, aby trafiały do zwłókniałych guzów, stosowanie szczepionek i podejść opartych na mRNA w celu zwiększenia rozpoznawania celów specyficznych dla nowotworu oraz wykorzystywanie słabości w naprawie DNA lub sygnalizacji KRAS. Wczesne badania kliniczne takich kombinacji, wraz z zaawansowanym profilowaniem genetycznym i immunologicznym, zaczynają określać, którzy pacjenci mogą skorzystać z których strategii. Dla czytelnika nieprofesjonalnego kluczowe przesłanie jest ostrożnie optymistyczne: rozumiejąc raka trzustki jako złożony ekosystem — a nie tylko jako skupisko komórek złośliwych — badacze w końcu składają wielotorowe plany leczenia, które mogą przekształcić ten historycznie trudny do leczenia nowotwór w chorobę bardziej podatną na terapię.
Cytowanie: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Słowa kluczowe: rak trzustki, mikrośrodowisko guza, immunoterapia, fibroblasty związane z nowotworem, mutacje KRAS