Clear Sky Science · nl
Pancreasductaal adenocarcinoom: moleculaire inzichten integreren voor gerichte interventies
Waarom deze kanker ons allemaal aangaat
Pancreasductaal adenocarcinoom behoort tot de dodelijkste veelvoorkomende vormen van kanker; de meeste patiënten leven minder dan twee jaar na de diagnose. Standaardbehandelingen zoals chemotherapie en bestraling hebben slechts bescheiden vooruitgang geboekt, en veel van de immunotherapie-doorbraken die huidkanker en longkanker transformeerden, hebben hier grotendeels gefaald. Dit overzicht bundelt wat onderzoekers recent hebben ontdekt over de biologie van pancreastumoren en hun omgeving, en hoe die kennis mogelijk eindelijk de deur opent naar effectievere, op maat gemaakte behandelingen.
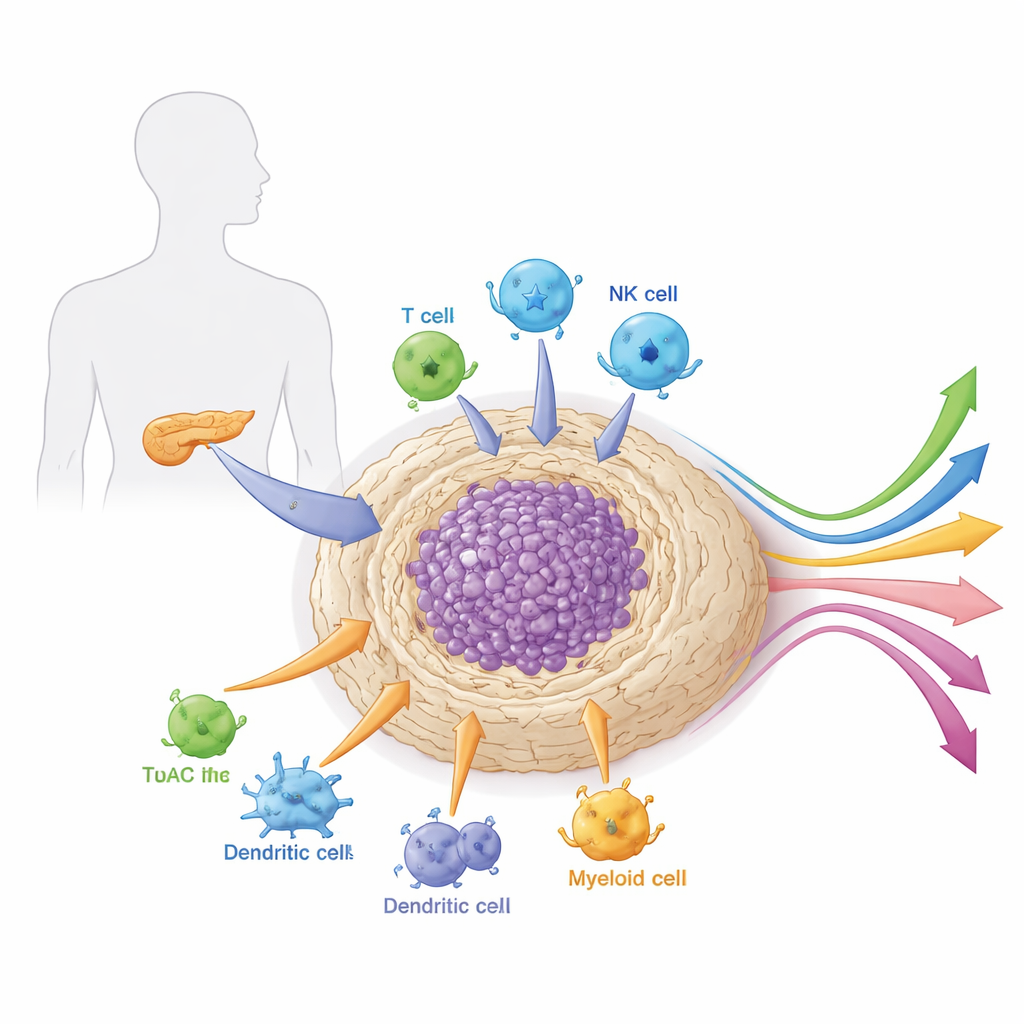
De buurt rond de tumor
Pancreastumoren groeien niet geïsoleerd. Ze zitten ingebed in een dicht, littekenachtig weefsel dat het stroma wordt genoemd en vol zit met ondersteunende cellen, immuuncellen, bloedvaten en bindweefsel. Deze lokale “buurt”, oftewel micro-omgeving, is uitzonderlijk taai en immuunsuppressief. Ze functioneert zowel als pantser als levensondersteuning voor de kanker: fysiek blokkeert ze medicijnen en immuuncellen, terwijl ze groeisinalen en voedingsstoffen levert. Het artikel legt uit hoe verschillende celtypen binnen deze micro-omgeving — met name kanker-geassocieerde fibroblasten, myeloïde cellen en gespecialiseerde lymfocyten — samenwerken om de tumor te beschermen tegen aanvallen en te bepalen hoe deze op therapie reageert.
De vele gezichten van ondersteunende cellen
Een centraal thema van het overzicht is een diverse familie cellen die kanker-geassocieerde fibroblasten worden genoemd. Ooit gezien als één type structurele “hulp”-cel, worden deze fibroblasten nu herkend als meerdere subgroepen met onderscheidende rollen. Sommige delen zich snel en bouwen de vezelige schaal die de tumor verhardt en de medicijnpenetratie belemmert. Andere trekken samen en leggen collageen neer, waardoor deze barrière verder wordt aangespannen. Inflammatoire fibroblasten scheiden wolken van signaaleiwitten uit die immuuncellen aantrekken en herprogrammeren, vaak richting tolerantie in plaats van aanval. Weer andere fibroblasten wijzigen hun eigen metabolisme om de tumor van voeding te voorzien of presenteren fragments van tumoreiwitten aan T-cellen, soms ter ondersteuning van de immuniteit en soms ter bevordering van immuunsuppressie. Deze rijke mix betekent dat het rücksichtslos verwijderen van alle fibroblasten averechts kan werken; toekomstige behandelingen zullen schadelijke subtypen selectief moeten uitschakelen terwijl beschermende typen worden behouden of zelfs versterkt.
Immuuncellen die ongewild bondgenoten worden
Het immuunsysteem binnen pancreastumoren is even complex. Myeloïde afgeleide suppressorcellen en tumorgeassocieerde macrofagen worden door fibroblast- en kankersignalen naar de tumor gelokt. Eenmaal daar ontnemen ze voedingsstoffen die nodig zijn voor killer-T-cellen, geven ze factoren vrij die de immuunactiviteit dempen en helpen ze bij het opbouwen van nieuwe bloedvaten die de kanker voeden. Belangrijke lymfocytpopulaties worden ook hervormd. Regulatorische T-cellen clusteren nabij cytotoxische T-cellen en verzwakken hun functie via checkpoint-moleculen en metabolische trucs. Dendritische cellen, die de anti-tumorimmuniteit zouden moeten primen, worden geblokkeerd door het stijve stroma en herprogrammeerd door ophoping van vetzuren, waardoor ze tumormateriaal slecht presenteren. Natural killer-cellen, normaal vaardig in het herkennen van gestreste cellen, worden stilgelegd door tumor- en stromale signalen. Gezamenlijk veranderen deze processen een potentieel vijandige immuuninfiltraat in een tolerante populatie, wat verklaart waarom standaard checkpoint-remmers op zichzelf zelden werken bij pancreaskanker.
Genen, signalen en waarom therapieën falen
Op genetisch en moleculair niveau worden pancreastumoren gedreven door een kenmerkende set veranderingen, met name mutaties in KRAS, TP53, CDKN2A en SMAD4. Copy-number-alteraties en epigenetische veranderingen herschakelen daarnaast groeipaden, celcycluscontrole en DNA-reparatie. Deze veranderingen voeden grote signaalroutes — zoals de MAPK- en PI3K–AKT–mTOR-pathways — die proliferatie aandrijven en tumoren helpen zich aan te passen wanneer een route wordt geblokkeerd. Ze beïnvloeden ook hoe kankercellen beschadigd DNA herstellen, wat de deur opent voor middelen zoals PARP-remmers in tumoren met specifieke reparatiedefecten. Tegelijkertijd zorgen dicht stroma, abnormaal metabolisme en kankerstamcelachtige cellen ervoor dat tumoren intrinsiek resistent zijn tegen chemotherapie en gerichte middelen, en snel verworven resistentie ontwikkelen.
Nieuwe strategieën en wat volgt
In plaats van te vertrouwen op één “gouden kogel” pleit het overzicht voor rationele combinaties die zowel de kankercellen als hun beschermende omgeving aanpakken. Dit omvat het combineren van checkpoint-remmers met middelen die fibroblasten herbouwen of suppressieve myeloïde cellen uitputten, het inrichten van T-cellen of natural killer-cellen zodat ze naar fibrotische tumoren kunnen trekken, het gebruik van vaccins en op mRNA gebaseerde benaderingen om de herkenning van tumor-specifieke doelen te versterken, en het benutten van zwaktes in DNA-reparatie of KRAS-signaalgeving. Vroege klinische proeven met dergelijke combinaties, samen met verfijnde genetische en immuunprofilering, beginnen te identificeren welke patiënten baat kunnen hebben bij welke strategie. Voor een niet-specialistische lezer is de kernboodschap voorzichtig hoopgevend: door pancreaskanker te begrijpen als een complex ecosysteem — in plaats van slechts een massa kwaadaardige cellen — stellen onderzoekers eindelijk meerledige behandelingsplannen samen die deze historisch hardnekkige kanker mogelijk ontvankelijker maken voor therapie.
Bronvermelding: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Trefwoorden: pancreaskanker, tumormicro-omgeving, immunotherapie, kanker-geassocieerde fibroblasten, KRAS-mutaties