Clear Sky Science · es
Adenocarcinoma ductal pancreático: integrar conocimientos moleculares para intervenciones dirigidas
Por qué este cáncer nos importa a todos
El adenocarcinoma ductal pancreático es uno de los cánceres comunes más letales; la mayoría de los pacientes viven menos de dos años tras el diagnóstico. Los tratamientos estándar, como la quimioterapia y la radiación, han conseguido avances modestos, y muchos de los éxitos en inmunoterapia que transformaron el tratamiento del melanoma y del cáncer de pulmón han fracasado en gran medida aquí. Esta revisión reúne lo que los científicos han descubierto recientemente sobre la biología de los tumores pancreáticos y su entorno, y cómo ese conocimiento puede por fin abrir la puerta a tratamientos más eficaces y personalizados.
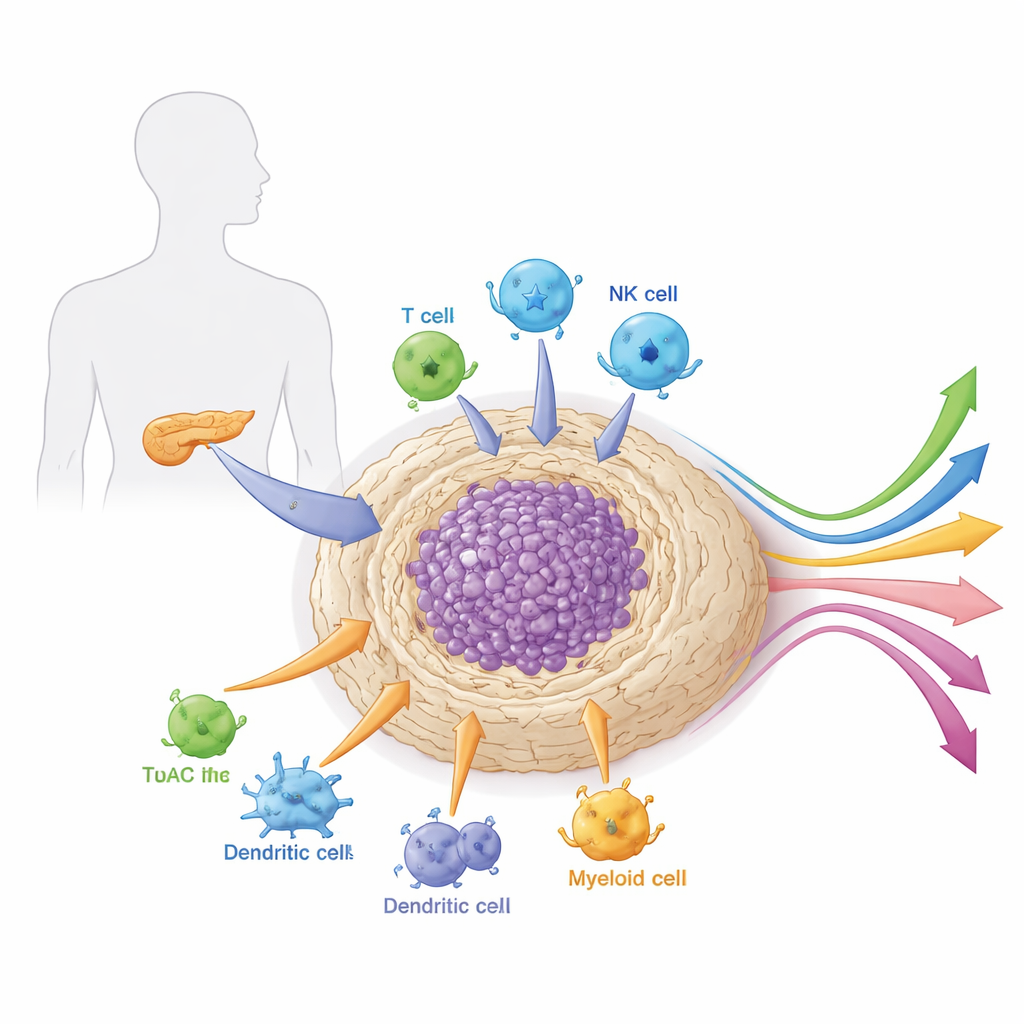
El vecindario alrededor del tumor
Los tumores pancreáticos no crecen aislados. Están incrustados en un tejido denso y parecido a una cicatriz llamado estroma, que está repleto de células de soporte, células inmunitarias, vasos sanguíneos y material conectivo. Este “vecindario” local, o microambiente, es inusualmente rígido e inmunosupresor. Actúa como armadura y sistema de soporte vital para el cáncer: bloquea físicamente fármacos y células inmunitarias mientras suministra señales de crecimiento y nutrientes. El artículo explica cómo los distintos tipos celulares dentro de este microambiente —especialmente los fibroblastos asociados al cáncer, las células mieloides y linfocitos especializados— cooperan para proteger al tumor del ataque y condicionan su respuesta a la terapia.
Las múltiples caras de las células de soporte
Un foco central de la revisión es una familia diversa de células llamadas fibroblastos asociados al cáncer. Antes se pensaba que eran un único tipo de célula estructural «auxiliar», pero ahora se reconocen múltiples subgrupos con roles distintos. Algunos proliferan rápidamente y construyen la capa fibrosa que endurece el tumor y bloquea la penetración de fármacos. Otros se contraen y depositan colágeno, reforzando aún más esta barrera. Los fibroblastos inflamatorios secretan nubes de proteínas señalizadoras que atraen y reprograman células inmunitarias, a menudo empujándolas hacia la tolerancia en lugar del ataque. Otros fibroblastos alteran su propio metabolismo para nutrir al tumor o incluso presentan fragmentos de proteínas tumorales a las células T, a veces apoyando la inmunidad y otras veces promoviendo la inmunosupresión. Esta mezcla compleja implica que eliminar de forma contundente todos los fibroblastos puede resultar contraproducente; los tratamientos futuros tendrán que desactivar selectivamente los subtipos dañinos mientras preservan o incluso potencian los protectores.
Células inmunitarias convertidas en cómplices involuntarios
El sistema inmune dentro de los tumores pancreáticos es igualmente complejo. Las células supresoras derivadas de la médula y los macrófagos asociados al tumor son atraídos por señales de fibroblastos y de las propias células cancerosas. Una vez allí, privan a las células T citotóxicas de nutrientes, liberan factores que apagan la actividad inmune y ayudan a formar nuevos vasos sanguíneos que nutren al cáncer. Las poblaciones clave de linfocitos también se remodelan. Las células T reguladoras se agrupan cerca de las células T citotóxicas y atenúan su función mediante moléculas de control y trucos metabólicos. Las células dendríticas, que deberían iniciar la inmunidad antitumoral, quedan bloqueadas por el estroma rígido y reprogramadas por la acumulación de ácidos grasos, por lo que presentan pobremente el material tumoral. Las células asesinas naturales, normalmente hábiles en reconocer células estresadas, se silencian por señales del tumor y del estroma. En conjunto, estos cambios convierten una infiltración inmune potencialmente hostil en una tolerante, lo que explica por qué los fármacos de bloqueo de puntos de control por sí solos rara vez funcionan en el cáncer de páncreas.
Genes, señales y por qué fallan las terapias
A nivel genético y molecular, los tumores pancreáticos están impulsados por un conjunto característico de alteraciones, especialmente mutaciones en KRAS, TP53, CDKN2A y SMAD4. Las alteraciones en el número de copias y los cambios epigenéticos reconfiguran además las vías de crecimiento, el control del ciclo celular y la reparación del ADN. Estas alteraciones alimentan cascadas de señalización principales —como las vías MAPK y PI3K–AKT–mTOR— que impulsan la proliferación y ayudan a los tumores a adaptarse cuando una vía se bloquea. También influyen en cómo las células cancerosas reparan el ADN dañado, lo que abre la puerta a fármacos como los inhibidores de PARP en tumores con defectos específicos en la reparación. Al mismo tiempo, el estroma denso, el metabolismo anómalo y las células con rasgos de células madre cancerosas hacen que los tumores sean intrínsecamente resistentes a la quimioterapia y a los fármacos dirigidos, y que desarrollen rápidamente resistencias adquiridas.
Nuevas estrategias y lo que sigue
En lugar de confiar en una sola «bala mágica», la revisión aboga por combinaciones racionales que ataquen tanto a las células cancerosas como a su entorno protector. Estas incluyen emparejar inhibidores de puntos de control con fármacos que remodelen fibroblastos o agoten las células mieloides supresoras, diseñar células T o células asesinas naturales para que migren hacia tumores fibróticos, usar vacunas y enfoques basados en ARNm para potenciar el reconocimiento de dianas tumorales específicas, y explotar debilidades en la reparación del ADN o en la señalización de KRAS. Ensayos clínicos tempranos con estas combinaciones, junto con perfiles genéticos e inmunitarios sofisticados, están empezando a identificar qué pacientes podrían beneficiarse de cada estrategia. Para el lector no especialista, el mensaje clave es de esperanza cautelosa: al entender el cáncer de páncreas como un ecosistema complejo —en lugar de solo una masa de células malignas— los investigadores están finalmente ensamblando planes terapéuticos multifacéticos que podrían convertir este cáncer históricamente intratable en uno más sensible al tratamiento.
Cita: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Palabras clave: cáncer de páncreas, microambiente tumoral, inmunoterapia, fibroblastos asociados al cáncer, mutaciones KRAS