Clear Sky Science · pt
Adenocarcinoma ductal pancreático: integrando insights moleculares para intervenções direcionadas
Por que este câncer nos interessa a todos
O adenocarcinoma ductal pancreático está entre os cânceres comuns mais letais, com a maioria dos pacientes vivendo menos de dois anos após o diagnóstico. Tratamentos padrão, como quimioterapia e radioterapia, trouxeram ganhos modestos, e muitas das inovações em imunoterapia que transformaram melanoma e câncer de pulmão falharam em grande parte aqui. Esta revisão reúne o que os cientistas aprenderam recentemente sobre a biologia dos tumores pancreáticos e seu entorno, e como esse conhecimento pode finalmente abrir a porta para tratamentos mais eficazes e personalizados.
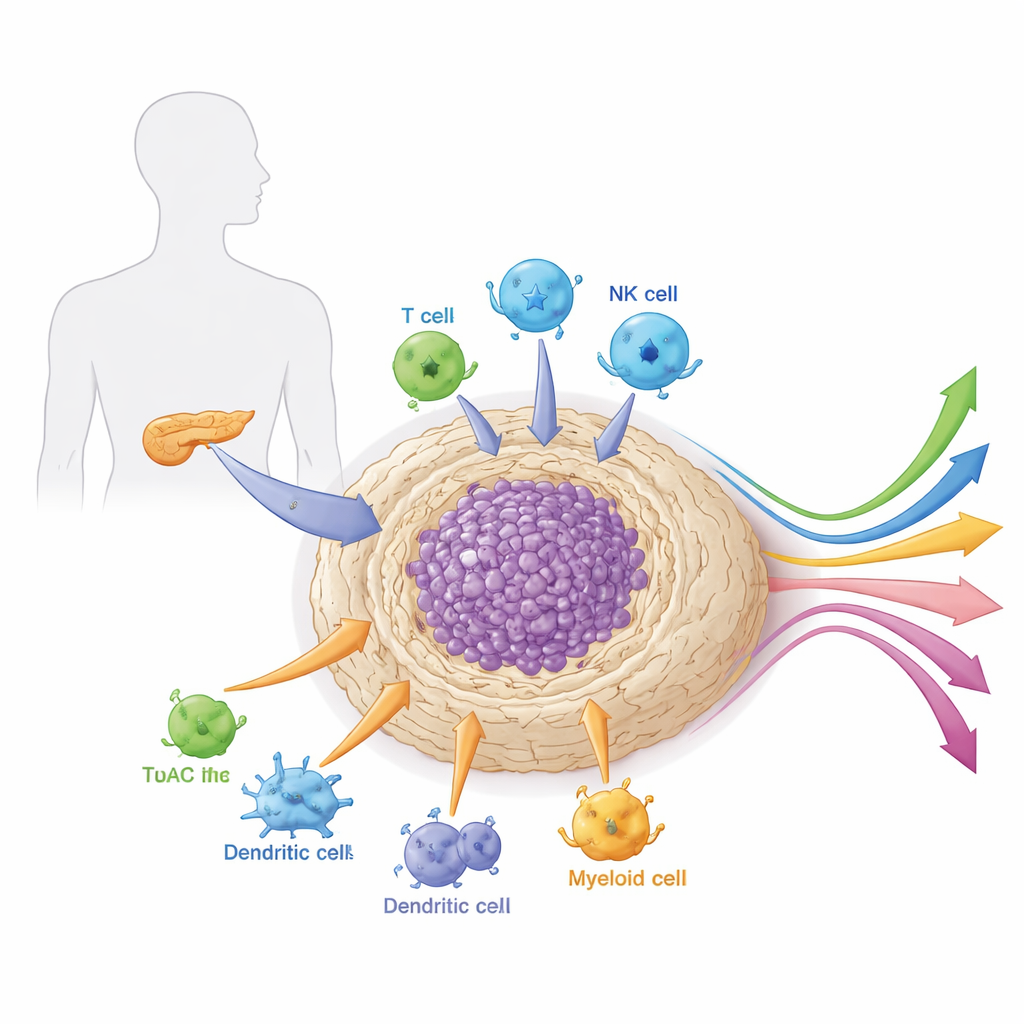
O bairro ao redor do tumor
Os tumores pancreáticos não crescem isolados. Eles estão inseridos em um tecido denso, semelhante a uma cicatriz, chamado estroma, repleto de células de suporte, células imunes, vasos sanguíneos e material conectivo. Esse “bairro” local, ou microambiente, é incomumente rígido e imunossupressor. Ele atua como armadura e sistema de suporte à vida do câncer, bloqueando fisicamente drogas e células imunes enquanto fornece sinais de crescimento e nutrientes. O artigo explica como diferentes tipos celulares dentro desse microambiente — em especial fibroblastos associados ao câncer, células mieloides e linfócitos especializados — cooperam para proteger o tumor do ataque e moldar sua resposta à terapia.
As muitas faces das células de suporte
Um foco central da revisão é uma família diversa de células chamadas fibroblastos associados ao câncer. Antes vistos como um único tipo de célula “auxiliar” estrutural, esses fibroblastos hoje são reconhecidos como subgrupos distintos com papéis diferentes. Alguns proliferam rapidamente e constroem a casca fibrosa que endurece o tumor e bloqueia a penetração de fármacos. Outros se contraem e depositam colágeno, estreitando ainda mais essa barreira. Fibroblastos inflamatórios secretam nuvens de proteínas sinalizadoras que atraem e reprogramam células imunes, muitas vezes empurrando-as para a tolerância em vez do ataque. Outros fibroblastos alteram seu próprio metabolismo para nutrir o tumor ou até apresentam fragmentos de proteínas tumorais para células T, por vezes auxiliando a imunidade e por vezes promovendo a supressão imune. Essa mistura complexa significa que eliminar bruscamente todos os fibroblastos pode ter efeito contrário; tratamentos futuros precisarão desarmar seletivamente os subtipos prejudiciais preservando ou até reforçando os protetores.
Células imunes transformadas em aliadas involuntárias
O sistema imune dentro dos tumores pancreáticos é igualmente complexo. Células supressoras derivadas de mieloides e macrófagos associados ao tumor são atraídos para o tumor por sinais vindos de fibroblastos e das próprias células cancerosas. Uma vez lá, eles retiram nutrientes necessários às células T citotóxicas, liberam fatores que atenuam a atividade imune e ajudam a formar novos vasos sanguíneos que nutrem o câncer. Populações chave de linfócitos também são remodeladas. Células T reguladoras se agrupam próximas às T citotóxicas e reduzem sua função por meio de moléculas de checkpoint e artifícios metabólicos. Células dendríticas, que deveriam ativar a imunidade antitumoral, são bloqueadas pelo estroma rígido e reprogramadas pelo acúmulo de ácidos graxos, passando a apresentar material tumoral de forma deficiente. Células assassinas naturais, normalmente aptas a reconhecer células estressadas, são silenciadas por sinais do tumor e do estroma. Juntas, essas alterações transformam uma infiltração imune potencialmente hostil em uma tolerante, explicando por que drogas de checkpoint isoladas raramente funcionam no câncer pancreático.
Genes, sinais e por que as terapias falham
No nível genético e molecular, os tumores pancreáticos são impulsionados por um conjunto característico de alterações, especialmente mutações em KRAS, TP53, CDKN2A e SMAD4. Alterações no número de cópias e mudanças epigenéticas reconfiguram ainda mais vias de crescimento, controle do ciclo celular e reparo do DNA. Essas alterações alimentam grandes cascatas de sinalização — como as vias MAPK e PI3K–AKT–mTOR — que impulsionam a proliferação e ajudam os tumores a se adaptar quando uma rota é bloqueada. Elas também influenciam como as células cancerosas reparam o DNA danificado, abrindo a porta para drogas como inibidores de PARP em tumores com defeitos específicos de reparo. Ao mesmo tempo, o estroma denso, o metabolismo anômalo e células com características de células-tronco cancerosas tornam os tumores intrinsecamente resistentes à quimioterapia e a fármacos direcionados, além de rápidos em desenvolver resistência adquirida.
Novas estratégias e o que vem a seguir
Em vez de confiar em uma única “bala mágica”, a revisão defende combinações racionais que enfrentem tanto as células cancerosas quanto seu ambiente protetor. Isso inclui associar inibidores de checkpoint a fármacos que remodelam fibroblastos ou esgotam células mieloides supressoras, engenhar células T ou células assassinas naturais para atingir tumores fibróticos, usar vacinas e abordagens baseadas em mRNA para melhorar o reconhecimento de alvos tumorais específicos e explorar vulnerabilidades no reparo de DNA ou na sinalização de KRAS. Ensaios clínicos iniciais dessas combinações, junto com perfis genéticos e imunes sofisticados, começam a identificar quais pacientes podem se beneficiar de cada estratégia. Para o leitor leigo, a mensagem chave é de esperança cautelosa: ao entender o câncer pancreático como um ecossistema complexo — em vez de apenas uma massa de células malignas — os pesquisadores estão finalmente montando planos terapêuticos multifacetados que podem tornar este câncer historicamente intratável mais responsivo ao tratamento.
Citação: Nagaraju, G.P., Nellipudi, H., Ganji, C. et al. Pancreatic ductal adenocarcinoma: integrating molecular insights for targeted interventions. Sig Transduct Target Ther 11, 165 (2026). https://doi.org/10.1038/s41392-026-02705-5
Palavras-chave: câncer de pâncreas, microambiente tumoral, imunoterapia, fibroblastos associados ao câncer, mutações em KRAS