Clear Sky Science · zh
特定干细胞程序与 CD112 免疫轴功能障碍驱动单体性 7 染色体相关的髓系肿瘤
为何这种血液问题重要
一些侵袭性血液癌具有一个令人费解的改变:患者在骨髓细胞中丢失了整条 7 号染色体的拷贝。这一缺陷称为单体性 7,与预后不良相关,但临床上仍缺乏针对性的治疗方法。本研究在基因和免疫信号层面上探查这些细胞内部发生的变化,揭示了一套特殊的干细胞程序和一个失调的免疫“刹车与油门”系统如何帮助这些癌症生长并逃避免疫防御。
骨髓干细胞的危险转变
骨髓增生异常综合征和急性髓系白血病是未成熟血细胞占据骨髓的疾病。作者将来自单体性 7 患者的骨髓样本与其他白血病患者和健康供体的样本进行比较。通过测定基因表达开关,他们发现单体性 7 细胞携带一种独特的“干性”程序:一组 49 个基因,使细胞保持自我更新的干细胞样状态,而不能成熟为正常血细胞。其中许多基因已被证明与较差的生存率或异常的能量代谢相关,这表明这种干细胞特征有助于解释单体性 7 肿瘤难以治疗的原因。
引导基因活性的隐性化学标记
研究小组接着研究了 DNA 甲基化,这是一种可以在不改变 DNA 序列的情况下使基因沉默或调节其活性的化学标记。使用高分辨率方法,他们显示单体性 7 骨髓具有特征性的甲基化“指纹”,许多区域比正常更强烈地带有标记。这些变化主要不位于基因起始位点,而是积聚在基因间增强子处——这些控制区像远端的调光开关。许多增强子在特定染色体上聚集,包括保留的那条 7 号染色体,这暗示着完好拷贝正在被重接线,而不是仅仅作为被动的残留。
关键基因的控制开关何时被重接线
因为增强子是转录因子(开启或关闭基因的蛋白)结合的停靠位点,研究者考察了哪些因子可能受到影响。他们发现多种同源盒蛋白(发育的主调节因子)的结合位点往往呈高甲基化状态。通过将这些化学图谱与公开的同源盒蛋白结合数据集结合,他们鉴定出一大类在单体性 7 病例中异常活跃的“HOX 靶基因”。其中许多与那组 49 个干性基因重叠。实验证实,至少有一个调控因子 PAX8 在某些增强子高甲基化时无法结合,这支持增强子化学改变有助于将细胞锁定为癌性干细胞样状态的观点。
骨髓中的失调免疫检查点
研究随后关注位于 7 号染色体上的 IKZF1 基因,该基因参与组织 DNA 的三维结构并调控其他基因。由于只有一份 7 号染色体拷贝,单体性 7 细胞产生较少的 IKZF1,并呈现出典型的“IKZF1 不足”基因模式。其中之一是 CD112,一种在细胞表面与免疫细胞对话的蛋白。研究者证明,IKZF1 正常情况下结合 CD112 启动子并对其加以抑制。当他们在健康干细胞中用 CRISPR 降低 IKZF1 时,CD112 水平上升,重现了患者样本中的情况。在来自单体性 7 患者的骨髓组织中,白血病细胞及异常前体细胞 CD112 呈强阳性,而正常样本仅见零星弱阳性染色。
白血病细胞如何解除自然杀伤细胞的武装
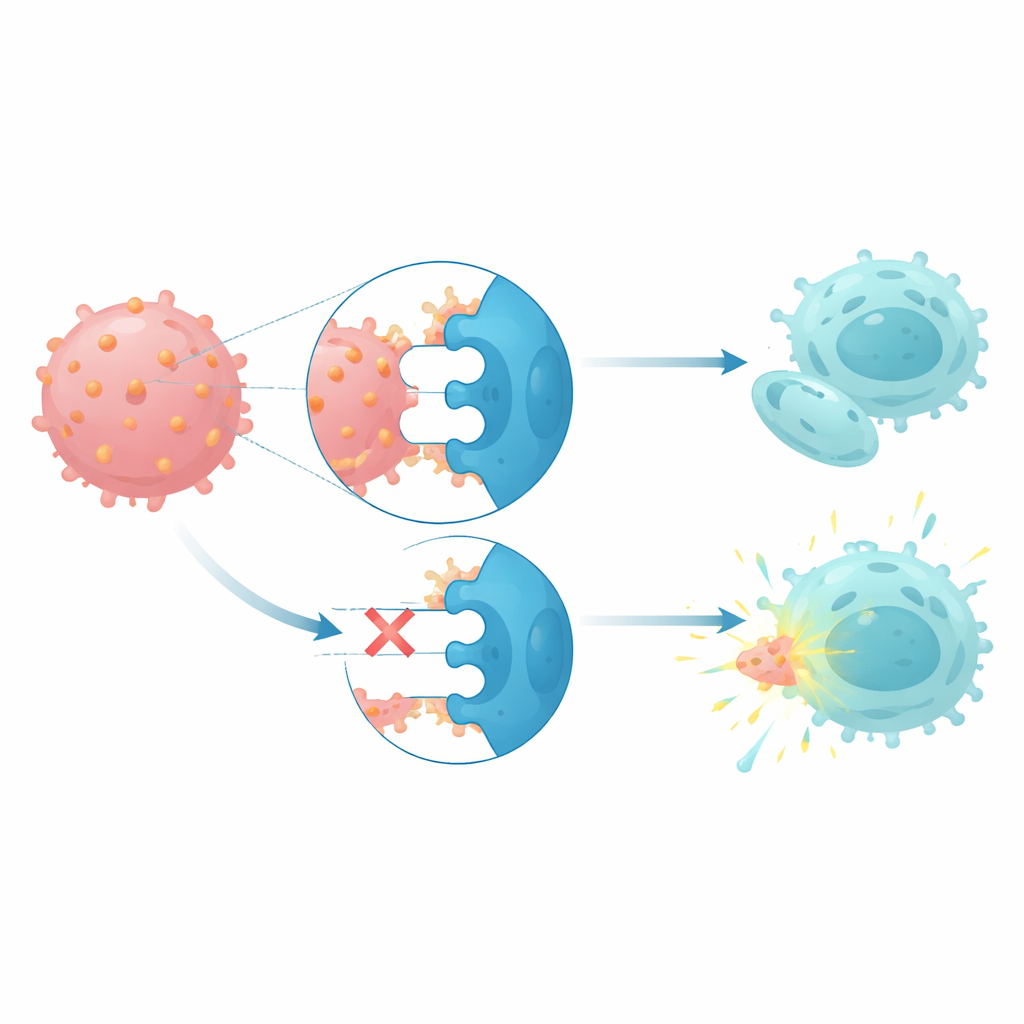
CD112 与自然杀伤细胞和 T 细胞上的三种受体相互作用:一个激活受体 DNAM1,以及两个抑制受体 TIGIT 和 PVRIG。在单体性 7 患者中,自然杀伤细胞和 T 细胞显示出抑制受体上调而激活受体下调的特征,符合免疫细胞被推向迟缓状态的模式。当健康的自然杀伤细胞与 CD112 高表达的白血病细胞共培养时,它们的 PVRIG 水平上升而 DNAM1 水平下降,表明与这些癌细胞的接触有助于重新编程免疫防御。功能性杀伤实验显示,阻断患者自然杀伤细胞上的 TIGIT 和 PVRIG 可恢复其裂解自身单体性 7 白血病细胞的能力,而单独阻断 CD112 效果较差。
这对未来治疗的意义
总体而言,这些发现将单体性 7 髓系肿瘤描绘成由干细胞样基因程序驱动并受 CD112 基于的免疫检查点失调保护的癌症。通过将 7 号染色体丢失与增强子变化、主调控因子的改变以及重接线的 CD112–TIGIT–PVRIG–DNAM1 轴联系起来,该研究提示,阻断抑制受体 TIGIT 和 PVRIG 的药物,可能与现有的 DNA 甲基化治疗联合使用,能够帮助患者自身的自然杀伤细胞识别并攻击这些难治的癌症。
引用: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
关键词: 单体性 7, 髓系肿瘤, 急性髓系白血病, 免疫检查点, 自然杀伤细胞