Clear Sky Science · de
Ein spezifisches Stammzellprogramm und Störungen der CD112-immunologischen Achse zugrunde liegend bei mit Monosomie 7 assoziierten myeloischen Neoplasien
Warum dieses Blutproblem wichtig ist
Einige aggressive Blutkrebserkrankungen teilen eine rätselhafte Veränderung: Bei betroffenen Patientinnen und Patienten geht in den Knochenmarkzellen eine komplette Kopie von Chromosom 7 verloren. Dieser Defekt, Monosomie 7 genannt, ist mit schlechten Prognosen verbunden, doch gezielte Therapien fehlen bislang. Die vorliegende Studie untersucht, was in diesen Zellen auf Ebene der Gene und Immun‑Signale vor sich geht, und zeigt, wie ein spezielles Stammzellprogramm und ein fehlerhaftes immunologisches „Bremse‑und‑Gas“-System dem Krebswachstum Vorschub leisten und dem Körper die Abwehr erschweren.
Eine riskante Verschiebung in Knochenmarkstammzellen
Myelodysplastische Syndrome und akute myeloische Leukämie sind Erkrankungen, bei denen unreife Blutzellen das Knochenmark dominieren. Die Autoren verglichen Knochenmarkproben von Patienten mit Monosomie 7 mit Proben anderer Leukämiepatienten und gesunden Spendern. Durch die Analyse, welche Gene ein- oder ausgeschaltet sind, stellten sie fest, dass Monosomie‑7‑Zellen ein charakteristisches „Stemness“-Programm trugen: eine Gruppe von 49 Genen, die Zellen in einem selbst erneuernden, stamzellenähnlichen Zustand halten, statt ihre Reifung zu normalen Blutzellen zuzulassen. Viele dieser Gene waren bereits mit schlechterem Überleben oder ungewöhnlichem Energiestoffwechsel bei Blutkrebserkrankungen verknüpft, was nahelegt, dass dieses Stammzellmuster dazu beiträgt, warum Monosomie‑7‑Neoplasien so schwer behandelbar sind.
Versteckte chemische Markierungen, die Genaktivität steuern
Als Nächstes betrachtete das Team die DNA‑Methylierung, eine chemische Markierung, die Genaktivität stummschalten oder verändern kann, ohne die DNA-Buchstaben selbst zu ändern. Mit einer hochauflösenden Methode zeigten sie, dass das Knochenmark mit Monosomie 7 einen charakteristischen Methylierungs‑„Fingerabdruck“ aufwies, mit vielen Regionen, die stärker markiert waren als normal. Diese Veränderungen lagen nicht vorwiegend an Genanfangsstellen, sondern häuften sich in intergenen Enhancern, Kontrollregionen, die wie entfernte Dimmer funktionieren. Viele dieser Enhancer konzentrierten sich auf bestimmten Chromosomen, einschließlich der verbleibenden Kopie von Chromosom 7, was darauf hindeutet, dass die intakte Kopie umverdrahtet wird, statt nur als passives Relikt zu fungieren.
Wenn Schaltstellen für Schlüsselgene umverdrahtet werden
Da Enhancer Andockstellen für Transkriptionsfaktoren sind, die Gene an- und ausschalten, fragten die Forschenden, welche Faktoren betroffen sein könnten. Sie fanden, dass Bindungsstellen für mehrere Homeobox‑Proteine, zentrale Entwicklungsregulatoren, häufig hypermethyliert waren. Durch die Kombination dieser chemischen Karten mit öffentlichen Datensätzen zu Homeobox‑Proteinbindungsstellen identifizierten sie eine große Gruppe von „HOX‑Zielgenen“, die in Monosomie‑7‑Fällen abnormal aktiv waren. Viele davon überschneiden sich mit dem 49‑Gen‑Stammzellprogramm. Experimente bestätigten, dass zumindest einer dieser Regulatoren, PAX8, bestimmte Enhancer nicht mehr binden konnte, wenn diese hypermethyliert waren, und stützen damit die Idee, dass veränderte Enhancer‑Chemie dazu beiträgt, Zellen in einem krebsartigen, stamzellähnlichen Zustand zu verankern.
Ein defekter Immun-Checkpoint im Knochenmark
Die Arbeit wandte sich dann IKZF1 zu, einem Gen auf Chromosom 7, das an der Organisation der 3D‑DNA‑Struktur und der Regulation anderer Gene beteiligt ist. Mit nur einer Kopie von Chromosom 7 produzierten Monosomie‑7‑Zellen weniger IKZF1 und zeigten ein Genmuster, das für „IKZF1‑Insuffizienz“ typisch ist. Darunter war CD112, ein Protein an der Zelloberfläche, das mit Immunzellen kommuniziert. Die Forschenden zeigten, dass IKZF1 normalerweise an den CD112‑Promotor bindet und dessen Expression unter Kontrolle hält. Wenn sie IKZF1 in gesunden Stammzellen mittels CRISPR reduzierten, stiegen die CD112‑Spiegel an — ein Muster, das den Beobachtungen bei Patienten entsprach. In Knochenmarkgewebe von Personen mit Monosomie 7 zeigten Leukämiezellen und abnorme Vorläufer starke CD112‑Positivität, während normale Proben nur vereinzelt schwache Färbung zeigten.
Wie Leukämiezellen natürliche Killerzellen lahmlegen
CD112 interagiert mit drei Rezeptoren auf natürlichen Killerzellen und T‑Zellen: einem aktivierenden Rezeptor namens DNAM1 und zwei inhibitorischen Rezeptoren, TIGIT und PVRIG. Bei Patienten mit Monosomie 7 zeigten natürliche Killerzellen und T‑Zellen höhere Spiegel der inhibitorischen Rezeptoren und niedrigere Spiegel des aktivierenden Rezeptors — ein Muster, das mit einer in Richtung Erschöpfung gedrängten Immunzellpopulation übereinstimmt. Wenn gesunde natürliche Killerzellen mit CD112‑reichen Leukämiezellen zusammen kultiviert wurden, stiegen ihre PVRIG‑Spiegel und DNAM1‑Spiegel fielen, was darauf hindeutet, dass der Kontakt mit diesen Krebszellen die Immunabwehr umprogrammiert. Funktionelle Abtötungsassays zeigten, dass die Blockade sowohl von TIGIT als auch von PVRIG auf Patienten‑NK‑Zellen deren Fähigkeit wiederherstellte, die eigenen Monosomie‑7‑Leukämiezellen zu lysieren, während die Blockade von CD112 allein weniger wirksam war.
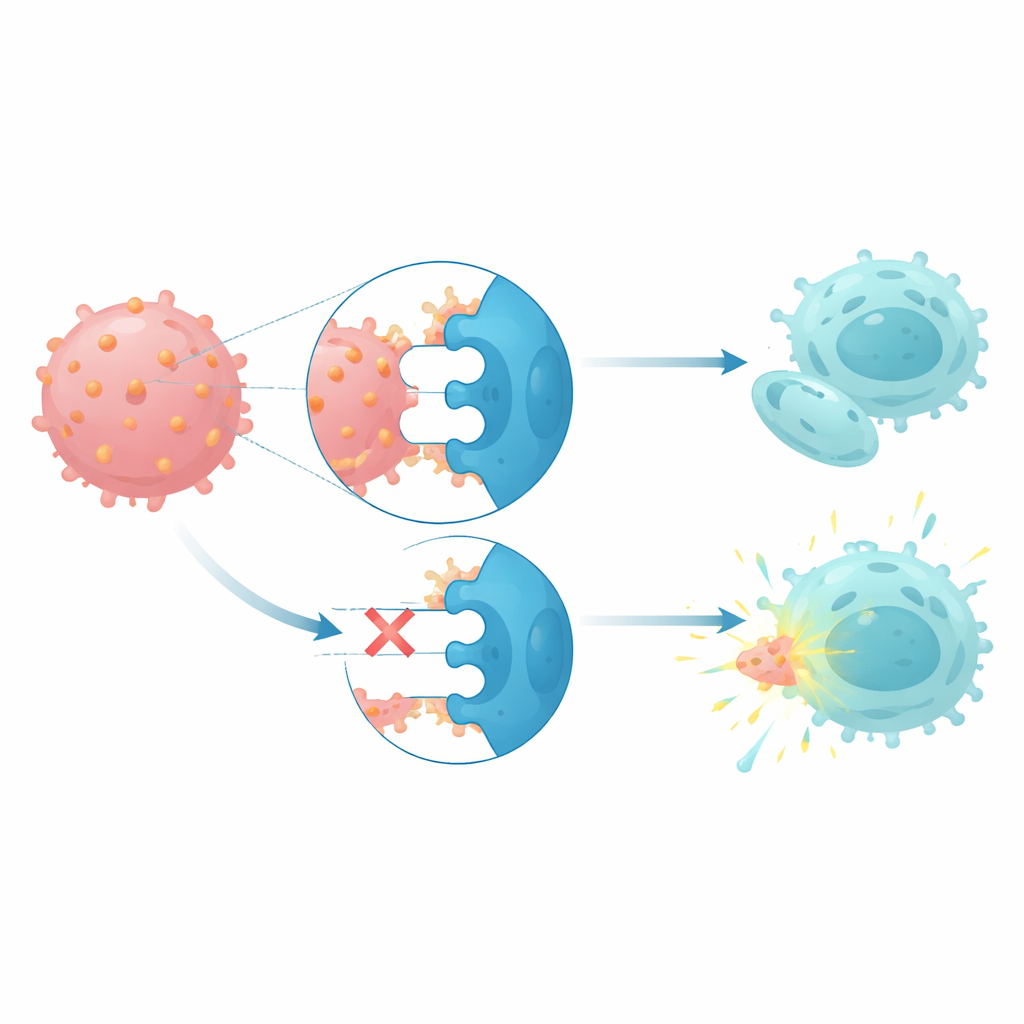
Was das für zukünftige Therapien bedeuten könnte
Zusammen zeichnen diese Befunde das Bild von Monosomie‑7‑assoziierten myeloischen Neoplasien als durch ein stamzellähnliches Genprogramm getriebene und durch eine verzerrte CD112‑basierte Immun‑Checkpoint‑Achse geschützte Krebserkrankungen. Indem sie den Verlust von Chromosom 7 mit Enhancer‑Veränderungen, veränderten Master‑Regulatoren und einer umverdrahteten CD112–TIGIT–PVRIG–DNAM1‑Achse verbinden, legt die Studie nahe, dass Wirkstoffe, die die inhibitorischen Rezeptoren TIGIT und PVRIG blockieren — möglicherweise in Kombination mit vorhandenen DNA‑Methylierungs‑Therapien — den körpereigenen natürlichen Killerzellen helfen könnten, diese sonst schwer behandelbaren Tumoren zu erkennen und anzugreifen.
Zitation: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Schlüsselwörter: Monosomie 7, myeloische Neoplasie, akute myeloische Leukämie, Immun-Checkpoint, natürliche Killerzellen