Clear Sky Science · ja
7番染色体単一欠失に関連する骨髄性腫瘍の基盤となる特定の幹細胞プログラムとCD112免疫軸の機能不全
この血液の問題が重要な理由
一部の侵襲的な血液がんでは不可解な変化が共通して観察されます:患者の骨髄細胞が染色体7の一コピーを失っていることです。この欠損は単一欠失(monosomy 7)と呼ばれ、予後不良と関連しますが、依然として標的治療は限られています。本研究は、これらの細胞内で遺伝子と免疫シグナルのレベルで何が起きているかを解き明かし、特定の幹細胞プログラムと故障した免疫の「ブレーキとアクセル」システムが、腫瘍の増殖と免疫回避をどのように助けているかを明らかにします。
骨髄幹細胞に生じる危険なシフト
骨髄異形成症候群と急性骨髄性白血病は、未熟な血球が骨髄を占拠する疾患です。著者らは単一欠失を持つ患者の骨髄サンプルを、他の白血病患者や健常ドナーのサンプルと比較しました。どの遺伝子がオン・オフになっているかを解析したところ、単一欠失細胞は特有の「幹性(stemness)」プログラム、すなわち細胞を成熟した正常血球に分化させず自己複製する幹様状態に保つ49遺伝子セットを有していることがわかりました。これらの遺伝子の多くは、血液腫瘍における生存率不良や異常な代謝と既に結びついており、この幹細胞パターンが単一欠失腫瘍が治療困難である理由の一端を説明していることが示唆されます。
遺伝子活性を導く隠れた化学的標識
続いてチームはDNAメチル化、すなわちDNA配列を変えずに遺伝子の働きを抑制・変更しうる化学的なタグを調べました。高解像度の手法を用いて、単一欠失の骨髄は特徴的なメチル化の「指紋」を示し、多くの領域で通常より強くタグ付けされていることを示しました。これらの変化は主に遺伝子の開始部位に集中するのではなく、むしろ遠隔の調節スイッチとして働くイントラジェニックでないエンハンサーに蓄積していました。これらのエンハンサーの多くは特定の染色体にクラスターを形成しており、残存する7番染色体コピー上にも集中していて、単に受動的に残っているのではなく再配線されている可能性を示唆します。
重要遺伝子の制御スイッチが再配線されるとき
エンハンサーは転写因子が結合するドッキングサイトであるため、どの因子が影響を受けているかを調べました。いくつかのホメオボックス(homeobox)タンパク質、発生のマスターレギュレーターの結合部位がしばしば過剰にメチル化されていることを見出しました。これらの化学的マップをホメオボックスタンパク質の既公開データと組み合わせることで、単一欠失例で異常に活性化している大規模な「HOX標的」遺伝子群を特定しました。これらの多くは49遺伝子の幹性プログラムと重複していました。実験により、少なくとも1つの調節因子であるPAX8がエンハンサーの過剰メチル化により特定のエンハンサーに結合できなくなることが確認され、エンハンサーの化学的変化が細胞を癌性の幹様状態に固定するのを助けるという考えを支持しました。
骨髄内の壊れた免疫チェックポイント
研究は次に、DNAの3次元構造を整理し他の遺伝子を制御する7番染色体上の遺伝子IKZF1に注目しました。7番染色体が1コピーしかないことで、単一欠失細胞はIKZF1の発現が低下し、「IKZF1不足」に典型的な遺伝子パターンを示しました。その中には細胞表面に存在し免疫細胞とやり取りするタンパク質CD112が含まれていました。研究者らは、IKZF1が通常CD112のプロモーターに結合してその発現を抑えていることを証明しました。健常幹細胞でCRISPRを用いてIKZF1を減らすとCD112レベルが上昇し、患者で観察された現象が再現されました。単一欠失患者の骨髄組織では、白血病芽球や異常な前駆細胞が強くCD112陽性である一方、正常サンプルでは散在する弱い染色を示すのみでした。
白血病細胞がナチュラルキラー細胞を無力化する仕組み
CD112はナチュラルキラー(NK)細胞やT細胞上の3つの受容体と相互作用します:活性化受容体のDNAM1と、抑制的受容体のTIGITおよびPVRIGです。単一欠失患者では、NK細胞やT細胞が抑制的受容体を高発現し活性化受容体を低発現する傾向があり、免疫細胞が鈍化した状態に追い込まれているパターンと一致します。健常なNK細胞をCD112高発現の白血病細胞と共培養すると、NK細胞のPVRIGレベルが上昇しDNAM1レベルが低下し、これらの癌細胞との接触が免疫防御を再プログラムすることが示唆されました。機能的な細胞傷害アッセイでは、患者由来のNK細胞でTIGITとPVRIGの両方を遮断すると単一欠失白血病芽球に対する溶解能が回復しましたが、CD112単独の遮断は効果が小さいことが示されました。
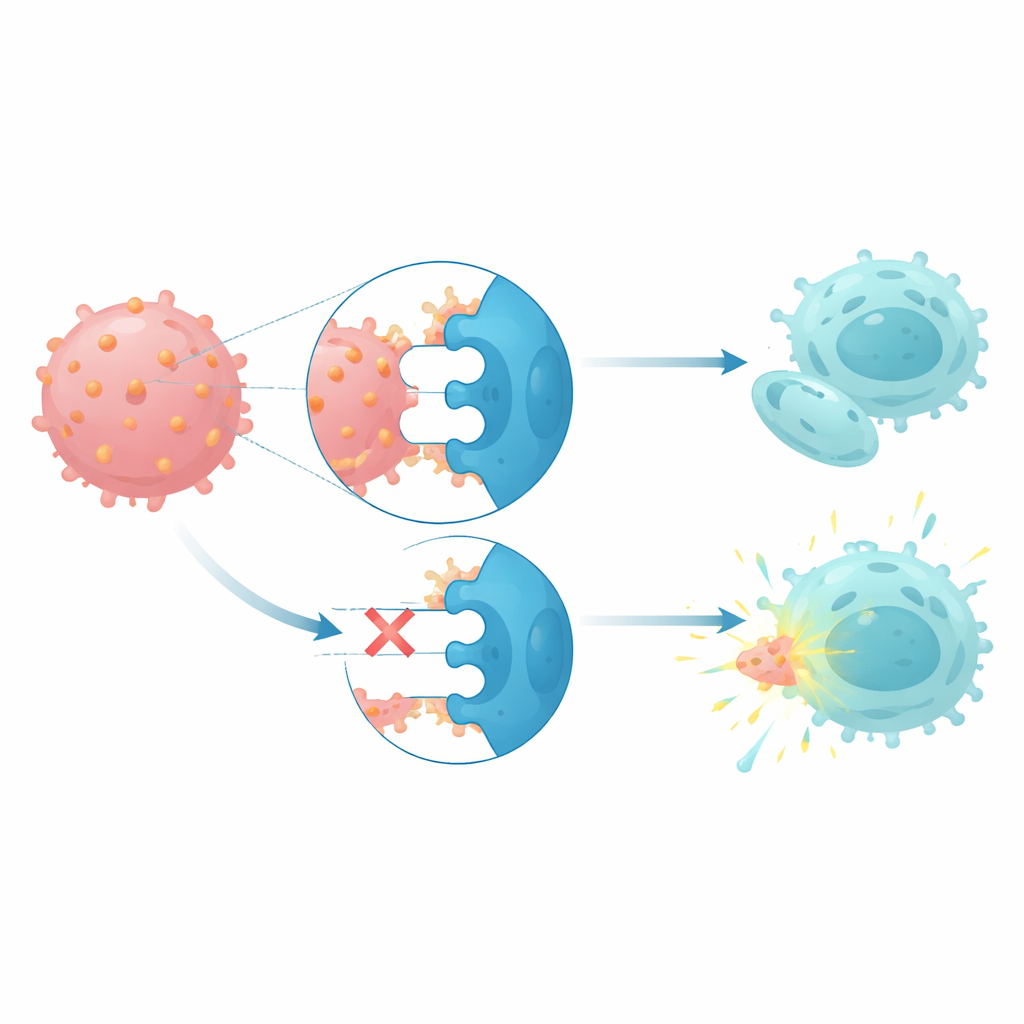
将来の治療にとっての意義
これらの知見を総合すると、単一欠失を伴う骨髄性腫瘍は幹様の遺伝子プログラムによって駆動され、歪んだCD112ベースの免疫チェックポイントによって保護されている癌と描写できます。染色体7の喪失をエンハンサーの変化、マスターレギュレーターの異常、そして再配線されたCD112–TIGIT–PVRIG–DNAM1軸に結びつけることで、本研究は抑制受容体であるTIGITとPVRIGを阻害する薬剤が、既存のDNAメチル化療法と併用することで、患者自身のNK細胞がこれらの治療困難な腫瘍を認識し攻撃するのを助ける可能性を示唆します。
引用: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
キーワード: 7番染色体単一欠失, 骨髄性腫瘍, 急性骨髄性白血病, 免疫チェックポイント, ナチュラルキラー細胞