Clear Sky Science · ar
برنامج خلوي جذعي محدد واضطرابات محور مناعي CD112 كعوامل أساسية في الأورام النخاعية المرتبطة بوجود نسخة واحدة من الصبغي 7
لماذا تهم هذه المشكلة الدموية
تشارك بعض سرطانات الدم العدوانية تغيرًا محيرًا: يفقد المرضى نسخة كاملة من الصبغي 7 في خلايا نخاع العظم. هذا العطب، المسمى منصوصومية 7، يرتبط بنتائج سيئة، ومع ذلك لا يملك الأطباء علاجات موجهة له بعد. تستقصي هذه الدراسة ما يحدث داخل هذه الخلايا على مستوى الجينات والإشارات المناعية، كاشفةً كيف يساعد برنامج جذعي خاص ونظام مناعي معطوب يشبه "الفرامل والبنزين" هذه الأورام على النمو والتهرب من دفاعات الجسم.
تحول محفوف بالمخاطر في خلايا جذع النخاع
تعد المتلازمات النقوية الخبيثة واللوكيميا النخاعية الحادة أمراضًا تهيمن فيها الخلايا الدموية غير الناضجة على نخاع العظم. قارن المؤلفون عينات نخاع من مرضى يعانون منصوصومية 7 مع عينات من مرضى لَوْكيميا آخرين والمتبرعين الأصحاء. بقراءة أي الجينات كانت مفعلة أو مطموسة، وجدوا أن خلايا منصوصومية 7 تحمل برنامج "جذعي" مميزًا: مجموعة من 49 جينًا تحافظ على الخلايا في حالة تجدد ذاتي وشبيهة بالجذع بدلاً من أن تنضج إلى خلايا دموية طبيعية. وقد رُبط الكثير من هذه الجينات سابقًا ببقاء أسوأ أو استخدام طاقي غير معتاد في سرطانات الدم، ما يشير إلى أن نمط الخلايا الجذعية هذا قد يفسر سبب صعوبة علاج الأورام المصاحبة لمنصوصومية 7.
علامات كيميائية مخفية توجه نشاط الجينات
نظر الفريق بعد ذلك إلى مثيلة الحمض النووي، وهي علامة كيميائية يمكنها كتم أو تعديل نشاط الجينات دون تغيير حروف الدنا نفسها. باستخدام طريقة عالية الدقة، أظهروا أن نخاع العظم في حالات منصوصومية 7 يمتلك "بصمة" مثيلية مميزة، مع العديد من المناطق الموسومة بكثافة أكبر من الطبيعي. لم تكن هذه التغييرات مركزة أساسًا عند مواقع بدء الجينات، بل تراكمت في المعززات البينية الجينية، مناطق تحكم تعمل كمفاتيح تعتيم بعيدة. كانت العديد من هذه المعززات متجمعة على صبغيات محددة، بما في ذلك النسخة المتبقية من الصبغي 7، مما يوحي بأن النسخة السليمة تُعاد توصيلها بدلاً من أن تظل مجرد أثر سلبي.
عندما تُعاد توجيه مفاتيح التحكم لجينات محورية
بما أن المعززات هي مواقع ارتكاز لعوامل النسخ، البروتينات التي تشغّل أو تطفئ الجينات، تساءل الباحثون أي العوامل قد تتأثر. وجدوا أن مواقع ارتباط لعدة بروتينات هوميو بوكس، منظِّمات رئيسية للتطور، كانت غالبًا مفرطة المثيلة. من خلال دمج هذه الخرائط الكيميائية مع مجموعات بيانات عامة لارتباط بروتينات الهوميوبوكس، حددوا مجموعة كبيرة من جينات "هدف HOX" التي كانت مفرطة النشاط في حالات منصوصومية 7. وتداخل العديد منها مع برنامج الجذعية المكوّن من 49 جينًا. أكدت التجارب أن واحدًا على الأقل من هؤلاء المنظِّمين، PAX8، فشل في الارتباط ببعض المعززات عندما كانت مفرطة المثيلة، مما يدعم فكرة أن كيمياء المعزز المتغيرة تساعد في قفل الخلايا في حالة شبيهة بالجذع سرطانية.
نقطة فحص مناعية معطوبة في نخاع العظم
تحولت الدراسة بعد ذلك إلى IKZF1، الجين الموجود على الصبغي 7 والذي يساعد في تنظيم البنية ثلاثية الأبعاد للدنا وتنظيم جينات أخرى. مع وجود نسخة واحدة فقط من الصبغي 7، أنتجت خلايا منصوصومية 7 كمية أقل من IKZF1 وأظهرت نمط جينيًا مميزًا لـ"نقص IKZF1". من بين هذه الجينات كان CD112، بروتين على سطح الخلايا يتواصل مع الخلايا المناعية. برهن الباحثون أن IKZF1 عادةً يربط مُروِّج CD112 ويكبّحه. عندما خفضوا IKZF1 في الخلايا الجذعية السليمة باستخدام كريسبر، ارتفعت مستويات CD112، مكررة ما لاحظوه في المرضى. في أنسجة نخاع من أشخاص مصابين بمنصوصومية 7، كانت الخلايا اللوكيمية والطوريات الشاذة موجبة بقوة لـCD112، في حين أظهرت العينات الطبيعية بقع تلوين ضعيفة ومبعثرة فقط.
كيف تعطل الخلايا اللوكيمية الخلايا القاتلة الطبيعية
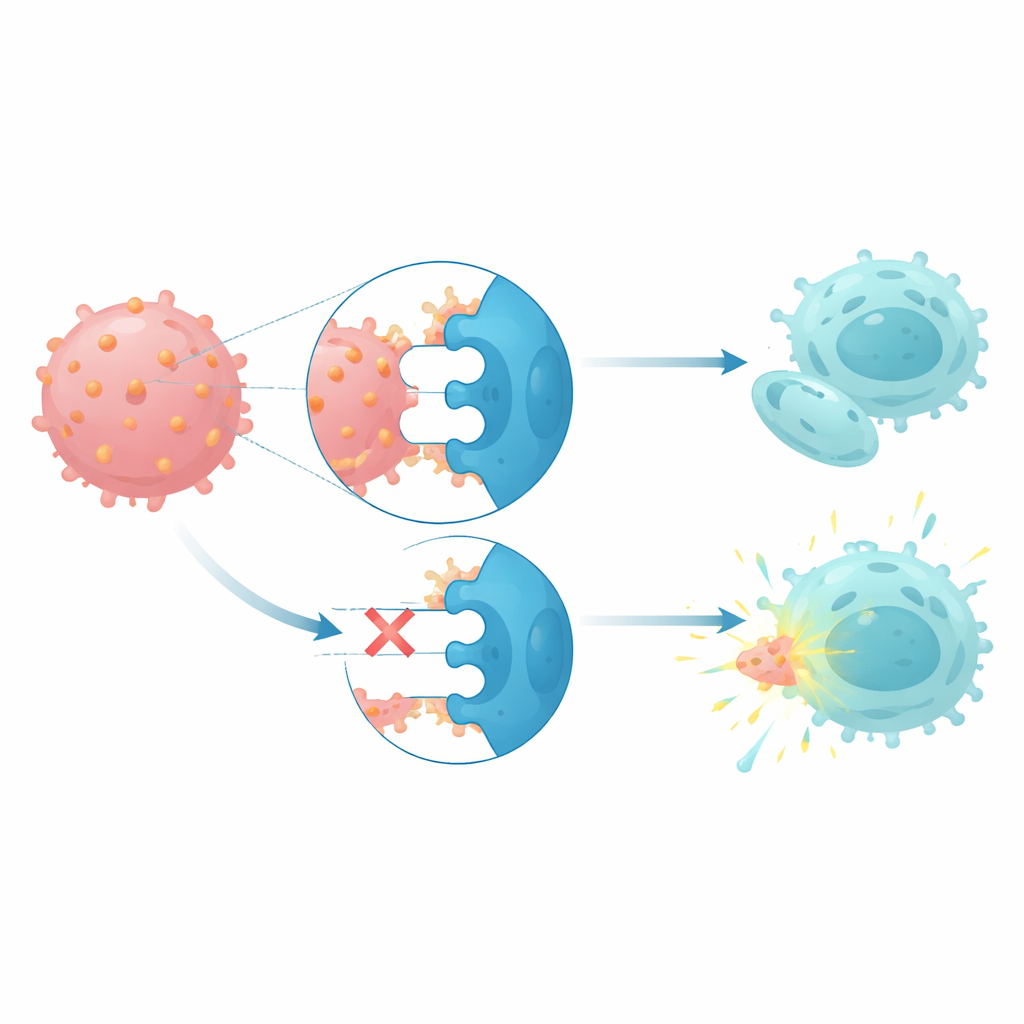
يتفاعل CD112 مع ثلاثة مستقبلات على الخلايا القاتلة الطبيعية والخلايا التائية: مستقبل منشط يسمى DNAM1 ومُستقبلان مثبطان، TIGIT وPVRIG. في مرضى منصوصومية 7، عرضت الخلايا القاتلة الطبيعية والخلايا التائية مستويات أعلى من المستقبلات المثبطة ومستويات أقل من المستقبل المنشط، نمط يتوافق مع دفع الخلايا المناعية إلى حالة خمودية. عندما تم استزراع خلايا قاتلة طبيعية سليمة مع خلايا لَوْكيمية عالية CD112، ارتفعت مستويات PVRIG وانخفضت مستويات DNAM1، مما يوحي أن الاتصال مع هذه الخلايا السرطانية يساعد في إعادة برمجة الدفاع المناعي. أظهرت اختبارات القتل الوظيفي أن حجب كل من TIGIT وPVRIG على خلايا قاتلة طبيعية من المرضى أعاد قدرتها على تحلل الخلايا اللوكيمية الخاصة بمنصوصومية 7، بينما كان حجب CD112 بمفرده أقل فعالية.
ما الذي قد يعنيه هذا للعلاج المستقبلي
معًا، تصوّر هذه النتائج أورام النخاع المرتبطة بمنصوصومية 7 كأورام تُقودها شبكة جينية شبيهة بالخلايا الجذعية وتحصنها نقطة فحص مناعية مشوّهة قائمة على CD112. بربط فقدان الصبغي 7 بتغيرات في المعززات، وتحوّر المنظِّمات الرئيسية، وإعادة توصيل محور CD112–TIGIT–PVRIG–DNAM1، تشير الدراسة إلى أن عقاقيرًا تحجب المستقبلات المثبطة TIGIT وPVRIG، ربما إلى جانب علاجات مثيلة الدنا المستخدَمة حاليًا، قد تساعد خلايا المرضى القاتلة الطبيعية على التعرف على هذه الأورام الشديدة الصعوبة ومهاجمتها.
الاستشهاد: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
الكلمات المفتاحية: منصوصومية 7, ورم نخاعي, اللوكيميا النخاعية الحادة, نقطة فحص مناعي, الخلايا القاتلة الطبيعية