Clear Sky Science · it
Un programma specifico di cellule staminali e disfunzioni dell’asse immunologico CD112 alla base delle neoplasie mieloidi associate a monosomia 7
Perché questo problema ematologico conta
Alcuni tumori del sangue aggressivi condividono una modifica enigmatica: i pazienti perdono un’intera copia del cromosoma 7 nelle cellule del midollo osseo. Questo difetto, chiamato monosomia 7, è associato a esiti sfavorevoli, eppure i medici non dispongono ancora di terapie mirate. Questo studio indaga cosa accade all’interno di queste cellule a livello di geni e segnali immunitari, rivelando come un programma staminale particolare e un sistema immunitario «freno-e-acceleratore» difettoso favoriscano la crescita del tumore e la sua fuga dalle difese dell’organismo.
Un cambiamento rischioso nelle cellule staminali del midollo
Le sindromi mielodisplastiche e la leucemia mieloide acuta sono malattie in cui cellule ematiche immature prendono il sopravvento nel midollo osseo. Gli autori hanno confrontato campioni di midollo da pazienti con monosomia 7 con campioni di altri pazienti leucemici e donatori sani. Leggendo quali geni erano attivi o inattivi, hanno scoperto che le cellule con monosomia 7 presentavano un distinto programma di «staminalità»: un insieme di 49 geni che mantengono le cellule in uno stato autorinnovante, simile a quello staminale, anziché permettere loro di maturare in cellule del sangue normali. Molti di questi geni erano già stati associati a una sopravvivenza peggiore o a un metabolismo energetico anomalo nei tumori ematici, suggerendo che questo profilo di cellule staminali contribuisca a spiegare perché le neoplasie con monosomia 7 sono così difficili da trattare.
Marchi chimici nascosti che indirizzano l’attività genica
Il gruppo ha poi esaminato la metilazione del DNA, un’etichetta chimica che può silenziare o modificare l’attività genica senza cambiare le lettere del DNA. Usando un metodo ad alta risoluzione, hanno mostrato che il midollo con monosomia 7 possedeva un «impronta» di metilazione caratteristica, con molte regioni più pesantemente marcate rispetto al normale. Questi cambiamenti non si concentravano principalmente nei siti di inizio dei geni, ma si accumulavano negli enhancers intergenici, regioni di controllo che agiscono come dimmer remoti. Molti di questi enhancers si raggruppavano su cromosomi specifici, inclusa la copia rimanente del cromosoma 7, suggerendo che la copia intatta venga riorganizzata piuttosto che fungere semplicemente da residuo passivo.
Quando gli interruttori di controllo dei geni chiave vengono riorganizzati
Poiché gli enhancers sono siti di ancoraggio per i fattori di trascrizione, le proteine che accendono o spengono i geni, i ricercatori hanno indagato quali fattori potessero essere interessati. Hanno trovato che i siti di legame per diversi fattori omeobox, regolatori master dello sviluppo, erano spesso ipermetilati. Combinando queste mappe chimiche con dataset pubblici di legame dei fattori omeobox, hanno identificato un ampio gruppo di geni «bersaglio HOX» anormalmente attivi nei casi con monosomia 7. Molti di questi si sovrapponevano al programma di 49 geni associato alla staminalità. Esperimenti hanno confermato che almeno uno di questi regolatori, PAX8, non riusciva a legare certi enhancers quando erano ipermetilati, a sostegno dell’idea che la chimica alterata degli enhancer contribuisca a bloccare le cellule in uno stato tumorale simile alle staminali.
Un checkpoint immunitario compromesso nel midollo
Lo studio si è poi concentrato su IKZF1, un gene sul cromosoma 7 che aiuta a organizzare la struttura 3D del DNA e a regolare altri geni. Con una sola copia del cromosoma 7, le cellule con monosomia 7 producono meno IKZF1 e mostrano un profilo genico tipico di «insufficienza di IKZF1». Tra questi geni figura CD112, una proteina di superficie che comunica con le cellule immunitarie. I ricercatori hanno dimostrato che IKZF1 lega normalmente il promotore di CD112 e ne mantiene i livelli sotto controllo. Quando hanno ridotto IKZF1 in cellule staminali sane usando CRISPR, i livelli di CD112 sono aumentati, rispecchiando quanto osservato nei pazienti. Nel midollo di persone con monosomia 7, i blasti leucemici e i precursori anomali risultavano fortemente positivi per CD112, mentre nei campioni normali si osservava solo una colorazione debole e sparsa.
Come le cellule leucemiche disarmano le natural killer
CD112 interagisce con tre recettori su cellule natural killer e cellule T: un recettore attivante chiamato DNAM1 e due recettori inibitori, TIGIT e PVRIG. Nei pazienti con monosomia 7, le cellule natural killer e le cellule T esprimevano livelli più alti dei recettori inibitori e livelli più bassi di quello attivante, un profilo coerente con cellule immunitarie spinte verso uno stato ipofunzionale. Quando cellule natural killer sane sono state co-coltivate con cellule leucemiche ad alta espressione di CD112, i loro livelli di PVRIG aumentavano e quelli di DNAM1 diminuivano, suggerendo che il contatto con queste cellule tumorali contribuisca a riprogrammare le difese immunitarie. Test funzionali di citotossicità hanno mostrato che il blocco simultaneo di TIGIT e PVRIG sulle cellule natural killer dei pazienti ristabiliva la loro capacità di lisare i blasti leucemici con monosomia 7 del paziente stesso, mentre il blocco di CD112 da solo era meno efficace.
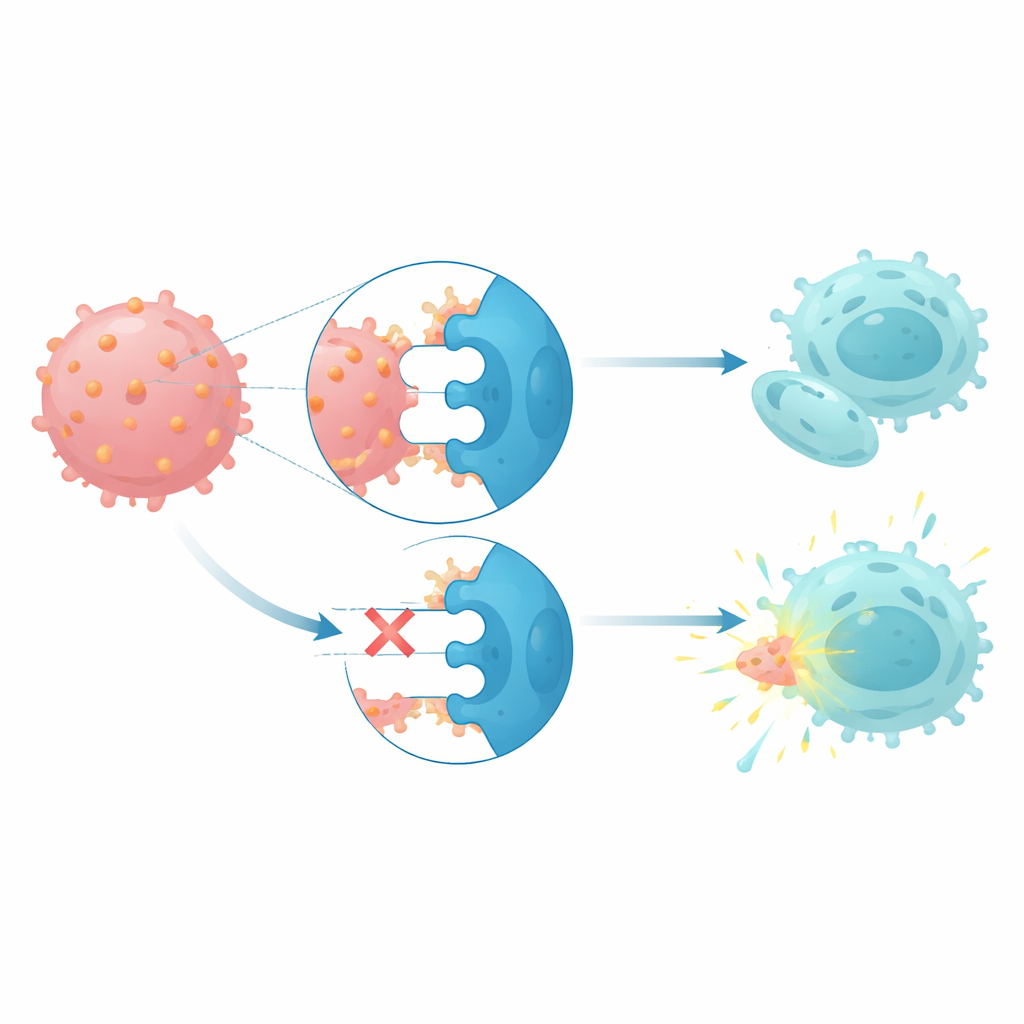
Cosa potrebbe significare per trattamenti futuri
Nel complesso, questi risultati descrivono le neoplasie mieloidi con monosomia 7 come tumori guidati da un programma genico di tipo staminale e protetti da un checkpoint immunitario distorto basato su CD112. Collegando la perdita del cromosoma 7 a cambiamenti negli enhancer, a regolatori master alterati e a un asse CD112–TIGIT–PVRIG–DNAM1 riorganizzato, lo studio suggerisce che farmaci che bloccano i recettori inibitori TIGIT e PVRIG, eventualmente in combinazione con le terapie attuali che modulano la metilazione del DNA, potrebbero aiutare le cellule natural killer dei pazienti a riconoscere e attaccare questi tumori altrimenti difficili da trattare.
Citazione: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Parole chiave: monosomia 7, neoplasia mieloide, leucemia mieloide acuta, checkpoint immunitario, cellule natural killer