Clear Sky Science · fr
Un programme spécifique de cellules souches et des dysfonctionnements de l’axe immunologique CD112 sous-tendant les néoplasmes myéloïdes associés à la monosomie 7
Pourquoi ce trouble sanguin importe
Certaines hémopathies agressives partagent une anomalie intrigante : les patients perdent une copie entière du chromosome 7 dans leurs cellules de la moelle osseuse. Ce défaut, nommé monosomie 7, est associé à un mauvais pronostic, et pourtant les cliniciens manquent encore de traitements ciblés. Cette étude explore ce qui se passe à l’intérieur de ces cellules au niveau des gènes et des signaux immunitaires, révélant comment un programme spécifique de cellules souches et un système immunitaire « frein-et‑accélérateur » défaillant favorisent la croissance de ces cancers et leur échappement aux défenses de l’organisme.
Un basculement risqué dans les cellules souches de la moelle
Les syndromes myélodysplasiques et la leucémie myéloïde aiguë sont des maladies dans lesquelles des cellules sanguines immatures envahissent la moelle osseuse. Les auteurs ont comparé des prélèvements de moelle de patients porteurs de monosomie 7 à des échantillons d’autres patients leucémiques et de donneurs sains. En lisant quels gènes étaient activés ou réprimés, ils ont constaté que les cellules monosomie 7 présentaient un programme distinct de « stemness » : un ensemble de 49 gènes qui maintiennent les cellules dans un état auto‑renouvelant et semblable à une cellule souche au lieu de les laisser maturer en cellules sanguines normales. Nombre de ces gènes avaient déjà été associés à une survie plus médiocre ou à des usages énergétiques atypiques dans les cancers hématologiques, suggérant que ce profil de cellules souches contribue à expliquer la résistance thérapeutique des néoplasmes monosomie 7.
Des marques chimiques cachées qui orientent l’activité génique
L’équipe a ensuite examiné la méthylation de l’ADN, une étiquette chimique qui peut silencier ou modifier l’activité des gènes sans changer la séquence d’ADN elle‑même. À l’aide d’une méthode haute résolution, ils ont montré que la moelle monosomie 7 présentait une « empreinte » de méthylation caractéristique, avec de nombreuses régions plus fortement marquées que la normale. Ces modifications ne se trouvaient pas principalement au niveau des sites de départ des gènes, mais s’accumulaient plutôt dans des enhancers intergéniques, des régions de contrôle qui agissent comme des variateurs à distance. Beaucoup de ces enhancers se regroupaient sur des chromosomes spécifiques, y compris la copie restante du chromosome 7, suggérant que la copie intacte est reconfigurée plutôt que de simplement rester un reliquat passif.
Quand les interrupteurs de contrôle de gènes clés sont reconfigurés
Parce que les enhancers sont des sites d’ancrage pour les facteurs de transcription, les protéines qui allument ou éteignent les gènes, les chercheurs ont cherché quels facteurs pouvaient être affectés. Ils ont découvert que les sites de liaison pour plusieurs protéines homeobox, régulateurs maîtres du développement, étaient souvent hyperméthylés. En combinant ces cartes chimiques avec des jeux de données publics sur la liaison des protéines homeobox, ils ont identifié un grand groupe de gènes « cibles HOX » anormalement actifs dans les cas monosomie 7. Nombre d’entre eux chevauchaient le programme de 49 gènes de stemness. Des expériences ont confirmé qu’au moins un de ces régulateurs, PAX8, ne se liait plus à certains enhancers lorsqu’ils étaient hyperméthylés, corroborant l’idée que la chimie modifiée des enhancers contribue à enfermer les cellules dans un état tumoral ressemblant à une cellule souche.
Un point de contrôle immunitaire brisé dans la moelle
Le travail s’est ensuite concentré sur IKZF1, un gène situé sur le chromosome 7 qui participe à l’organisation tridimensionnelle de l’ADN et à la régulation d’autres gènes. Avec une seule copie du chromosome 7, les cellules monosomie 7 produisaient moins d’IKZF1 et affichaient un profil génique typique d’« insuffisance en IKZF1 ». Parmi eux figurait CD112, une protéine de surface qui communique avec les cellules immunitaires. Les chercheurs ont démontré qu’IKZF1 se lie normalement au promoteur de CD112 et le maintient sous contrôle. Lorsqu’ils ont réduit IKZF1 dans des cellules souches saines par CRISPR, les niveaux de CD112 ont augmenté, reproduisant ce qu’ils observaient chez les patients. Dans des prélèvements de moelle de personnes atteintes de monosomie 7, les blastes leucémiques et les précurseurs anormaux étaient fortement positifs pour CD112, tandis que les échantillons normaux ne présentaient qu’une coloration faible et éparse.
Comment les cellules leucémiques désarment les cellules natural killer
CD112 interagit avec trois récepteurs présents sur les cellules natural killer et les lymphocytes T : un récepteur activateur nommé DNAM1 et deux récepteurs inhibiteurs, TIGIT et PVRIG. Chez les patients monosomie 7, les cellules natural killer et T exprimaient des niveaux plus élevés des récepteurs inhibiteurs et des niveaux plus faibles du récepteur activateur, un profil cohérent avec une mise en état léthargique des cellules immunitaires. Quand des cellules natural killer saines ont été cocultivées avec des cellules leucémiques à forte expression de CD112, leurs niveaux de PVRIG ont augmenté et ceux de DNAM1 ont diminué, suggérant que le contact avec ces cellules cancéreuses participe à la reprogrammation des défenses immunitaires. Des essais fonctionnels de cytotoxicité ont montré que le blocage simultané de TIGIT et PVRIG sur les cellules natural killer des patients restaurait leur capacité à lyser leurs propres blastes monosomie 7, tandis que le blocage de CD112 seul était moins efficace.
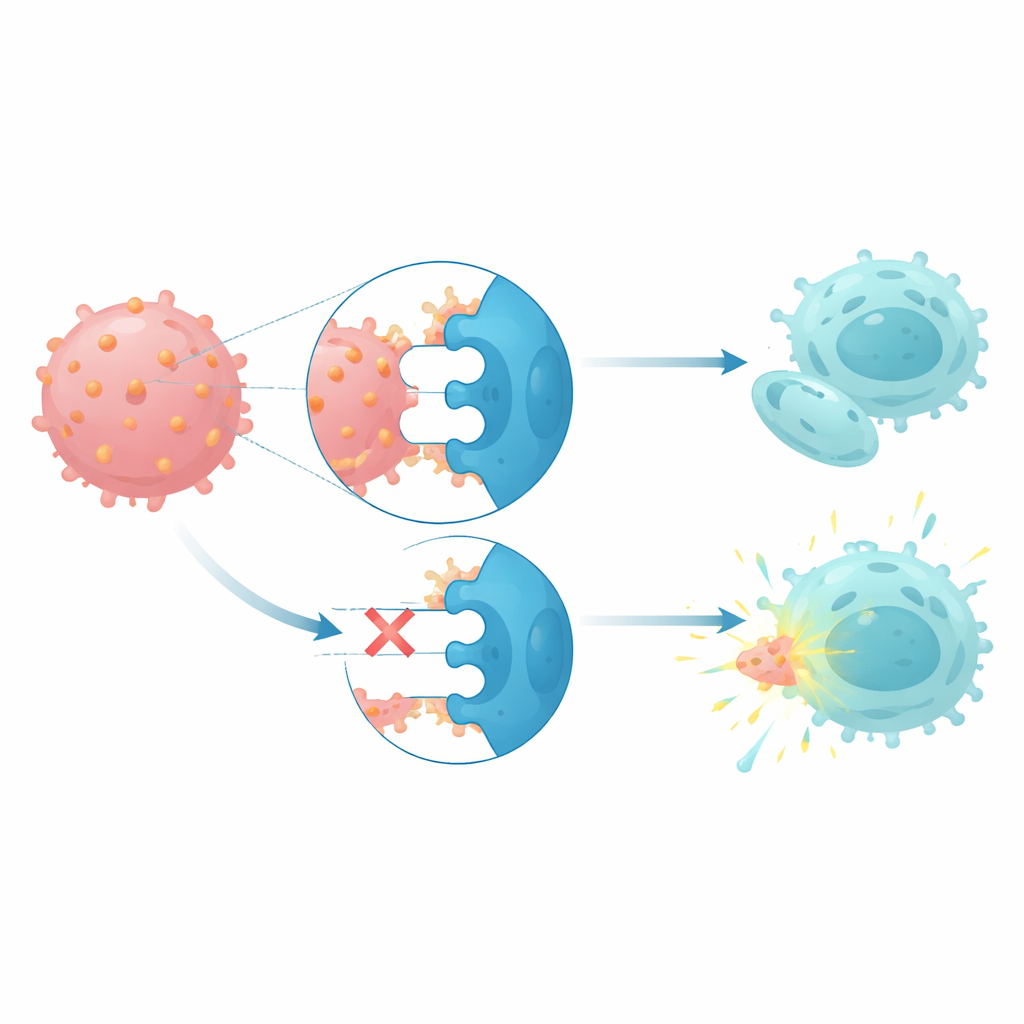
Ce que cela pourrait signifier pour les traitements futurs
Pris ensemble, ces résultats décrivent les néoplasmes myéloïdes monosomie 7 comme des cancers pilotés par un programme génique de type souche et protégés par un point de contrôle immunitaire déformé basé sur CD112. En reliant la perte du chromosome 7 à des changements d’enhancers, à l’altération de régulateurs maîtres et à une reconfiguration de l’axe CD112–TIGIT–PVRIG–DNAM1, l’étude suggère que des médicaments bloquant les récepteurs inhibiteurs TIGIT et PVRIG, éventuellement associés aux thérapies existantes ciblant la méthylation de l’ADN, pourraient aider les propres cellules natural killer des patients à reconnaître et attaquer ces cancers par ailleurs difficiles à traiter.
Citation: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Mots-clés: monosomie 7, néoplasme myéloïde, leucémie myéloïde aiguë, point de contrôle immunitaire, cellules tueuses naturelles