Clear Sky Science · ru
Специфическая программа стволовых клеток и нарушения иммунной оси CD112, лежащие в основе миелоидных новообразований, связанных с моносомией 7
Почему эта проблема крови важна
Некоторые агрессивные раки крови объединяет загадочное изменение: у пациентов в клетках костного мозга отсутствует целая копия хромосомы 7. Этот дефект, называемый моносомией 7, связан с плохим прогнозом, но у врачей по‑прежнему нет целевых методов лечения. В этом исследовании изучают, что происходит внутри этих клеток на уровне генов и иммунных сигналов, выявляя, как особая стволовая программа и испорченная «тормоз‑и‑газ» иммунной системы помогают этим опухолям расти и уклоняться от защиты организма.
Опасный сдвиг в стволовых клетках костного мозга
Миелодиспластические синдромы и острый миелоидный лейкоз — это заболевания, при которых незрелые клетки крови захватывают костный мозг. Авторы сравнили образцы костного мозга пациентов с моносомией 7, образцы других больных лейкемией и доноров со здоровым костным мозгом. Читая, какие гены включены или выключены, они обнаружили, что клетки при моносомии 7 несут отличительную «стволовую» программу: набор из 49 генов, которые удерживают клетки в состоянии самоподдерживающегося, стволоподобного состояния, вместо того чтобы позволить им созревать в нормальные клетки крови. Многие из этих генов уже связывали с худшей выживаемостью или необычным энергетическим метаболизмом при опухолях крови, что указывает на то, что этот стволовой паттерн помогает объяснить, почему новообразования при моносомии 7 так трудно лечить.
Скрытые химические метки, направляющие активность генов
Далее команда изучила метилирование ДНК — химическую метку, которая может заглушать или изменять активность генов без изменения последовательности ДНК. С помощью высокоразрешающего метода они показали, что костный мозг при моносомии 7 обладает характерным «отпечатком» метилирования, с многочисленными регионами, более интенсивно помеченными, чем обычно. Эти изменения в основном не локализовались в стартовых участках генов, а накапливались в интергенных усилителях — контрольных регионах, которые действуют как отдалённые регуляторы яркости. Многие из этих усилителей сгруппированы на определённых хромосомах, включая оставшуюся копию хромосомы 7, что намекает на то, что целая копия подвергается перенастройке, а не просто является пассивным остатком.
Когда переключатели контроля ключевых генов перенастраиваются
Поскольку усилители служат посадочными участками для транскрипционных факторов — белков, включающих и выключающих гены, — исследователи выясняли, какие факторы могут быть затронуты. Они обнаружили, что сайты связывания нескольких гомеобоксных белков, мастер‑регуляторов развития, часто гиперметилированы. Комбинируя эти химические карты с общедоступными наборами данных о связывании гомеобоксных белков, они выделили большую группу «HOX‑таргетных» генов, которые были аномально активны при моносомии 7. Многие из них перекрывались с 49‑генной стволовой программой. Эксперименты подтвердили, что по крайней мере один из этих регуляторов, PAX8, не способен связываться с некоторыми усилителями, когда те гиперметилированы, что поддерживает идею о том, что изменённая химия усилителей способствует закреплению клеток в раковом стволоподобном состоянии.
Сломанный иммунный контроль в костном мозге
Далее работа сосредоточилась на IKZF1, гене на хромосоме 7, который участвует в организации 3D‑структуры ДНК и регуляции других генов. При наличии только одной копии хромосомы 7 клетки с моносомией 7 вырабатывали меньше IKZF1 и демонстрировали профиль генов, типичный для «недостаточности IKZF1». Среди них оказался CD112 — белок на поверхности клетки, который взаимодействует с иммунными клетками. Исследователи доказали, что IKZF1 обычно связывается с промотором CD112 и сдерживает его экспрессию. Когда они уменьшили количество IKZF1 в здоровых стволовых клетках с помощью CRISPR, уровни CD112 возросли, как это наблюдалось у пациентов. В препаратах костного мозга людей с моносомией 7 бластные и аномальные предшественники сильно позитивно окрашивались на CD112, тогда как в нормальных образцах наблюдалась лишь разбросанная слабая окраска.
Как клетки лейкемии обезоруживают натуральные киллеры
CD112 взаимодействует с тремя рецепторами на натуральных киллерах и Т‑клетках: активирующим рецептором DNAM1 и двумя ингибирующими рецепторами — TIGIT и PVRIG. У пациентов с моносомией 7 натуральные киллеры и Т‑клетки демонстрировали повышенные уровни ингибирующих рецепторов и сниженные уровни активирующего — паттерн, согласующийся с тем, что иммунные клетки загоняются в вялое состояние. Когда здоровые натуральные киллеры культивировали совместно с лейкозными клетками с высоким уровнем CD112, у них повышался PVRIG и снижался DNAM1, что говорит о том, что контакт с этими раковыми клетками помогает перепрограммировать иммунную защиту. Функциональные тесты на убивание показали, что блокада одновременно TIGIT и PVRIG на натуральных киллерах пациентов восстанавливала их способность лизировать собственные бласты при моносомии 7, тогда как блокада только CD112 была менее эффективна.
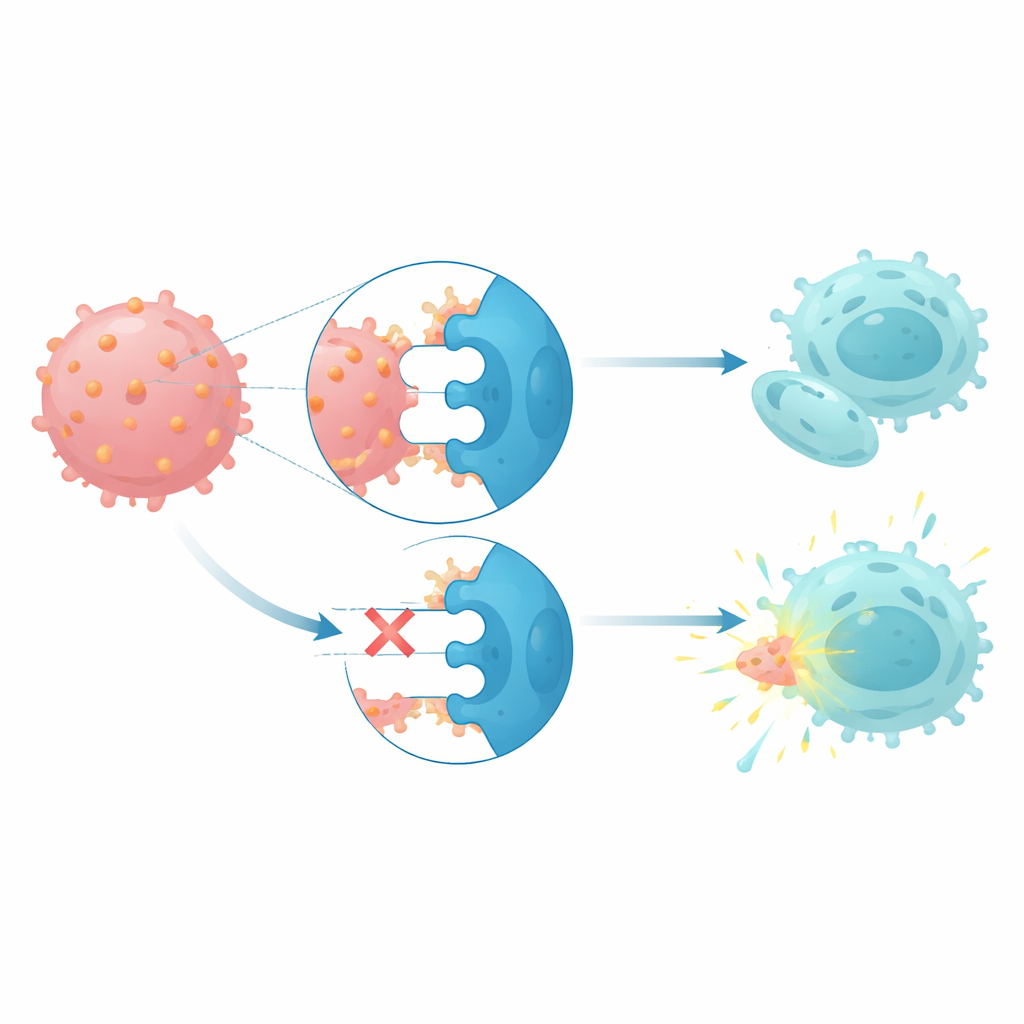
Что это может значить для будущего лечения
В совокупности эти результаты представляют миелоидные новообразования при моносомии 7 как опухоли, управляемые стволоподобной генной программой и защищённые искажённым иммунным контрольным пунктом на основе CD112. Соединив потерю хромосомы 7 с изменениями усилителей, модификацией ключевых регуляторов и перенастроенной осью CD112–TIGIT–PVRIG–DNAM1, исследование предполагает, что препараты, блокирующие ингибирующие рецепторы TIGIT и PVRIG, возможно в сочетании с существующей терапией, направленной на метилирование ДНК, могут помочь собственным натуральным киллерам пациентов распознавать и атаковать эти иначе трудно поддающиеся лечению опухоли.
Цитирование: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Ключевые слова: моносомия 7, миелоидное новообразование, острый миелоидный лейкоз, иммунный контрольный пункт, натуральные киллеры