Clear Sky Science · tr
Tek bir kök hücre programı ve CD112 bağışıklık ekseni bozuklukları monosomi 7 ilişkili miyeloid neoplazilerin temelini oluşturuyor
Bu kan problemi neden önemli
Bazı agresif kanser türlerinde gizemli bir değişiklik ortak: hastalar kemik iliği hücrelerinde kromozom 7’nin tüm bir kopyasını kaybediyor. Monosomi 7 adı verilen bu kusur kötü sonuçlarla ilişkili, ancak doktorların buna yönelik hedefe yönelik tedavileri hâlâ sınırlı. Bu çalışma, bu hücrelerin içinde genler ve bağışıklık sinyalleri düzeyinde neler olduğunu araştırıyor ve özel bir kök hücre programı ile hatalı bir bağışıklık “fren-ve-gaz” sisteminin bu kanserlerin büyümesini ve vücudun savunmasından kaçmasını nasıl kolaylaştırdığını ortaya koyuyor.
Kemik iliği kök hücrelerinde riskli bir kayma
Myelodisplastik sendromlar ve akut miyeloid lösemi, olgunlaşmamış kan hücrelerinin kemik iliğini istila ettiği hastalıklardır. Yazarlar, monosomi 7’li hastalardan alınan kemik iliği örneklerini diğer lösemi hastaları ve sağlıklı bağışıklık vericilerden alınan örneklerle karşılaştırdı. Hangi genlerin açık veya kapalı olduğunu okuyarak, monosomi 7 hücrelerinin ayırt edici bir “kök hücrelik” programı taşıdığını buldular: hücreleri olgun normal kan hücrelerine dönüşmek yerine kendini yenileyen, kök hücre benzeri bir durumda tutan 49 genlik bir dizi. Bu genlerin birçoğu daha kötü sağkalım veya kanserlerde sıra dışı enerji kullanımına önceden bağlanmıştı; bu da bu kök hücre deseninin monosomi 7 neoplazilerinin neden tedaviye dirençli olduğunu açıklamaya yardımcı olabileceğini düşündürüyor.
Gen aktivitesini yönlendiren gizli kimyasal işaretler
Araştırma ekibi daha sonra DNA metilasyonuna baktı; bu, DNA’daki harfleri değiştirmeden gen aktivitesini susturabilen veya değiştirebilen kimyasal bir etikettir. Yüksek çözünürlüklü bir yöntem kullanarak, monosomi 7 kemik iliğinin karakteristik bir metilasyon “parmak izi”ne sahip olduğunu ve birçok bölgenin normalden daha yoğun şekilde etiketlendiğini gösterdiler. Bu değişiklikler esas olarak gen başlangıç bölgelerinde değil, uzak ayar anahtarları gibi davranan intergenik enhançerlerde birikiyordu. Bu enhançerlerin birçoğu belirli kromozomlarda, kalan kromozom 7 kopyası dahil olmak üzere kümelenmişti; bu da sağlam kopyanın sadece pasif bir artakalan olmaktan ziyade yeniden kablolandığını düşündürüyor.
Anahtar genlerin kontrol anahtarları yeniden kablolandığında
Enhãncerler, genleri açıp kapatan transkripsiyon faktörleri için bağlanma bölgeleri olduğundan, araştırmacılar hangi faktörlerin etkilenmiş olabileceğini sordular. Bir dizi homeobox proteini gibi gelişimin ana düzenleyicileri için bağlanma bölgelerinin sıklıkla hipermetile olduğunu buldular. Bu kimyasal haritaları homeobox protein bağlanma veritabanlarıyla birleştirerek, monosomi 7 vakalarında anormal derecede aktif olan büyük bir “HOX hedefi” gen grubunu tanımladılar. Bu genlerin çoğu 49 genlik kök hücre programıyla örtüşüyordu. Deneyler, bu düzenleyicilerden en az birinin, PAX8’in hipermetile olmuş bazı enhançerlere bağlanamadığını doğrulayarak, değişmiş enhançer kimyasının hücreleri kanserli, kök hücre benzeri durumda kilitlemeye yardımcı olduğu fikrini destekledi.
Kemik iliğinde bozuk bir immün kontrol noktası
Çalışma daha sonra DNA’nın 3D yapısını düzenlemeye ve diğer genleri kontrol etmeye yardımcı olan kromozom 7’deki IKZF1 genine yöneldi. Kromozom 7’nin yalnızca bir kopyası olduğunda, monosomi 7 hücreleri daha az IKZF1 üretiyor ve “IKZF1 yetersizliği”ne benzer bir gen deseni sergiliyordu. Bunların arasında, hücre yüzeyinde bulunan ve bağışıklık hücreleriyle etkileşime giren CD112 proteini vardı. Araştırmacılar, IKZF1’in normalde CD112 promotörüne bağlanıp onu kontrol altında tuttuğunu kanıtladılar. Sağlıklı kök hücrelerde IKZF1’i CRISPR ile azalttıklarında CD112 seviyeleri yükseldi ve hastalarda görülen durumu yansıttı. Monosomi 7’li kişilerden alınan kemik iliği dokusunda, lösemi blastları ve anormal öncüller güçlü şekilde CD112 pozitifken, normal örneklerde sadece dağınık zayıf boyanma görüldü.
Lösemi hücreleri doğal öldürücü hücreleri nasıl etkisizleştiriyor
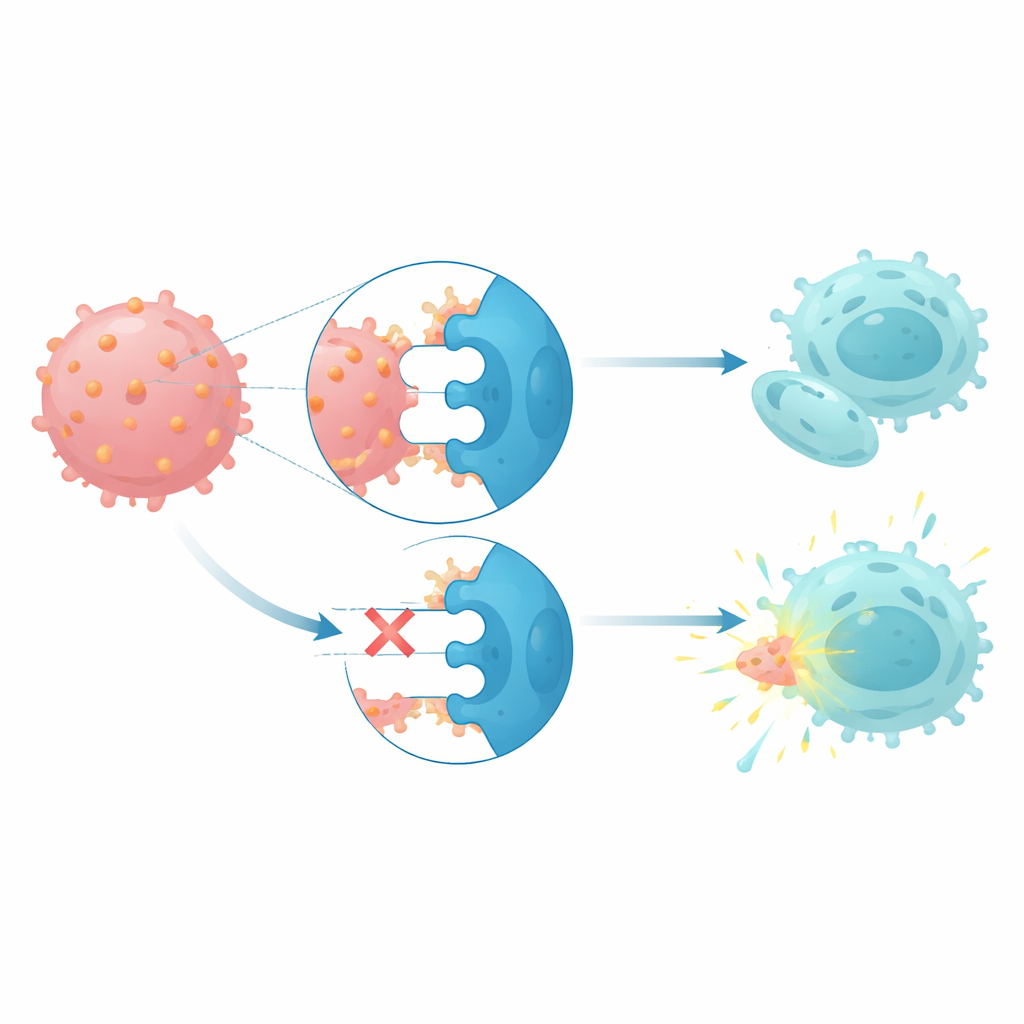
CD112, doğal öldürücü hücreler ve T hücreleri üzerindeki üç reseptörle etkileşir: DNAM1 adlı aktive edici bir reseptör ve iki inhibitör reseptör TIGIT ile PVRIG. Monosomi 7 hastalarında, doğal öldürücü hücreler ve T hücreleri inhibitör reseptörleri daha yüksek, aktive edici reseptörü ise daha düşük seviyelerde gösteriyordu; bu desen bağışıklık hücrelerinin yavaşlamaya zorlandığıyla uyumlu. Sağlıklı doğal öldürücü hücreler CD112-yüksek lösemi hücreleriyle ortak kültüre alındığında, PVRIG seviyelerinin yükseldiği ve DNAM1 seviyelerinin düştüğü gözlendi; bu, bu kanser hücreleriyle temasın bağışıklık savunmalarını yeniden programlamaya yardımcı olduğunu düşündürüyor. İşlevsel öldürme testleri, hasta doğal öldürücü hücrelerinde hem TIGIT hem de PVRIG’i engellemenin kendi monosomi 7 lösemi blastlarını lizis etme yeteneklerini geri getirdiğini gösterirken, yalnızca CD112’yi engellemenin daha az etkili olduğunu ortaya koydu.
Gelecek tedavi için ne anlama gelebilir
Bu bulgular birlikte monosomi 7 miyeloid neoplazilerini kök hücre benzeri bir gen programı tarafından yönlendirilen ve bozulmuş bir CD112 tabanlı immün kontrol noktasıyla korunmuş kanserler olarak resmediyor. Kromozom 7 kaybını enhançer değişiklikleri, ana düzenleyicilerin bozulması ve yeniden kablolanmış CD112–TIGIT–PVRIG–DNAM1 ekseniyle ilişkilendirerek, çalışma inhibitör reseptörler TIGIT ve PVRIG’i hedef alan ilaçların, muhtemelen mevcut DNA metilasyon terapileri ile birlikte, hastaların kendi doğal öldürücü hücrelerinin bu zor tedavi edilen kanserleri tanımasına ve onlara saldırmasına yardımcı olabileceğini öne sürüyor.
Atıf: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Anahtar kelimeler: monosomi 7, miyeloid neoplazm, akut miyeloid lösemi, immün kontrol noktası, doğal öldürücü hücreler