Clear Sky Science · es
Un programa específico de células madre y disfunciones del eje inmunológico CD112 que subyacen en las neoplasias mieloides asociadas a la monosomía 7
Por qué importa este problema sanguíneo
Algunos cánceres sanguíneos agresivos comparten un cambio desconcertante: los pacientes pierden una copia entera del cromosoma 7 en las células de la médula ósea. Este defecto, denominado monosomía 7, se asocia con malos desenlaces, pero los médicos aún carecen de terapias dirigidas específicas. Este estudio explora lo que ocurre dentro de estas células a nivel de genes y señales inmunitarias, y revela cómo un programa particular de células madre y un sistema inmunitario de “freno y acelerador” defectuoso ayudan a que estos cánceres crezcan y escapen de las defensas del organismo.
Un cambio arriesgado en las células madre de la médula ósea
Los síndromes mielodisplásicos y la leucemia mieloide aguda son enfermedades en las que células sanguíneas inmaduras ocupan la médula ósea. Los autores compararon muestras de médula ósea de pacientes con monosomía 7 con muestras de otros pacientes con leucemia y donantes sanos. Al leer qué genes estaban activos o silenciados, encontraron que las células con monosomía 7 portaban un programa de “stemness” distinto: un conjunto de 49 genes que mantienen a las células en un estado autorrenovable y similar al de células madre, en lugar de permitirles madurar hacia células sanguíneas normales. Muchos de estos genes ya se habían vinculado con peor supervivencia o con un uso energético inusual en cánceres sanguíneos, lo que sugiere que este patrón de células madre ayuda a explicar por qué las neoplasias con monosomía 7 son tan difíciles de tratar.
Marcas químicas ocultas que orientan la actividad génica
El equipo analizó a continuación la metilación del ADN, una etiqueta química que puede silenciar o modular la actividad génica sin cambiar las letras del ADN. Usando un método de alta resolución, mostraron que la médula ósea con monosomía 7 presentaba una “huella” característica de metilación, con muchas regiones más marcadas de lo normal. Estos cambios no se localizaban principalmente en los inicios de los genes, sino que se acumulaban en potenciadores intergénicos, regiones de control que actúan como reguladores remotos. Muchos de estos potenciadores se agruparon en cromosomas específicos, incluida la copia restante del cromosoma 7, lo que sugiere que la copia intacta está siendo reconfigurada en lugar de comportarse simplemente como un remanente pasivo.
Cuando los interruptores de control de genes clave se reconfiguran
Dado que los potenciadores son puntos de anclaje para los factores de transcripción, las proteínas que encienden y apagan genes, los investigadores buscaron qué factores podrían verse afectados. Hallaron que los sitios de unión de varios homeobox —reguladores maestros del desarrollo— estaban frecuentemente hipermetilados. Al combinar estos mapas químicos con conjuntos de datos públicos de unión de proteínas homeobox, identificaron un amplio grupo de genes “objetivo de HOX” que estaban anormalmente activos en los casos con monosomía 7. Muchos de estos coincidían con el programa de 49 genes de stemness. Experimentos confirmaron que al menos uno de estos reguladores, PAX8, dejaba de unirse a ciertos potenciadores cuando éstos estaban hipermetilados, respaldando la idea de que la química alterada de los potenciadores contribuye a bloquear a las células en un estado canceroso similar al de células madre.
Un punto de control inmunitario roto en la médula ósea
El trabajo se centró luego en IKZF1, un gen del cromosoma 7 que ayuda a organizar la estructura 3D del ADN y a regular otros genes. Con solo una copia del cromosoma 7, las células con monosomía 7 producían menos IKZF1 y mostraban un patrón génico típico de “insuficiencia de IKZF1”. Entre estos genes estaba CD112, una proteína de superficie celular que se comunica con las células inmunitarias. Los investigadores demostraron que IKZF1 normalmente se une al promotor de CD112 y lo mantiene bajo control. Cuando redujeron IKZF1 en células madre sanas mediante CRISPR, los niveles de CD112 aumentaron, reproduciendo lo observado en pacientes. En tejido de médula ósea de personas con monosomía 7, los blastos leucémicos y los precursores anómalos mostraron una marcada positividad para CD112, mientras que las muestras normales presentaron solo tinción débil y dispersa.
Cómo las células leucémicas desarman a las células asesinas naturales
CD112 interactúa con tres receptores en células NK y células T: un receptor activador llamado DNAM1 y dos receptores inhibidores, TIGIT y PVRIG. En pacientes con monosomía 7, las células NK y las células T mostraron niveles más altos de los receptores inhibidores y niveles más bajos del activador, un patrón coherente con el empuje de las células inmunitarias hacia un estado apagado. Cuando células NK sanas se co-cultivaron con células leucémicas que expresan altos niveles de CD112, sus niveles de PVRIG aumentaron y los de DNAM1 disminuyeron, lo que sugiere que el contacto con estas células cancerosas contribuye a reprogramar las defensas inmunitarias. Ensayos funcionales de citotoxicidad mostraron que bloquear simultáneamente TIGIT y PVRIG en las células NK de los pacientes restauraba su capacidad para lisar sus propios blastos con monosomía 7, mientras que bloquear solo CD112 fue menos eficaz.
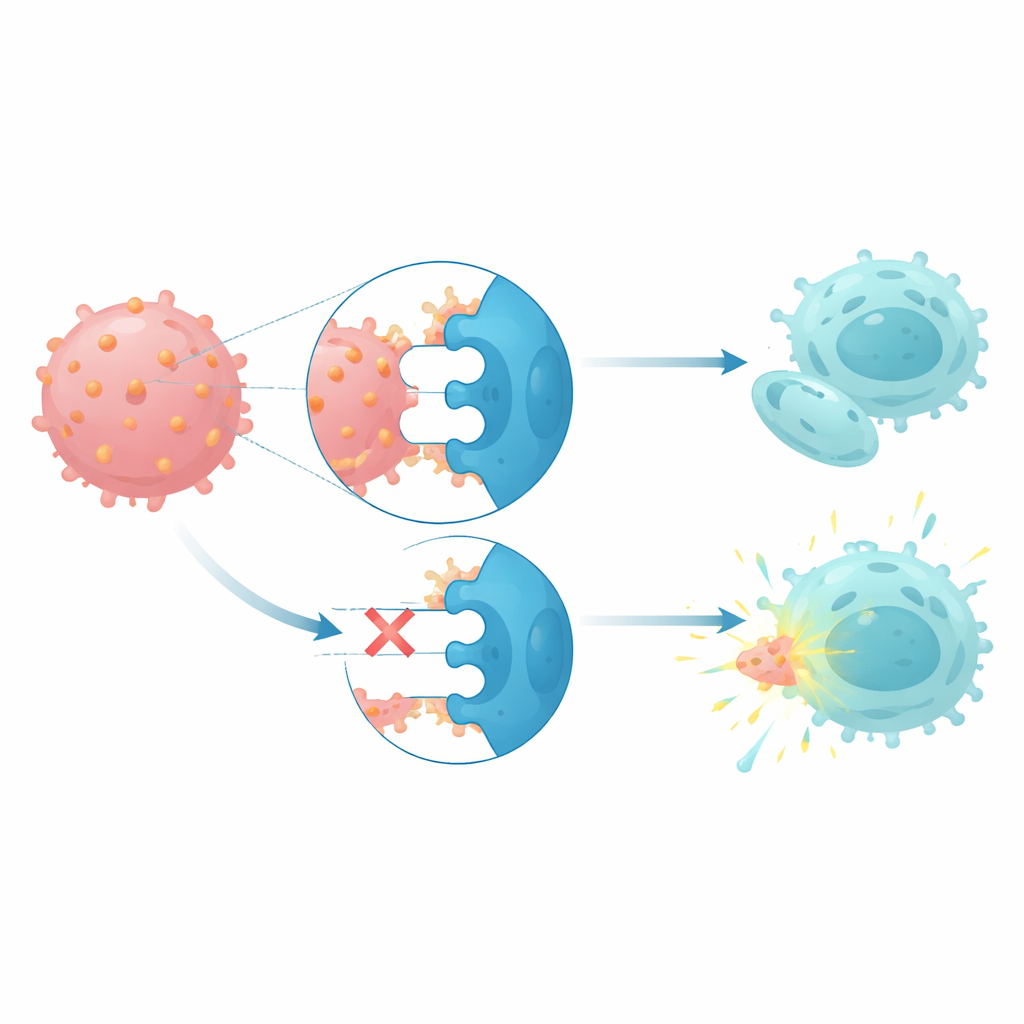
Qué podría significar esto para tratamientos futuros
En conjunto, estos hallazgos describen a las neoplasias mieloides con monosomía 7 como cánceres impulsados por un programa génico similar al de células madre y protegidos por un punto de control inmunitario distorsionado basado en CD112. Al conectar la pérdida del cromosoma 7 con cambios en potenciadores, reguladores maestros alterados y un eje CD112–TIGIT–PVRIG–DNAM1 reconfigurado, el estudio sugiere que fármacos que bloqueen los receptores inhibidores TIGIT y PVRIG, posiblemente junto con terapias existentes dirigidas a la metilación del ADN, podrían ayudar a que las propias células NK de los pacientes reconozcan y ataquen estos cánceres, difíciles de tratar por otros medios.
Cita: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Palabras clave: monosomía 7, neoplasia mieloide, leucemia mieloide aguda, punto de control inmunitario, células asesinas naturales