Clear Sky Science · sv
Ett specifikt stamcellsprogram och dysfunktion i CD112-immunaxeln bakom monosomi 7-associerade myeloida neoplasier
Varför detta blodproblem är viktigt
Vissa aggressiva blodcancerformer har en gåtfull förändring: patienterna förlorar en hel kopia av kromosom 7 i sina benmärgsceller. Denna defekt, kallad monosomi 7, är kopplad till dålig prognos, men läkare saknar fortfarande riktade behandlingar. Denna studie undersöker vad som händer i dessa celler på gen- och immunsignalsnivå och avslöjar hur ett särskilt stamcellsprogram och ett felande immunellt "broms-och-gas"-system hjälper dessa cancerformer att växa och undkomma kroppens försvar.
En riskfylld förskjutning i benmärgens stamceller
Myelodysplastiska syndrom och akut myeloisk leukemi är sjukdomar där omogna blodceller tar över benmärgen. Författarna jämförde benmärgsprover från patienter med monosomi 7 med prover från andra leukemipatienter och friska givare. Genom att läsa av vilka gener som var aktiva respektive inaktiva fann de att monosomi 7-celler bar ett distinkt "stemness"-program: en uppsättning om 49 gener som håller cellerna i ett självförnyande, stamcellslikt tillstånd istället för att tillåta dem att mogna till normala blodceller. Många av dessa gener hade redan kopplats till sämre överlevnad eller ovanlig energianvändning i blodcancer, vilket tyder på att detta stamcellsprogram kan bidra till att förklara varför monosomi 7-neoplasier är svåra att behandla.
Dolda kemiska markeringar som styr genaktivitet
Teamet såg sedan på DNA-metylering, en kemisk märkning som kan tysta eller förändra genaktivitet utan att ändra DNA-sekvensen. Med en högupplöst metod visade de att monosomi 7-benmärg hade ett karakteristiskt metylerings"fingeravtryck", med många regioner som var mer tungt märkta än normalt. Dessa förändringar låg inte huvudsakligen vid geners startställen, utan ackumulerades i intergena enhancers, kontrollregioner som fungerar som avlägsna dimmerströmbrytare. Många av dessa enhancers klustrade på specifika kromosomer, inklusive den kvarvarande kopian av kromosom 7, vilket antyder att den intakta kopian omprogrammeras snarare än att bara fungera som en passiv rest.
När kontrollbrytare för nyckelgener omkopplas
Eftersom enhancers är dockningsplatser för transkriptionsfaktorer, de proteiner som slår på och av gener, undersökte forskarna vilka faktorer som kan påverkas. De fann att bindningsställen för flera homeobox-proteiner, utvecklingens huvudregulatorer, ofta var hypermetylerade. Genom att kombinera dessa kemiska kartor med publika dataset över homeobox-bindning identifierade de en stor grupp "HOX-målgener" som var abnormt aktiva i monosomi 7-fall. Många av dessa överlappade med det 49-gener långa stamcellsprogrammet. Experiment bekräftade att åtminstone en av dessa regulatorer, PAX8, misslyckades med att binda vissa enhancers när de var hypermetylerade, vilket stöder idén att förändrad enhancer-kemi hjälper till att låsa celler i ett canceröst stamcellslikt tillstånd.
En bruten immuncheckpoint i benmärgen
Arbetet riktades sedan mot IKZF1, en gen på kromosom 7 som hjälper till att organisera DNA:s 3D-struktur och reglera andra gener. Med endast en kopia av kromosom 7 producerade monosomi 7-celler mindre IKZF1 och visade ett genmönster typiskt för "IKZF1-brist." Bland dessa fanns CD112, ett protein på cellytan som kommunicerar med immunceller. Forskarna visade att IKZF1 normalt binder CD112-promotorn och håller den i schack. När de minskade IKZF1 i friska stamceller med CRISPR steg CD112-nivåerna, vilket speglade vad de såg hos patienter. I benmärgsvävnad från personer med monosomi 7 var leukemiblaster och onormala prekursorer starkt positiva för CD112, medan normala prover visade endast spridda svaga fläckar.
Hur leukemiceller avväpnar naturliga mördarceller
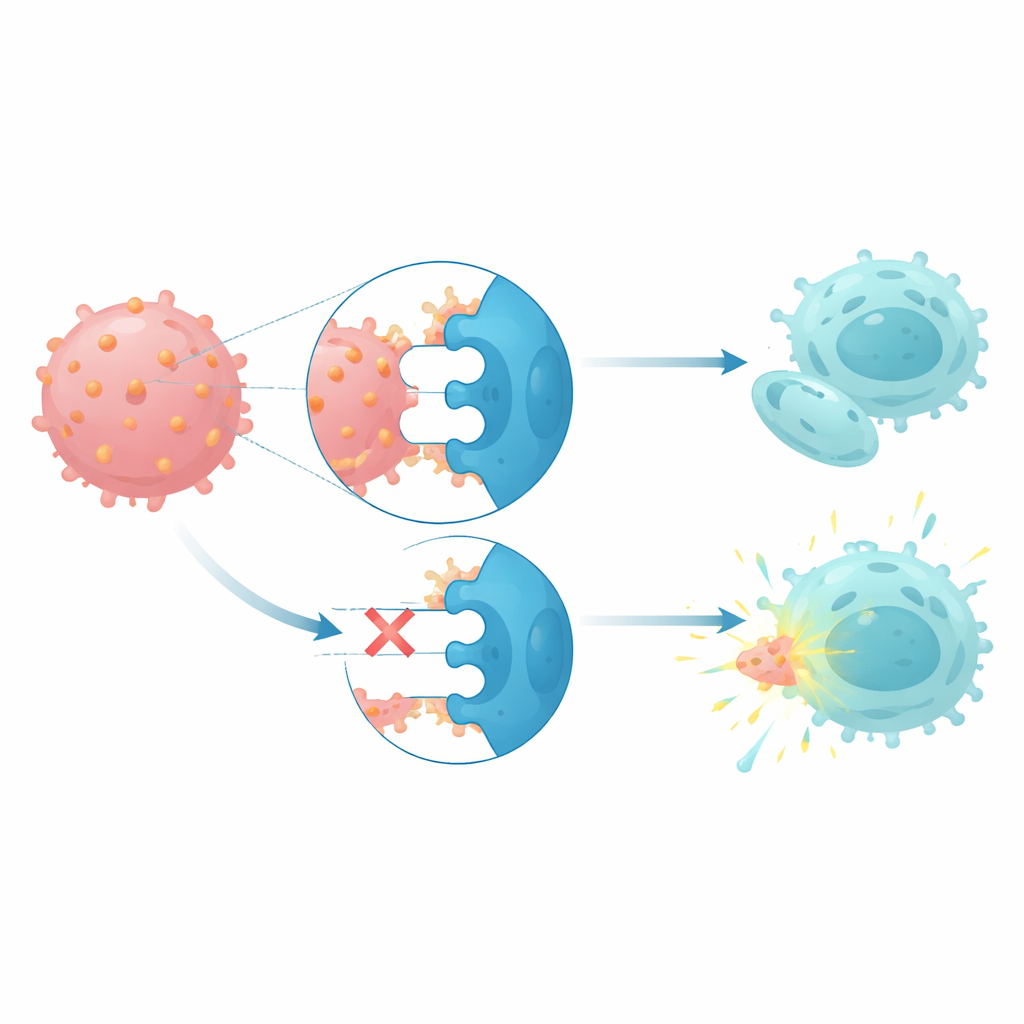
CD112 interagerar med tre receptorer på naturliga mördarceller och T-celler: en aktiverande receptor kallad DNAM1 och två hämmande receptorer, TIGIT och PVRIG. Hos patienter med monosomi 7 uppvisade naturliga mördarceller och T‑celler högre nivåer av de hämmande receptorerna och lägre nivåer av den aktiverande — ett mönster som stämmer med att immunceller drivs in i ett slött tillstånd. När friska naturliga mördarceller samodlades med CD112-höga leukemiceller ökade deras PVRIG-nivåer och DNAM1-nivåer sjönk, vilket tyder på att kontakt med dessa cancerceller hjälper till att omprogrammera immunsvaret. Funktionella dödandestester visade att blockering av både TIGIT och PVRIG på patienternas naturliga mördarceller återställde deras förmåga att lysera sina egna monosomi 7-leukemiblaster, medan blockering av CD112 ensam var mindre effektivt.
Vad detta kan innebära för framtida behandling
Tillsammans målar dessa fynd upp monosomi 7-myeloida neoplasier som cancerformer drivna av ett stamcellslikt genprogram och skyddade av en förvriden CD112-baserad immuncheckpoint. Genom att koppla förlust av kromosom 7 till förändringar i enhancers, förändrade huvudregulatorer och en omkopplad CD112–TIGIT–PVRIG–DNAM1-axel, föreslår studien att läkemedel som blockerar de hämmande receptorerna TIGIT och PVRIG, eventuellt i kombination med befintliga DNA-metyleringsterapier, kan hjälpa patienters egna naturliga mördarceller att känna igen och angripa dessa annars svårbehandlade cancerformer.
Citering: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Nyckelord: monosomi 7, myeloid neoplasm, akut myeloisk leukemi, immuncheckpoint, naturliga mördarceller