Clear Sky Science · pt
Um programa específico de células-tronco e disfunções do eixo imune CD112 que fundamentam neoplasias mieloides associadas à monossomia 7
Por que esse problema sanguíneo importa
Alguns cânceres sanguíneos agressivos compartilham uma mudança intrigante: pacientes perdem uma cópia inteira do cromossomo 7 em suas células da medula óssea. Esse defeito, chamado monossomia 7, está associado a prognóstico ruim, mas ainda faltam tratamentos direcionados. Este estudo investiga o que ocorre dentro dessas células no nível dos genes e dos sinais imunes, revelando como um programa específico de células-tronco e um sistema imune defeituoso de “freio-e-aceleração” ajudam esses cânceres a crescer e escapar das defesas do organismo.
Uma mudança arriscada nas células-tronco da medula óssea
Síndromes mielodisplásicas e leucemia mieloide aguda são doenças em que células sanguíneas imaturas dominam a medula óssea. Os autores compararam amostras de medula óssea de pacientes com monossomia 7 a amostras de outros pacientes com leucemia e doadores saudáveis. Ao ler quais genes estavam ativados ou silenciados, descobriram que as células com monossomia 7 exibiam um programa de “stemness” distinto: um conjunto de 49 genes que mantém as células em um estado autorrenovador e semelhante a células-tronco, em vez de permitir que amadureçam em células sanguíneas normais. Muitos desses genes já haviam sido associados a pior sobrevida ou a uso energético atípico em cânceres sanguíneos, sugerindo que esse padrão de células-tronco ajuda a explicar por que as neoplasias com monossomia 7 são tão difíceis de tratar.
Marcas químicas ocultas que direcionam a atividade gênica
A equipe investigou em seguida a metilação do DNA, uma marca química que pode silenciar ou alterar a atividade gênica sem mudar as letras do DNA. Usando um método de alta resolução, demonstraram que a medula óssea com monossomia 7 tinha uma “impressão digital” característica de metilação, com muitas regiões mais fortemente marcadas que o normal. Essas alterações não se concentraram principalmente em sítios iniciadores de genes, mas acumularam-se em enhancers intergênicos, regiões de controle que funcionam como dimmers distantes. Muitos desses enhancers se aglomeraram em cromossomos específicos, incluindo a cópia restante do cromossomo 7, sugerindo que a cópia intacta está sendo reconfigurada em vez de agir apenas como um resíduo passivo.
Quando os interruptores de controle de genes-chave são reconfigurados
Como os enhancers são locais de ancoragem para fatores de transcrição, as proteínas que ligam e desligam genes, os pesquisadores perguntaram quais fatores poderiam ser afetados. Eles descobriram que sítios de ligação para vários proteínas homeobox, reguladores mestres do desenvolvimento, estavam frequentemente hipermetilados. Ao combinar esses mapas químicos com conjuntos de dados públicos de ligação de proteínas homeobox, identificaram um grande grupo de genes “alvo HOX” que estavam anormalmente ativos em casos com monossomia 7. Muitos deles se sobrepunham ao programa de 49 genes de stemness. Experimentos confirmaram que pelo menos um desses reguladores, PAX8, deixou de se ligar a certos enhancers quando estes estavam hipermetilados, apoiando a ideia de que a química alterada dos enhancers ajuda a aprisionar as células em um estado cancerígeno parecido com células-tronco.
Um ponto de controle imune comprometido na medula óssea
O trabalho então se voltou para IKZF1, um gene no cromossomo 7 que ajuda a organizar a estrutura 3D do DNA e regular outros genes. Com apenas uma cópia do cromossomo 7, células com monossomia 7 produziram menos IKZF1 e exibiram um padrão de genes típico de “insuficiência de IKZF1”. Entre esses estava CD112, uma proteína na superfície celular que se comunica com células imunes. Os pesquisadores demonstraram que o IKZF1 normalmente se liga ao promotor de CD112 e o mantém sob controle. Quando reduziram IKZF1 em células-tronco saudáveis usando CRISPR, os níveis de CD112 aumentaram, espelhando o observado em pacientes. Em tecido de medula óssea de pessoas com monossomia 7, blastos leucêmicos e precursores anormais foram fortemente positivos para CD112, enquanto amostras normais mostraram apenas marcação fraca e dispersa.
Como células leucêmicas desarmam células natural killer
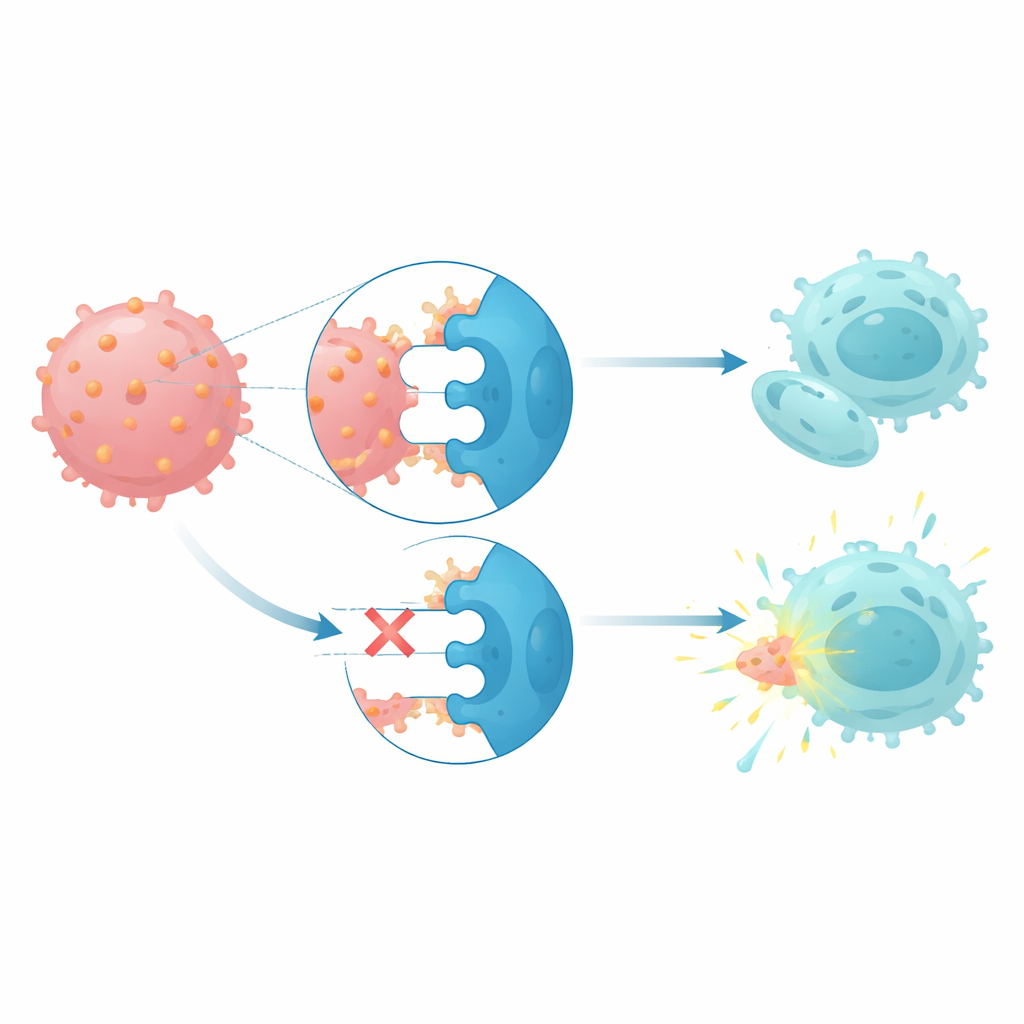
CD112 interage com três receptores em células natural killer e células T: um receptor ativador chamado DNAM1 e dois receptores inibitórios, TIGIT e PVRIG. Em pacientes com monossomia 7, células NK e células T exibiam níveis mais altos dos receptores inibitórios e níveis menores do ativador, um padrão compatível com células imunes sendo empurradas a um estado letárgico. Quando células NK saudáveis foram cultivadas em contato com células leucêmicas ricas em CD112, seus níveis de PVRIG aumentaram e os de DNAM1 diminuíram, sugerindo que o contato com essas células cancerosas contribui para reprogramar as defesas imunes. Ensaios funcionais de citotoxicidade mostraram que bloquear simultaneamente TIGIT e PVRIG nas células NK de pacientes restaurou sua capacidade de lisar seus próprios blastos leucêmicos com monossomia 7, enquanto bloquear apenas o CD112 foi menos eficaz.
O que isso pode significar para tratamentos futuros
Em conjunto, esses achados descrevem as neoplasias mieloides com monossomia 7 como cânceres impulsionados por um programa gênico semelhante a células-tronco e protegidos por um ponto de controle imune distorcido baseado em CD112. Ao conectar a perda do cromossomo 7 a mudanças em enhancers, reguladores mestres alterados e a reconfiguração do eixo CD112–TIGIT–PVRIG–DNAM1, o estudo sugere que fármacos que bloqueiem os receptores inibitórios TIGIT e PVRIG, possivelmente em combinação com terapias existentes que visam a metilação do DNA, poderiam ajudar as próprias células NK dos pacientes a reconhecer e atacar esses cânceres de difícil tratamento.
Citação: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Palavras-chave: monossomia 7, neoplasia mieloide, leucemia mieloide aguda, ponto de controle imune, células natural killer