Clear Sky Science · pl
Specyficzny program komórek macierzystych i zaburzenia osi immunologicznej CD112 leżące u podstaw mieloidalnych nowotworów związanych z monosomią 7
Dlaczego ten problem krwi jest istotny
Niektóre agresywne nowotwory krwi mają wspólną, zagadkową zmianę: pacjenci tracą całą kopię chromosomu 7 w komórkach szpiku. Ten defekt, zwany monosomią 7, wiąże się z gorszym rokowaniem, a mimo to lekarze wciąż nie dysponują ukierunkowanymi terapiami. Badanie analizuje, co dzieje się wewnątrz tych komórek na poziomie genów i sygnałów immunologicznych, ujawniając, jak specyficzny program komórek macierzystych i wadliwy system „hamulca-i-gazu” immunologii pomagają tym nowotworom rosnąć i unikać obrony organizmu.
Ryzykowna zmiana w komórkach macierzystych szpiku
Zespoły mielodysplastyczne i ostra białaczka szpikowa to choroby, w których niedojrzałe komórki krwi opanowują szpik. Autorzy porównali próbki szpiku od pacjentów z monosomią 7 z próbkami innych pacjentów z białaczką oraz dawców zdrowych. Analiza aktywności genów wykazała, że komórki z monosomią 7 nosiły odrębny program „stemness”: zestaw 49 genów utrzymujących komórki w stanie samoodnawiającym się, przypominającym komórki macierzyste, zamiast pozwalać im dojrzewać do normalnych krwinek. Wiele z tych genów było wcześniej powiązanych z gorszym przeżyciem lub nietypowym metabolizmem w nowotworach krwi, co sugeruje, że ten wzorzec komórkowy przyczynia się do trudności w leczeniu nowotworów związanych z monosomią 7.
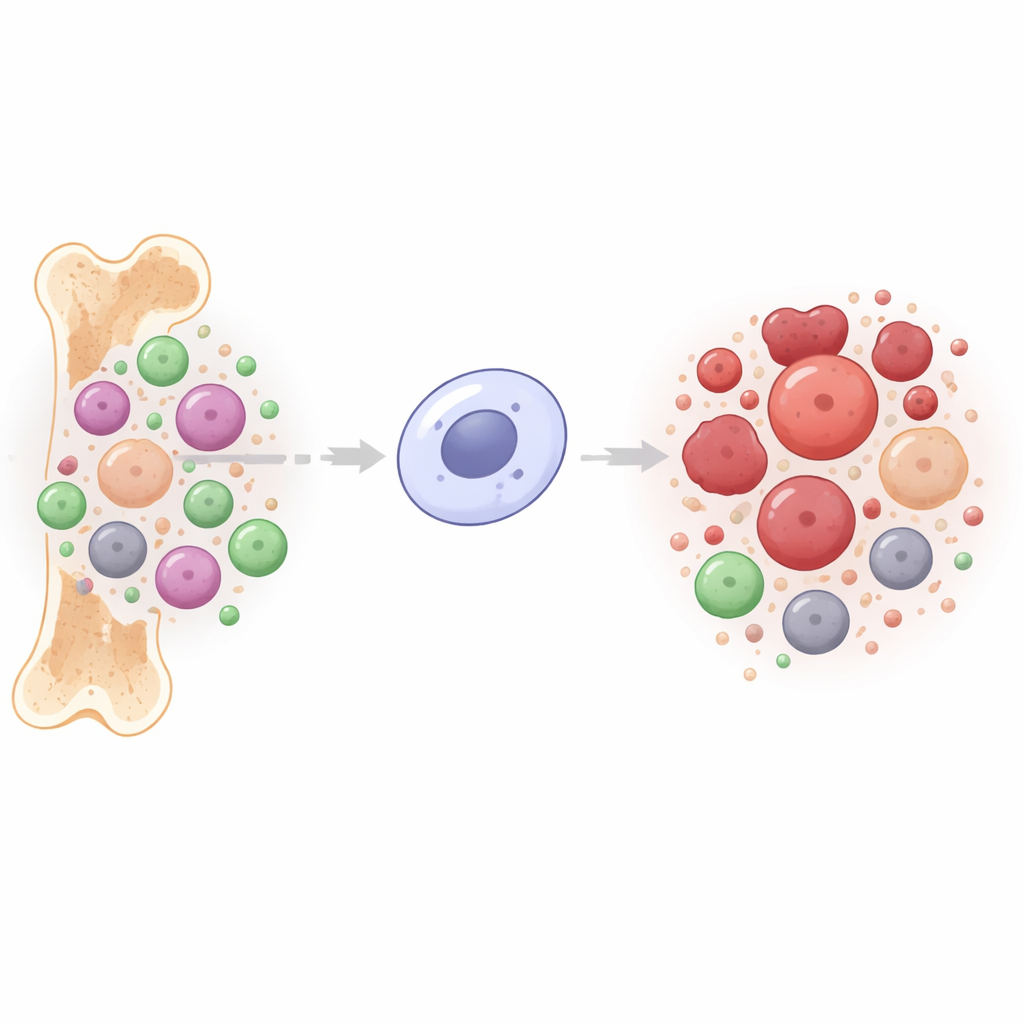
Ukryte chemiczne znaki kierujące aktywnością genów
Zespół następnie zbadał metylację DNA, chemiczny znacznik, który może wyciszać lub zmieniać aktywność genów bez zmiany sekwencji DNA. Przy użyciu wysokorozdzielczej metody pokazali, że szpik z monosomią 7 ma charakterystyczny „odcisk palca” metylacji, z wieloma regionami bardziej intensywnie znakowanymi niż normalnie. Zmiany te nie koncentrowały się głównie przy miejscach startu genów, lecz gromadziły się w międzygenowych enhancerach — obszarach kontrolnych działających jak odległe ściemniacze. Wiele z tych enhancerów skupiało się na konkretnych chromosomach, w tym na pozostającej kopii chromosomu 7, co sugeruje, że zachowana kopia jest przełączana na inny tryb działania, zamiast być jedynie biernym pozostałością.
Gdy przełączniki kontrolujące kluczowe geny zostają przeprogramowane
Ponieważ enhancery są miejscami wiązania czynników transkrypcyjnych — białek włączających i wyłączających geny — badacze sprawdzili, które z tych czynników mogą być dotknięte. Stwierdzili, że miejsca wiązania kilku białek homeobox, głównych regulatorów rozwoju, były często nadmiernie zmetylowane. Łącząc te mapy chemiczne z publicznymi zestawami danych o wiązaniu białek homeobox, zidentyfikowali dużą grupę genów „docelowych HOX”, które były patologicznie aktywne w przypadkach monosomii 7. Wiele z nich pokrywało się z 49-genowym programem stemness. Eksperymenty potwierdziły, że przynajmniej jeden z tych regulatorów, PAX8, nie wiązał się z niektórymi enhancerami, gdy te były nadmiernie zmetylowane, co wspiera tezę, że zmieniona chemia enhancerów pomaga zablokować komórki w nowotworowym, macierzystym stanie.
Złamany punkt kontrolny immunologiczny w szpiku
Dalsze prace skupiły się na IKZF1, genie zlokalizowanym na chromosomie 7, który pomaga organizować trójwymiarową strukturę DNA i regulować inne geny. Przy jednej kopii chromosomu 7 komórki z monosomią 7 produkowały mniej IKZF1 i wykazywały wzorzec genowy typowy dla „niedoboru IKZF1”. Wśród genów objętych tym wzorcem znalazł się CD112, białko powierzchniowe komunikujące się z komórkami układu odpornościowego. Badacze wykazali, że IKZF1 normalnie wiąże promotor CD112 i tłumi jego ekspresję. Gdy zredukowali IKZF1 w zdrowych komórkach macierzystych za pomocą CRISPR, poziomy CD112 wzrosły, odzwierciedlając obserwacje u pacjentów. W tkance szpiku od osób z monosomią 7 blasty białaczkowe i nieprawidłowe prekursorowe komórki silnie eksponowały CD112, podczas gdy próbki kontrolne pokazywały jedynie rozproszone, słabe barwienie.
Jak komórki białaczkowe unieszkodliwiają komórki NK
CD112 oddziałuje z trzema receptorami na komórkach NK i limfocytach T: receptorem aktywującym zwanym DNAM1 oraz dwoma receptorami hamującymi, TIGIT i PVRIG. U pacjentów z monosomią 7 komórki NK i limfocyty T wykazywały wyższe poziomy receptorów hamujących i niższe poziomy receptora aktywującego, co odpowiada wzorcowi osłabienia aktywności immunologicznej. Gdy zdrowe komórki NK współhodowano z komórkami białaczkowymi o wysokiej ekspresji CD112, poziomy PVRIG wzrosły, a DNAM1 spadł, sugerując, że kontakt z tymi komórkami nowotworowymi pomaga przeprogramować obronę immunologiczną. Funkcjonalne testy cytotoksyczności wykazały, że jednoczesne blokowanie TIGIT i PVRIG na komórkach NK pochodzących od pacjentów przywracało ich zdolność do lizy własnych blastów monosomii 7, podczas gdy sama blokada CD112 była mniej skuteczna.
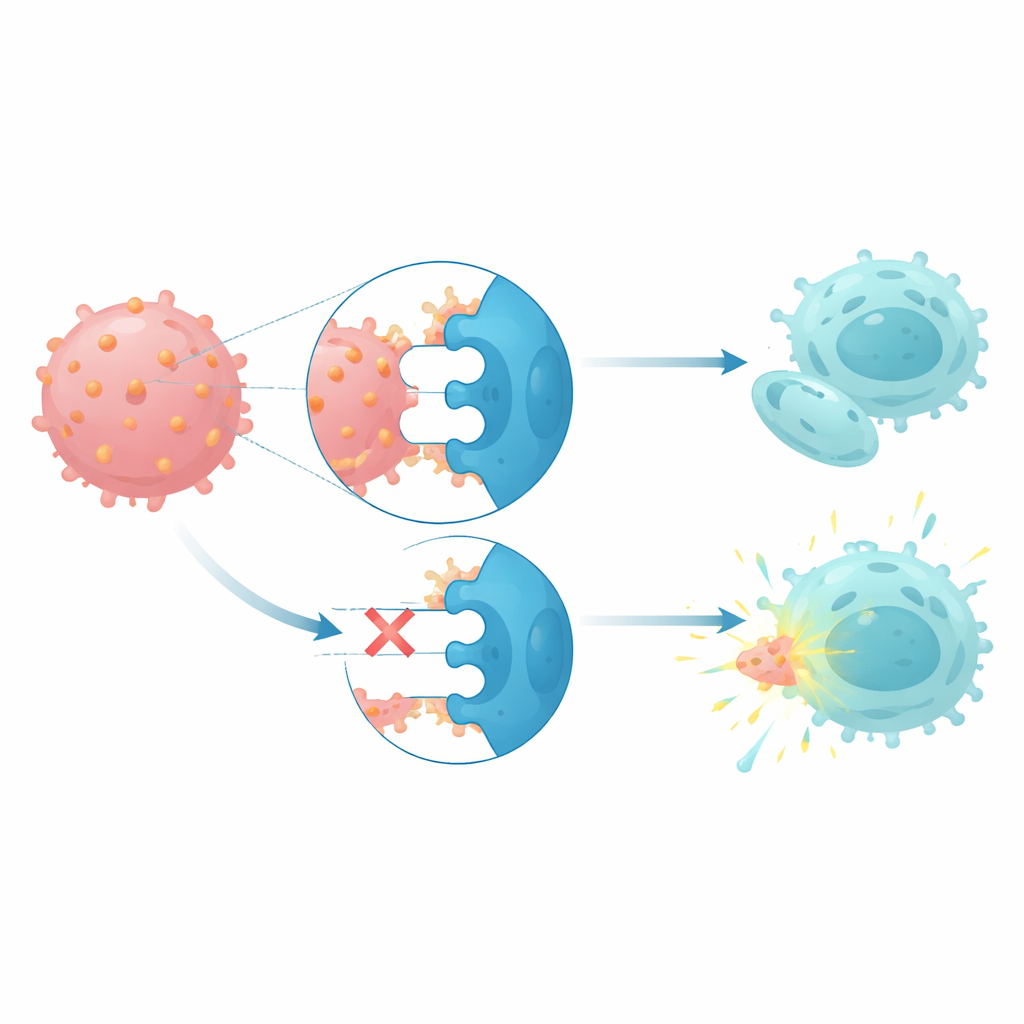
Co to może oznaczać dla przyszłego leczenia
Wszystkie te ustalenia przedstawiają mieloidalne nowotwory związane z monosomią 7 jako choroby napędzane programem genów o charakterze macierzystym i osłonięte przez zniekształcony punkt kontrolny immunologiczny oparty na CD112. Łącząc utratę chromosomu 7 ze zmianami w enhancerach, zmienionymi głównymi regulatorami i przebudowaną osią CD112–TIGIT–PVRIG–DNAM1, badanie sugeruje, że leki blokujące receptory hamujące TIGIT i PVRIG, być może w połączeniu z istniejącymi terapiami modyfikującymi metylację DNA, mogłyby pomóc komórkom NK pacjentów rozpoznać i zaatakować te trudne do leczenia nowotwory.
Cytowanie: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Słowa kluczowe: monosomia 7, nowotwór mieloidalny, ostra białaczka szpikowa, punkt kontrolny immunologiczny, komórki NK