Clear Sky Science · nl
Een specifiek stamcelprogramma en CD112-immunologische as-dysfuncties die monosomie 7-geassocieerde myeloïde neoplasmata onderbouwen
Waarom dit bloedprobleem ertoe doet
Sommige agressieve bloedkankers delen een raadselachtige verandering: patiënten verliezen een volledige kopie van chromosoom 7 in hun beenmergcellen. Dit defect, monosomie 7 genoemd, hangt samen met een slechte prognose, maar artsen hebben nog geen gerichte behandelingen daarvoor. Deze studie onderzoekt wat er in deze cellen gebeurt op het niveau van genen en immuunsignalen en onthult hoe een specifiek stamcelprogramma en een defect immuun ‘rem-en-gas’-systeem deze kankers helpen groeien en aan de afweer van het lichaam ontsnappen.
Een risicovolle verschuiving in beenmergstamcellen
Myelodysplastische syndromen en acute myeloïde leukemie zijn aandoeningen waarbij onrijpe bloedcellen het beenmerg overnemen. De auteurs vergeleken beenmergmonsters van patiënten met monosomie 7 met monsters van andere leukemiepatiënten en van gezonde donoren. Door uit te lezen welke genen aan- of uitstaan, ontdekten ze dat monosomie 7-cellen een onderscheidend ‘stemness’-programma droegen: een set van 49 genen die cellen in een zelfvernieuwende, stamcelachtige staat houden in plaats van dat ze uitrijpen tot normale bloedcellen. Veel van deze genen waren al gekoppeld aan slechtere overleving of afwijkend energiegebruik in bloedkankers, wat suggereert dat dit stamcelpatroon kan helpen verklaren waarom monosomie 7-neoplasmata zo moeilijk te behandelen zijn.
Verborgen chemische merken die genactiviteit sturen
Het team keek vervolgens naar DNA-methylering, een chemische markering die genactiviteit kan stilleggen of wijzigen zonder de DNA-letters zelf te veranderen. Met een hoogresolutiemethode toonden ze aan dat beenmerg van monosomie 7 een karakteristieke methylerings-‘vingerafdruk’ had, met veel regio’s zwaarder gemarkeerd dan normaal. Deze veranderingen zaten niet vooral bij genstarters, maar stapelden zich op in intergene enhancers, controlegebieden die werken als afstandsbedieningen. Veel van deze enhancers clusterden op specifieke chromosomen, waaronder de overgebleven kopie van chromosoom 7, wat erop wijst dat de intacte kopie opnieuw bekabeld wordt in plaats van slechts een passief overblijfsel te zijn.
Wanneer schakelaars voor sleutelgenen worden herbedraad
Aangezien enhancers bindingsplaatsen zijn voor transcriptiefactoren, de eiwitten die genen aan- of uitzetten, vroegen de onderzoekers welke factoren geraakt konden zijn. Ze vonden dat bindingsplaatsen voor meerdere homeobox-eiwitten, meesterregelaars van ontwikkeling, vaak hypergemethyleerd waren. Door deze chemische kaarten te combineren met publieke datasets van homeobox-bindings vonden ze een grote groep “HOX-doel”genen die abnormaal actief waren in monosomie 7-gevallen. Velen hiervan overlappen met het 49-genen stamcelprogramma. Experimenten bevestigden dat ten minste één van deze regulatoren, PAX8, bepaalde enhancers niet kon binden wanneer die hypergemethyleerd waren, wat het idee ondersteunt dat veranderde enhancerchemie helpt cellen vast te zetten in een kankerstamcelachtige staat.
Een defect immuuncheckpoint in het beenmerg
Het werk richtte zich vervolgens op IKZF1, een gen op chromosoom 7 dat helpt de 3D-structuur van DNA te organiseren en andere genen te reguleren. Met slechts één kopie van chromosoom 7 maakten monosomie 7-cellen minder IKZF1 aan en vertoonden ze een genpatroon typisch voor “IKZF1-insufficiëntie.” Onder deze genen bevond zich CD112, een eiwit op het celoppervlak dat communiceert met immuuncellen. De onderzoekers toonden aan dat IKZF1 normaal gesproken aan de CD112-promotor bindt en het onder controle houdt. Toen ze IKZF1 in gezonde stamcellen verminderden met CRISPR, steeg het CD112-niveau, wat de bevindingen bij patiënten weerspiegelde. In beenmergweefsel van mensen met monosomie 7 waren leukemieblasten en aberrante voorlopercellen sterk positief voor CD112, terwijl normale monsters slechts verspreide zwakke kleuring lieten zien.
Hoe leukemiecellen natural killer-cellen uitschakelen
CD112 interageert met drie receptoren op natural killer-cellen en T-cellen: een activerende receptor genaamd DNAM1 en twee remmende receptoren, TIGIT en PVRIG. Bij patiënten met monosomie 7 toonden natural killer-cellen en T-cellen hogere niveaus van de remmende receptoren en lagere niveaus van de activerende receptor, een patroon dat past bij immuuncellen die in een slome toestand worden geduwd. Wanneer gezonde natural killer-cellen werden geco-cultiveerd met CD112-rijke leukemiecellen, stegen hun PVRIG-niveaus en daalden hun DNAM1-niveaus, wat suggereert dat contact met deze kankercellen de immuunverdediging herprogrammeert. Functionele kilsassays toonden dat het blokkeren van zowel TIGIT als PVRIG op patiënt-derived natural killer-cellen hun vermogen herstelde om hun eigen monosomie 7-leukemieblasten te lyseren, terwijl alleen CD112 blokkeren minder effectief was.
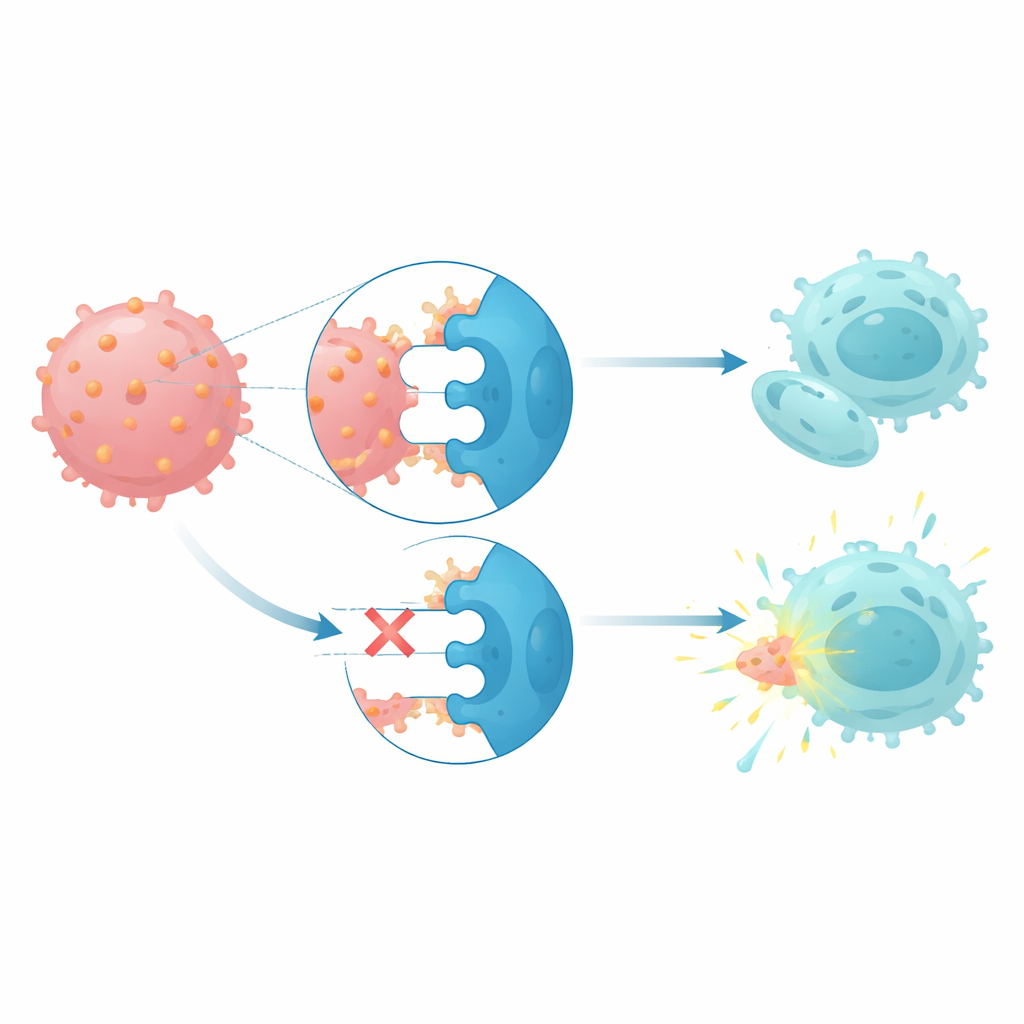
Wat dit voor toekomstige behandeling kan betekenen
Samen schetsen deze bevindingen monosomie 7-myeloïde neoplasmata als kankers aangedreven door een stamcelachtig genprogramma en afgeschermd door een verstoord CD112-gebaseerd immuuncheckpoint. Door verlies van chromosoom 7 te verbinden met enhancer‑veranderingen, gewijzigde meesterregelaars en een herbedrade CD112–TIGIT–PVRIG–DNAM1-as, suggereert de studie dat geneesmiddelen die de remmende receptoren TIGIT en PVRIG blokkeren, mogelijk in combinatie met bestaande DNA-methyleringstherapieën, de eigen natural killer-cellen van patiënten kunnen helpen deze anders moeilijk te behandelen kankers te herkennen en aan te vallen.
Bronvermelding: Lema Fernandez, A.G., Nardelli, C., Quintini, M. et al. A specific stem cell program and CD112 immunological axis dysfunctions underpinning monosomy 7-associated myeloid neoplasms. Sig Transduct Target Ther 11, 173 (2026). https://doi.org/10.1038/s41392-026-02681-w
Trefwoorden: monosomie 7, myeloïde neoplasma, acute myeloïde leukemie, immuuncheckpoint, natural killer-cellen