Clear Sky Science · zh
用针对膜近端AXL的抗体重编程肿瘤微环境以克服免疫检查点阻断耐药性
为何有些肿瘤能隐藏于免疫系统之外
癌症免疫疗法已改变了许多患者的治疗前景,但对仍有相当大一部分几乎不被免疫系统识别的肿瘤,它仍然无能为力。这类所谓的“冷”肿瘤几乎缺乏攻击性的免疫细胞,并且常对现有强效的检查点药物耐药。本研究探讨了一种新型抗体,能够激活这些肿瘤内部的先天防线,帮助将冷而寂静的癌症转变为被大量致瘤免疫细胞包围的状态。
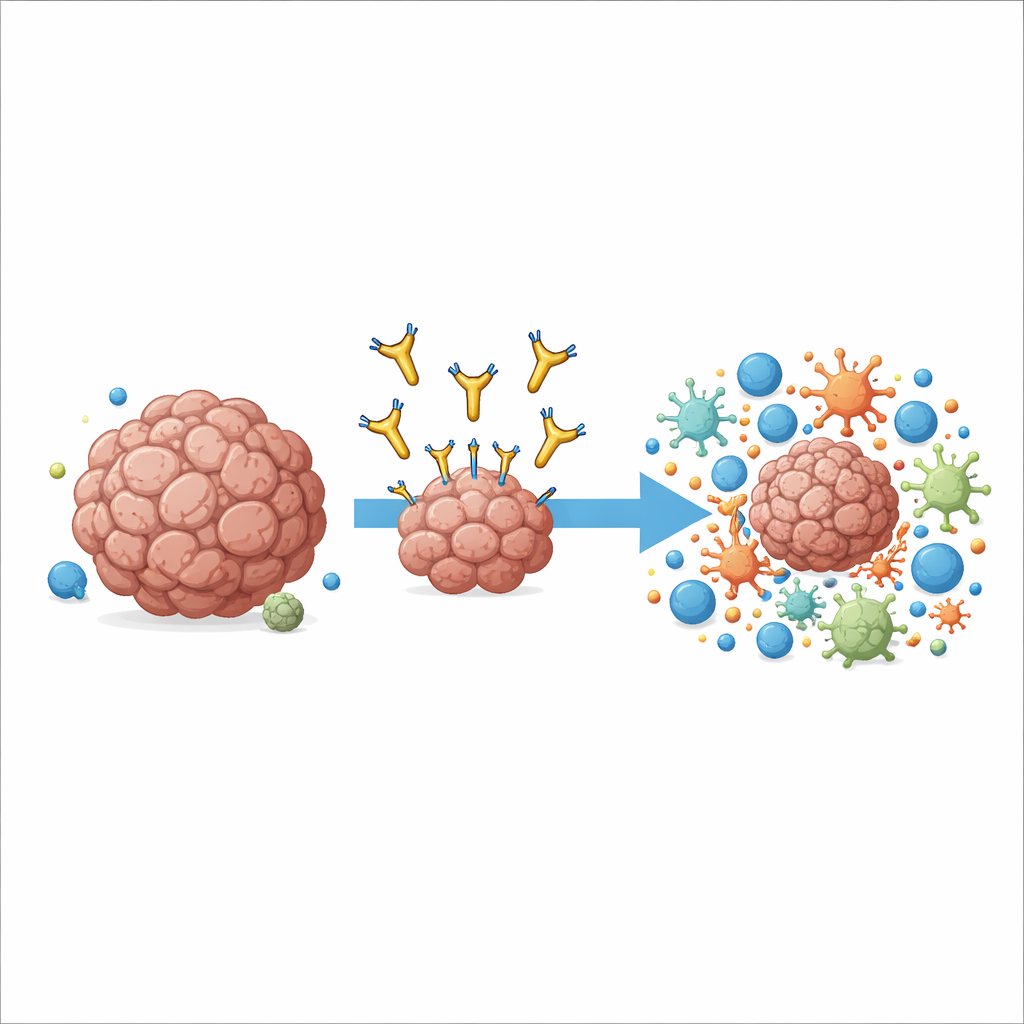
以新方式瞄准一个熟悉的癌症靶点
这项工作围绕一个名为AXL的分子展开,AXL位于许多癌细胞和肿瘤内某些免疫细胞的表面。AXL水平升高与疾病侵袭性、转移以及对常规免疫疗法的耐受性相关。早期药物尝试通过结合AXL的最外端来阻断其促生长信号,但在临床试验中仅显示出有限益处且有时伴随副作用。作者采取了不同策略:他们构建了一种名为6C5的抗体,该抗体结合AXL时位于靠近细胞膜的位置,而非远端顶端。这个看似微妙的结合位点变化对免疫系统如何利用该抗体作为抓手起到了关键作用。
招募体内的“清道夫”
6C5并非通过直接毒杀癌细胞起效,而是通过召集并重新定向擅长吞噬和处理碎片的免疫细胞,尤其是巨噬细胞和某些树突状细胞。在携带人源AXL的黑色素瘤和结肠癌小鼠模型中,当肿瘤细胞表现AXL时,6C5强力抑制甚至缩小了肿瘤,包括肺转移灶;而在缺乏T细胞和B细胞的小鼠中,该抗体几乎无效,表明持久的肿瘤控制依赖于完整的适应性免疫反应。对处理后肿瘤的单细胞详尽分析显示,6C5显著增加了浸润肿瘤的巨噬细胞、树突状细胞和杀伤性T细胞的数量和活性,将原本稀疏的免疫沙漠转变为拥挤的战场。
抗体引导的清除如何引发更广泛的免疫攻击
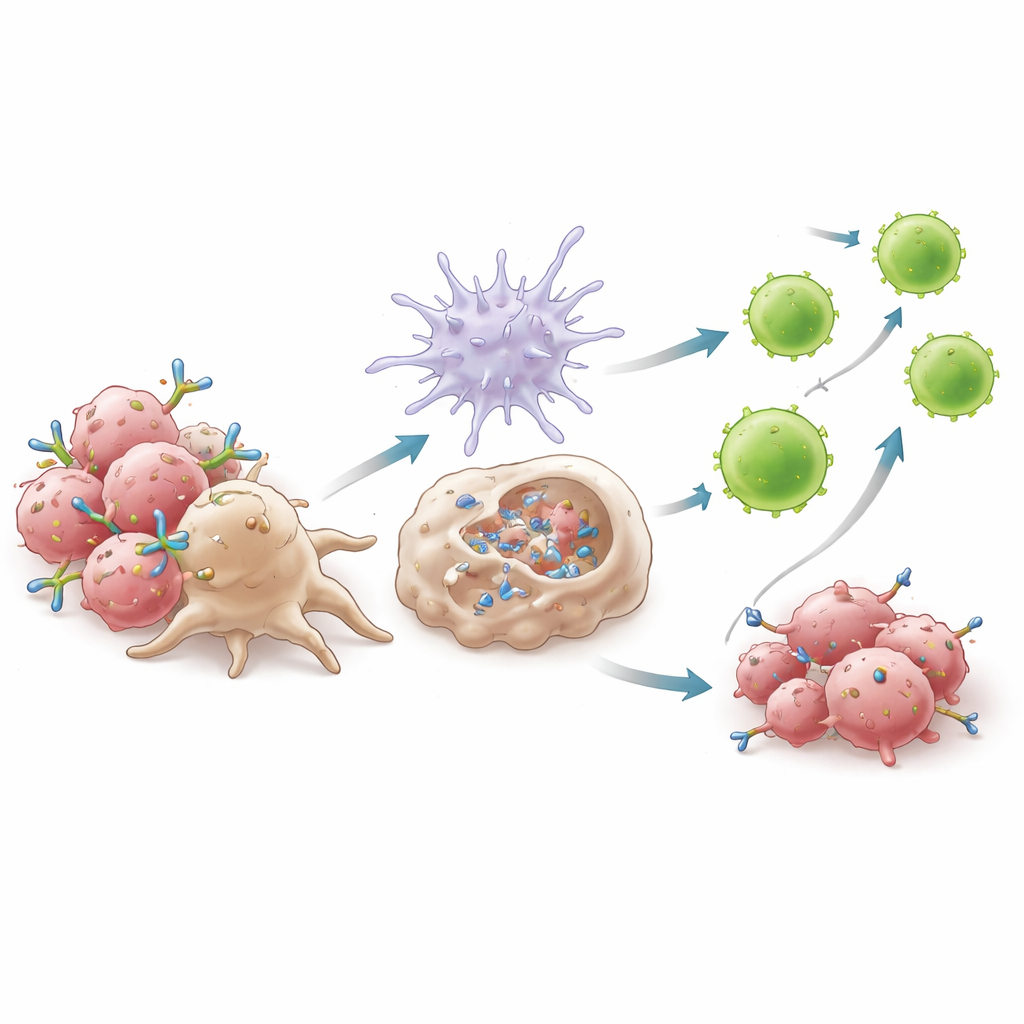
机制学实验表明,6C5的成功取决于它如何将巨噬细胞与肿瘤细胞连接。由于结合位点靠近膜面,6C5形成的紧凑簇状结构更易被巨噬细胞受体有效抓握,从而增强一种称为抗体依赖性细胞吞噬的过程。在6C5存在时,巨噬细胞更容易吞噬有抗体包裹的肿瘤细胞,但若改变抗体的尾部以阻断与巨噬细胞受体的接触,这种吞噬就会减弱。这种吞噬触发了I型干扰素的产生——强效的警报分子——其途径依赖于接头蛋白MyD88。随后这些干扰素激活树突状细胞,增强其呈递肿瘤片段的能力并促进其向淋巴结迁移。在淋巴结中,它们促发了细胞毒性CD8+ T细胞的波动性激活,尤其是一类富含效应分子的高活性亚群,这些T细胞随后返回肿瘤进行攻击。
揭示辅助T细胞中的一个隐蔽刹车
尽管6C5激发了强烈的抗肿瘤反应,但它也暴露出一种意想不到的免疫自我破坏形式。治疗扩增了一类不表达经典调节性T细胞标志Foxp3但表现出类似抑制性功能的CD4+ T细胞群体。这些细胞高表达PD-1和CTLA-4等检查点分子,产生更少的生长因子IL-2,并释放更多免疫抑制信号。去除所有CD4+ T细胞虽然增强了肿瘤控制,却牺牲了长期免疫记忆,强调并非所有辅助细胞都是有害的。因此,作者采取间接策略针对这一“类Treg”高PD-1亚群。将6C5与双重检查点阻断(抗–PD-1加抗–CTLA-4)联合使用,选择性减少了肿瘤中的这些抑制性细胞,同时保留了有益的T细胞并进一步改善了肿瘤控制。
用联合疗法建立持久保护
因为Tregs和这些高PD-1辅助细胞都大量消耗IL-2,研究团队还测试了一种下一代药物,该药将改造过的IL-2信号偶联到PD-1上,将其作用聚焦于耗竭的肿瘤浸润T细胞。当6C5与这种以PD-1为靶的IL-2融合蛋白联合使用时,约一半的小鼠完全清除了肿瘤。值得注意的是,所有治愈的动物在随后重新挑战肿瘤时都能将其排斥,表明具备强大且持久的免疫记忆。相比之下,单纯清除CD4+ T细胞并未产生这种持久保护。总体而言,这些结果表明,调节而非消灭CD4+细胞群体可以释放强大的抗癌免疫,同时不破坏免疫系统“记住”肿瘤的能力。
这对未来癌症治疗可能意味着什么
本研究表明,抗体结合到肿瘤分子的哪个位置可从根本上改变其动员免疫系统的方式。通过靶向AXL的膜近端位点,6C5的作用更像免疫放大器而非单纯的信号阻断器——它推动巨噬细胞清除、干扰素警报、树突状细胞激活以及强有力的杀伤性T细胞攻击。与此同时,研究揭示了治疗过程中出现的新型非经典抑制性T细胞,并展示了如何通过与检查点抑制剂或基于IL-2的制剂的定制组合来中和这些刹车。如果类似的抗体和策略在人类中证明安全且有效,它们可能为将顽固的免疫冷肿瘤转化为对免疫治疗有反应的免疫热肿瘤提供一种途径。
引用: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
关键词: 癌症免疫疗法, 肿瘤微环境, AXL抗体, 巨噬细胞吞噬, 免疫检查点耐药