Clear Sky Science · nl
Hertprogrammatie van het tumormilieu met een antilichaam tegen membraan-proximale AXL om weerstand tegen immuuncheckpointblokkade te overwinnen
Waarom sommige tumoren voor het immuunsysteem verborgen blijven
Kankerimmunotherapie heeft de behandeling van veel patiënten veranderd, maar faalt nog steeds bij een groot deel van tumoren die het immuunsysteem nauwelijks opmerkt. Deze zogenaamde “koude” tumoren bevatten weinig aanvallende immuuncellen en zijn vaak resistent tegen de krachtigste checkpointmiddelen van nu. Deze studie onderzoekt een nieuw type antilichaam dat de eerstelijnsverdediging van het lichaam binnen zulke tumoren activeert, waardoor een koude, stille kanker verandert in een tumor die wemelt van tumor-dodende immuuncellen.
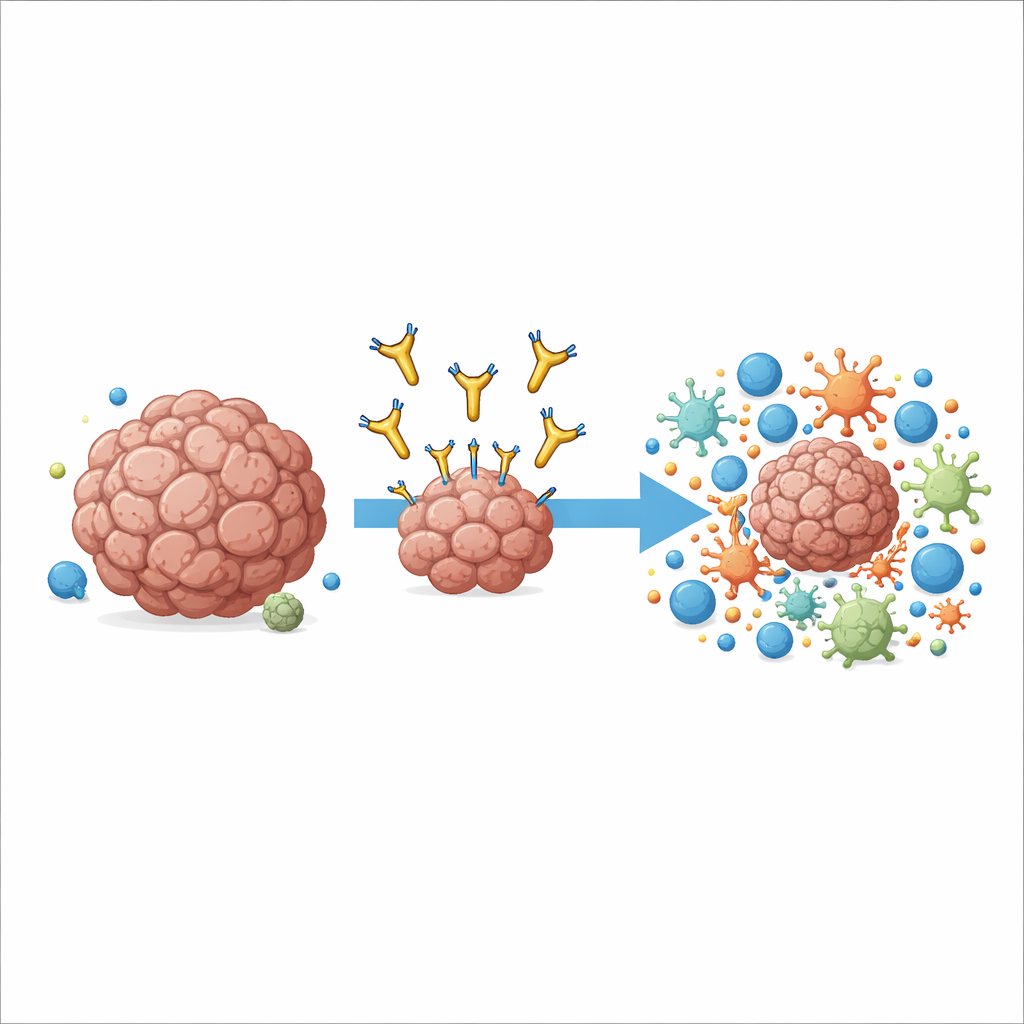
Een nieuwe manier om een bekend kankermolecuul te richten
Het werk concentreert zich op een molecule genaamd AXL, die op het oppervlak van veel kankercellen en sommige immuuncellen in de tumor zit. Hoge AXL-niveaus worden geassocieerd met agressieve ziekte, uitzaaiing naar andere organen en resistentie tegen standaardimmunotherapieën. Eerdere middelen probeerden het groeisignaal van AXL te blokkeren door zich aan de buitenste punt vast te hechten, maar die gaven in klinische onderzoeken slechts bescheiden voordelen en veroorzaakten soms bijwerkingen. De auteurs kozen een andere aanpak: ze ontwikkelden een antilichaam, 6C5 genoemd, dat AXL heel dicht bij het celmembraan pakt in plaats van aan de verre tip. Deze subtiele verschuiving in aanhechtingspositie bleek cruciaal te zijn voor hoe het immuunsysteem het antilichaam als greepsteen kon gebruiken.
De opruimers van het lichaam rekruteren
In plaats van kankercellen rechtstreeks te vergiftigen, werkt 6C5 door immuuncellen in te roepen en om te leiden die gespecialiseerd zijn in het opnemen en verwerken van celresten, met name macrofagen en bepaalde dendritische cellen. In muismodellen van melanoom en colonkanker die zodanig zijn aangepast dat ze menselijke AXL dragen, vertraagde 6C5 tumorgroei krachtig of deed tumoren zelfs krimpen, inclusief longmetastasen, maar alleen wanneer tumorcellen AXL toonden. Het antilichaam had weinig effect in muizen zonder T- en B-cellen, wat aantoont dat blijvende tumorcontrole afhankelijk was van een volledige adaptieve immuunrespons. Gedetailleerde single-cell-analyses van behandelde tumoren toonden aan dat 6C5 het aantal en de activiteit van macrofagen, dendritische cellen en cytotoxische T-cellen in de tumormassa dramatisch vergrootte, waardoor een dunbevolkte immuindesert veranderde in een druk slagveld.
Hoe antilichaam-geleide opruiming een brede immuunaanval ontketent
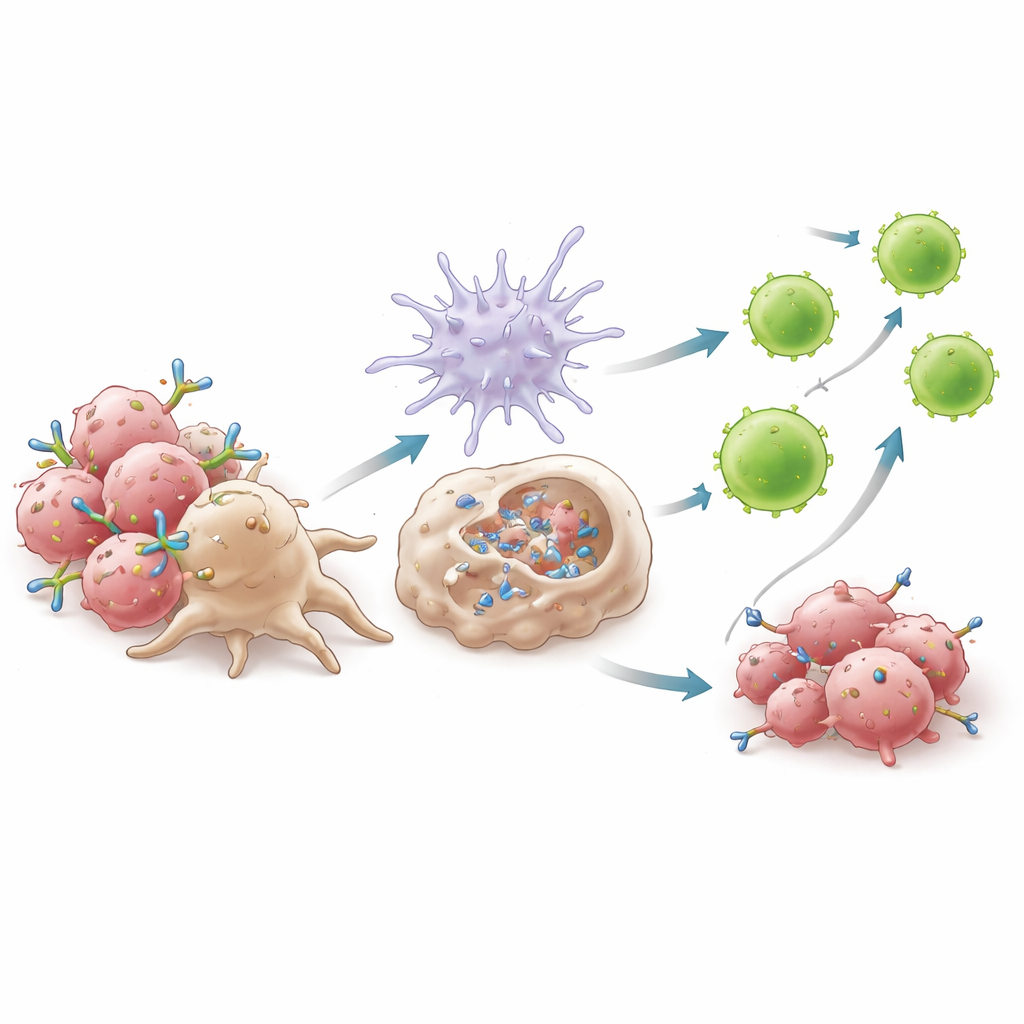
Mechanistische experimenten toonden aan dat het succes van 6C5 afhangt van hoe het macrofagen aan tumorcellen bindt. Door AXL dicht bij het membraan te grijpen vormt 6C5 compacte clusters die macrofaagreceptoren efficiënt kunnen vastpakken, wat een proces genaamd antilichaam-gedreven cellulaire fagocytose versterkt. Macrofagen namen antilichaam-omhulde tumorcellen gemakkelijker op wanneer 6C5 aanwezig was, maar niet wanneer het Fc-gedeelte van het antilichaam was gewijzigd om interactie met macrofaagreceptoren te voorkomen. Deze opname leidde tot productie van type I interferonen—krachtige alarmerende moleculen—via een route die afhankelijk was van het adaptor-eiwit MyD88. Deze interferonen activeerden op hun beurt dendritische cellen, verhoogden hun vermogen om tumordeeltjes te presenteren en stimuleerden hun migratie naar lymfeklieren. Daar zetten ze golven van cytotoxische CD8+ T-cellen in gang, met name een zeer actieve subset gemarkeerd door sterke effector-moleculen, die vervolgens terugkeerden naar de tumor om aan te vallen.
Een verborgen rem in hulp-T-cellen ontdekken
Hoewel 6C5 een krachtige antitumorrespons opwekte, onthulde het ook een onverwachte vorm van immuunsabotage. De behandeling breidde een populatie CD4+ T-cellen uit die niet het klassieke Treg-marker Foxp3 droegen maar zich op vergelijkbare onderdrukkende wijze gedroegen. Deze cellen uitten zeer hoge niveaus van checkpointmoleculen zoals PD-1 en CTLA-4, produceerden minder van de groeifactor IL-2 en gaven meer immunosuppressieve signalen af. Het uitroeien van alle CD4+ T-cellen verbeterde de tumorcontrole maar offerde het langetermijn immuungeheugen op, wat benadrukt dat niet alle helpercellen schadelijk zijn. In plaats daarvan richtten de auteurs zich indirect op deze “Treg-achtige” PD-1–hoge subset. Door 6C5 te combineren met dubbele checkpointblokkade (anti–PD-1 plus anti–CTLA-4) werd deze onderdrukkende populatie selectief verminderd in tumoren, terwijl gunstige T-cellen behouden bleven en de tumorcontrole verder verbeterde.
Duurbare bescherming opbouwen met combinatietherapie
Aangezien zowel Tregs als deze PD-1–hoge hulpcellen gretige verbruikers van IL-2 zijn, testte het team ook een volgende-generatie middel dat een gemodificeerd IL-2-signaal koppelt aan PD-1, waardoor de werking wordt gericht op uitgeputte tumor-infiltrerende T-cellen. Wanneer 6C5 werd gecombineerd met deze PD-1–gerichte IL-2-fusie, maakten ongeveer de helft van de muizen hun tumoren volledig schoon. Opmerkelijk was dat alle genezen dieren een latere tumorhertest afwezen, wat wijst op robuust en langdurig immuungeheugen. Daarentegen bood het eenvoudig verwijderen van CD4+ T-cellen deze duurzame bescherming niet. Gezamenlijk tonen deze resultaten aan dat het fijntunen in plaats van uitroeien van de CD4+ populatie sterke antikanker-immuniteit kan ontketenen zonder het vermogen van het immuunsysteem om de tumor te "onthouden" te ondermijnen.
Wat dit kan betekenen voor toekomstige kankerbehandeling
Deze studie laat zien dat de plaats waar een antilichaam op een tumormolecuul bindt fundamenteel kan veranderen hoe het het immuunsysteem inroept. Door een membraan-proximaal epitopen op AXL te richten, werkt 6C5 minder als een signaalblokker en meer als een immuunversterker—het stimuleert macrofaag-opruiming, interferon-alarmen, activatie van dendritische cellen en krachtige aanvallen van killer-T-cellen. Tegelijkertijd maakt het werk nieuwe, niet-klassieke onderdrukkende T-cellen zichtbaar die tijdens de therapie ontstaan en laat zien hoe op maat gemaakte combinaties met checkpointremmers of IL-2–gebaseerde middelen deze remmen kunnen neutraliseren. Als soortgelijke antilichamen en strategieën veilig en effectief blijken te zijn bij mensen, kunnen ze een manier bieden om hardnekkige immuunkoude tumoren om te zetten in immuunhete tumoren die eindelijk reageren op immunotherapie.
Bronvermelding: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Trefwoorden: kankerimmunotherapie, tumormilieu, AXL-antilichaam, fagocytose door macrofagen, weerstand tegen immuuncheckpoints