Clear Sky Science · ru
Перепрограммирование микросреды опухоли с помощью антитела против мембранно‑проксимального AXL для преодоления резистентности к ингибиторам контрольных точек
Почему некоторые опухоли «скрываются» от иммунной системы
Иммунотерапия рака изменила подход к лечению многих пациентов, но по‑прежнему не работает в большом числе случаев — в тех опухолях, которые иммунная система практически не замечает. Такие «холодные» опухоли содержат мало атакующих иммунных клеток и часто устойчивы к современным препаратам, нацеленным на контрольные точки. В этом исследовании изучается новый тип антитела, который пробуждает первичные защитные силы организма внутри таких опухолей, помогая превратить холодный, бесшумный рак в опухоль, кишащую клетками, убивающими опухоль.
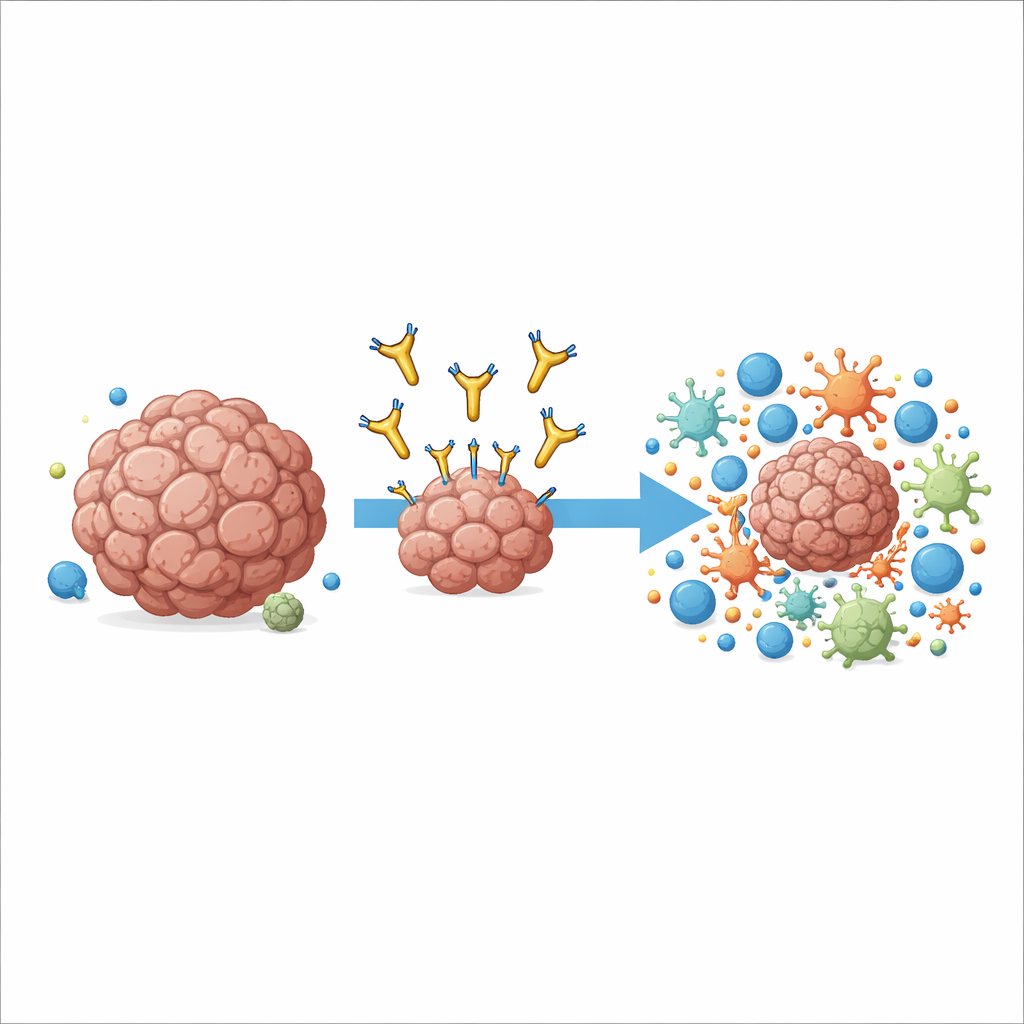
Новый способ нацелиться на известную мишень в раке
Работа сосредоточена на молекуле AXL, расположенной на поверхности многих раковых клеток и некоторых иммунных клеток в опухоли. Высокий уровень AXL связан с агрессивным течением болезни, метастазированием и резистентностью к стандартной иммунотерапии. Ранее препараты пытались блокировать сигналы роста AXL, связываясь с его внешним концевым участком, но в клинических испытаниях они показали лишь скромную пользу и иногда вызывали побочные эффекты. Авторы избрали другой путь: они создали антитело под названием 6C5, которое захватывает AXL очень близко к мембране клетки, а не на удалённом кончике. Это тонкое смещение точки связывания оказалось решающим для того, как иммунная система может использовать антитело как «ручку».
Привлечение «уборщиков» организма
Вместо прямого уничтожения раковых клеток 6C5 действует, привлекая и перенаправляя иммунные клетки, специализирующиеся на поедании и переработке мусора, в частности макрофаги и определённые дендритные клетки. В моделях мышей с меланомой и колоректальным раком, генетически модифицированных для экспрессии человеческого AXL, 6C5 сильно замедлял или даже уменьшал опухоли, включая метастазы в лёгкие, но только когда опухолевые клетки экспрессировали AXL. Антитело мало влияло на рост опухолей у мышей, лишённых Т‑ и В‑клеток, что указывает на то, что длительный контроль опухоли зависел от полноценного адаптивного ответа. Детализированный анализ одиночных клеток в обработанных опухолях показал, что 6C5 драматически увеличивал число и активность макрофагов, дендритных клеток и цитотоксических Т‑клеток, инфильтрирующих массу опухоли, превращая скудную иммунную пустыню в оживлённое поле боя.
Как антитело‑направленный «убор» вызывает более широкий иммунный ответ
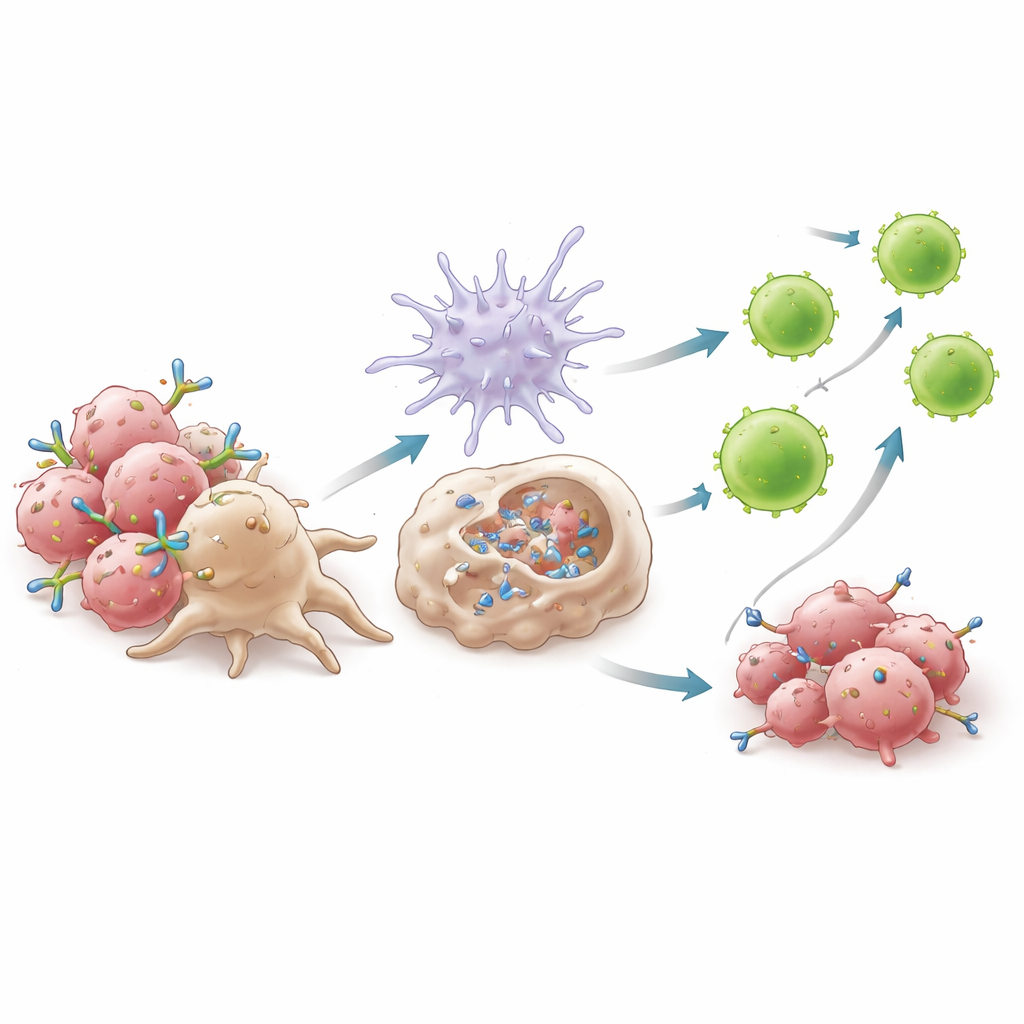
Механистические эксперименты показали, что успех 6C5 зависит от того, как оно прикрепляет макрофаги к опухолевым клеткам. Связываясь с AXL близко к мембране, 6C5 формирует компактные кластеры, за которые рецепторы макрофагов могут надёжно «схватиться», усиливая процесс, называемый анти‑тело‑зависимым клеточным фагоцитозом. Макрофаги охотнее поглощали покрытые антителом опухолевые клетки в присутствии 6C5, но не тогда, когда участок Fc антитела был изменён так, чтобы предотвращать взаимодействие с рецепторами макрофагов. Этот акт поедания вызывал выработку интерферонов типа I — мощных сигнальных молекул тревоги — через путь, опосредованный адаптерным белком MyD88. Эти интерфероны активировали дендритные клетки, повышали их способность представлять фрагменты опухоли и стимулировали их миграцию в лимфоузлы. Там они инициировали волны цитотоксических CD8+ Т‑клеток, особенно высокоактивного подмножества с выраженными эффекторными молекулами, которые затем возвращались в опухоль для атаки.
Обнаружение скрытого «тормоза» среди помощников‑Т клеток
Хотя 6C5 вызвало мощный противоопухолевый ответ, лечение также выявило неожиданный механизм самосаботажа иммунитета. Терапия увеличивала популяцию CD4+ Т‑клеток, не несущих классического маркера регуляторных Т‑клеток Foxp3, но ведущих себя подобно ним и обладающих иммунодепрессивными свойствами. Эти клетки экспрессировали очень высокие уровни контрольных молекул, таких как PD‑1 и CTLA‑4, продуцировали меньше ростового фактора IL‑2 и вырабатывали больше иммуносупрессивных сигналов. Истощение всех CD4+ Т‑клеток усиливало контроль опухоли, но при этом жертвовало долгосрочной иммунной памятью, подчёркивая, что не все хелперные клетки вредны. Вместо полного уничтожения авторы нацелились на это «Treg‑подобное» PD‑1‑высокое подмножество косвенно. Комбинация 6C5 с двойной блокадой контрольных точек (анти–PD‑1 плюс анти–CTLA‑4) селективно сокращала эти подавляющие клетки в опухолях, сохраняя при этом полезные Т‑клетки и ещё больше улучшая контроль опухоли.
Создание долговременной защиты с помощью комбинированной терапии
Поскольку как классические Treg, так и эти PD‑1‑высокие помощники активно потребляют IL‑2, команда также протестировала препарат следующего поколения, который связывает модифицированный сигнал IL‑2 с PD‑1, фокусируя его действие на истощённых опухольно‑инфильтрирующих Т‑клетках. При сочетании 6C5 с этим PD‑1‑таргетированным IL‑2‑фьюжном примерно у половины мышей опухоли полностью исчезли. Примечательно, что все вылеченные животные отвергли повторную пересадку опухоли, что свидетельствует о надёжной и длительной иммунной памяти. Напротив, простое удаление CD4+ Т‑клеток не давало такой устойчивой защиты. В совокупности результаты показывают, что настройка, а не уничтожение CD4+ сектора может высвободить сильный противораковый иммунитет, не подрывая способность иммунной системы «запоминать» опухоль.
Что это может значить для будущего лечения рака
Это исследование демонстрирует, что место связывания антитела на опухолевой молекуле принципиально меняет способ его вовлечения иммунной системы. Нацеливание на мембранно‑проксимальную область AXL превращает 6C5 из простого блокатора сигналов в усилитель иммунитета — он стимулирует уборку макрофагами, интерферонные сигналы тревоги, активацию дендритных клеток и мощные атаки цитотоксических Т‑клеток. Одновременно работа выявляет новые, нетипичные супрессивные Т‑клетки, возникающие во время терапии, и показывает, как подобранные комбинации с ингибиторами контрольных точек или агентами на базе IL‑2 могут нейтрализовать эти «тормоза». Если аналогичные антитела и стратегии окажутся безопасными и эффективными у людей, они могут предложить способ превратить упорные иммунно‑холодные опухоли в иммунно‑горячие, которые наконец ответят на иммунотерапию.
Цитирование: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Ключевые слова: иммунотерапия рака, микросреда опухоли, антитело к AXL, фагоцитоз макрофагами, резистентность к ингибиторам иммунных контрольных точек