Clear Sky Science · he
תכנות מחודש של מיקרוסביבת הגידול בעזרת נוגדן כנגד AXL קרוב לממברנה כדי להתגבר על עמידות לחסימת נקודות ביקורת חיסונית
למה חלק מהגידולים מתחבאים מהמנגנון החיסוני
אימונותרפיה לסרטן שינתה את הטיפול עבור מטופלים רבים, אך היא עדיין נכשלת בשיעור ניכר של גידולים שהמערכת החיסונית כמעט ואינה מבחינה בהם. גידולים אלה, המכונים "קרים", מכילים מעט תאי חיסון תוקפים ולעתים קרובות עמידים לתרופות החזקות נגד נקודות הביקורת כיום. מחקר זה בוחן סוג חדש של נוגדן שמעורר את קווי ההגנה הראשוניים בגוף בתוך גידולים כאלה, ועוזר להפוך סרטן קר ושקט לסרטן מלא בתאי חיסון שהורגים גידולים.
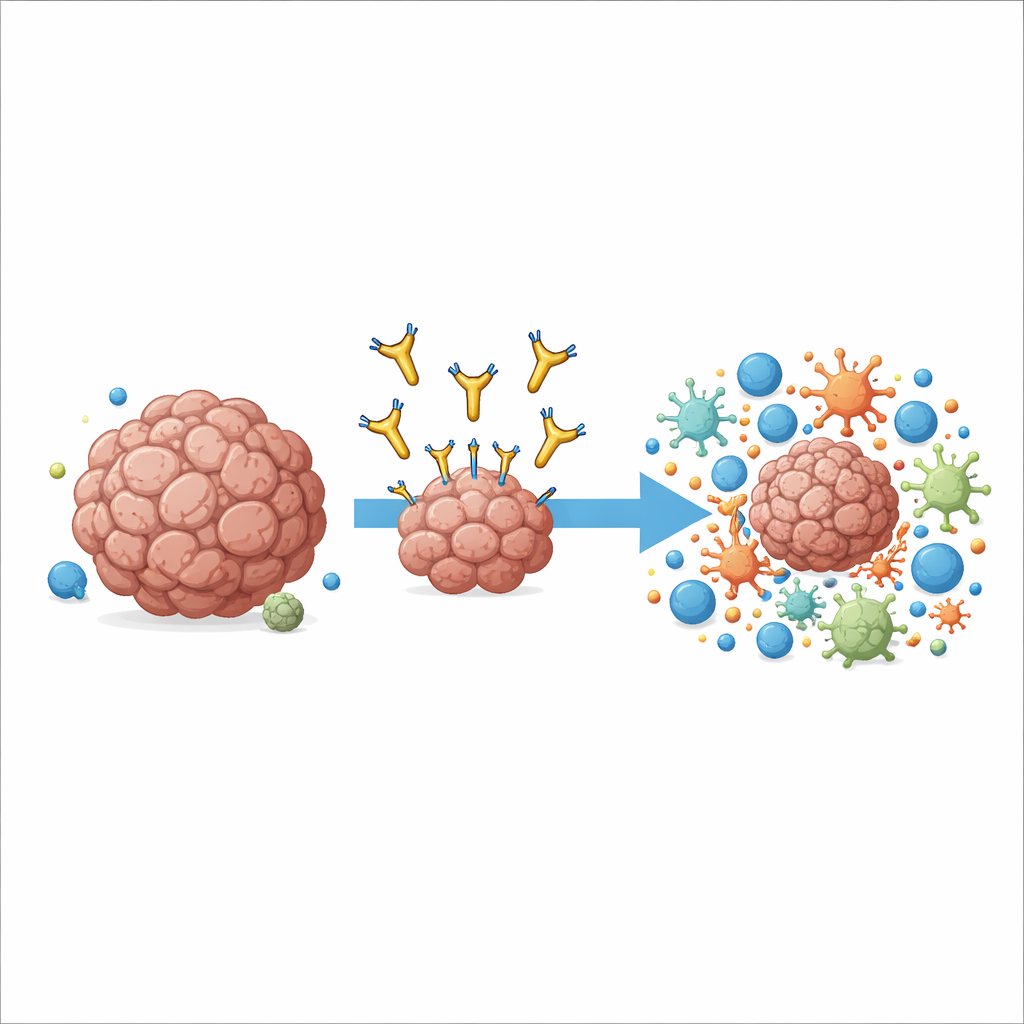
דרך חדשה לכיוון מטרה מוכרת בסרטן
העבודה מתמקדת במולקולה בשם AXL, הנמצאת על פני השטח של תאים סרטניים רבים וכמה תאי חיסון בגידול. רמות גבוהות של AXL מקושרות למחלה אגרסיבית, לפיזור לאיברים אחרים ולעמידות לאימונותרפיות סטנדרטיות. תרופות קודמות ניסו לחסום את אות הצמיחה של AXL על‑ידי קשירה לקצה החיצוני שלה, אך הן הראו תועלת מתונה בניסויים קליניים ולעתים גרמו לתופעות לוואי. המחברים נקטו בגישה שונה: הם בנו נוגדן בשם 6C5, הקושר את AXL בקרבה לממברנה של התא במקום בקצה המרוחק. הזזת עיגון עדינה זו התגלתה כקריטית לאופן שבו המערכת החיסונית יכולה להשתמש בנוגדן כידית.
גיוס "פוחלצים" של הגוף
במקום להרוס תאים סרטניים ישירות, 6C5 פועל על־ידי קריאה וניתוב מחדש של תאי חיסון המתמחים בבליעה ועיבוד שברי תאים, בעיקר מאקרופגים וכמה תאי דנדריט. במודלים עכבריים של מלנומה וסרטן המעי שהונדסו לשאת AXL אנושי, 6C5 האט בעוצמה או אף הקטין את הגידולים, כולל גרורות ריאתיות, אך רק כאשר תאי הגידול ביטאו AXL. הנוגדן הראה השפעה מועטה בעכברים שחסרו תאי T ו-B, מה שמראה כי שליטה ממושכת על הגידול תלויה בתגובה חיסונית אדפטיבית מלאה. ניתוחים חד‑תאיים מפורטים של גידולים מטופלים חשפו כי 6C5 הגדיל באופן דרמטי את מספר ותפקוד המאקרופגים, תאי דנדריט ותאי T צודקי הגידול שחדרו למסה הסרטנית, והפך מדבר חיסוני דל לשדה קרב צפוף.
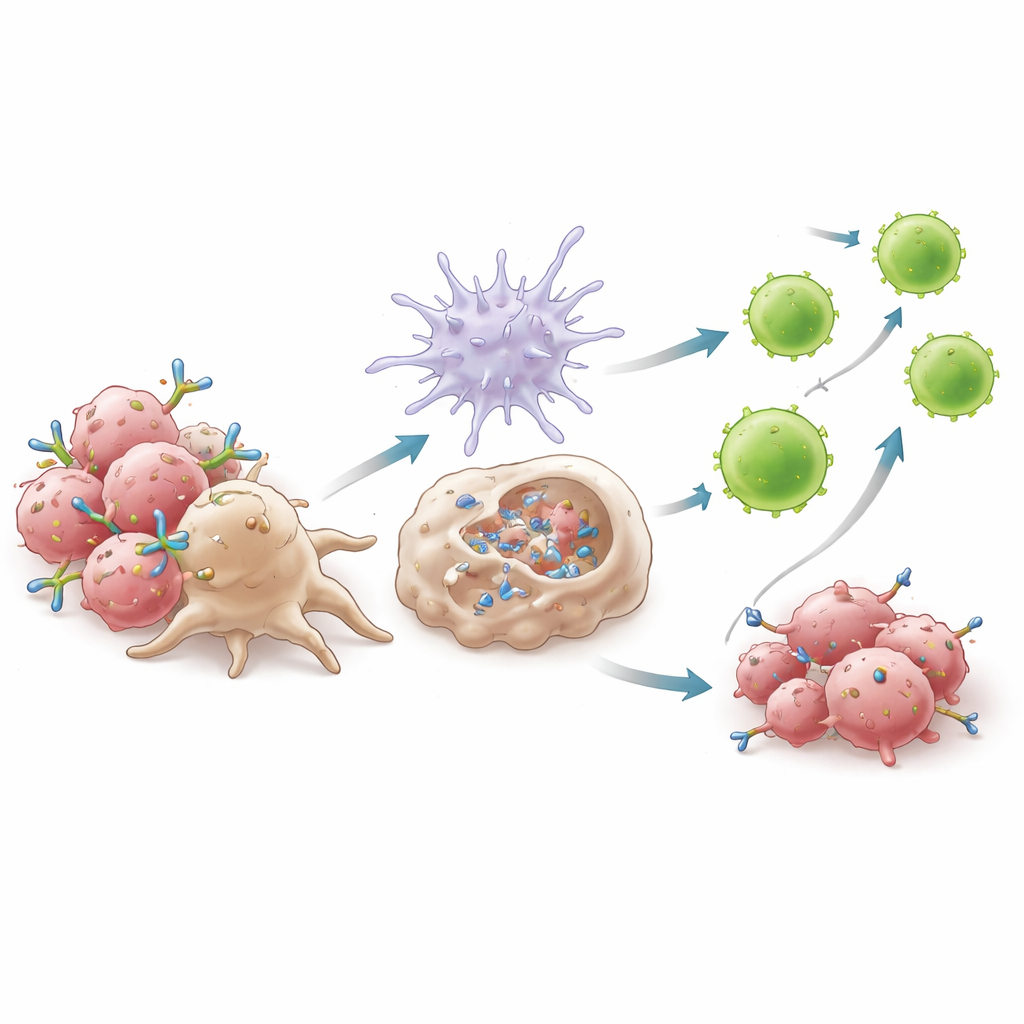
כיצד הניקוי המונחה‑נוגדן מעורר התקפה חיסונית רחבה
ניסויים מנגנוניים הראו שהצלחת 6C5 תלויה בדרך שבה הוא קושר את המאקרופגים לתאי הגידול. בקשירתו ל‑AXL קרוב לממברנה, 6C5 יוצר אשכולות קומפקטיים שיכולים להיתפס ביעילות על ידי קולטני המאקרופגים, ומשפר תהליך שנקרא פגוציטוזה תלויה בנוגדן. מאקרופגים בלעו בקלות יתרה תאים סרטניים מצופים נוגדן כשהיה נוכח 6C5, אך לא כאשר אזור ה‑Fc שלו שונה כדי למנוע אינטראקציה עם קולטני המאקרופגים. הבליעה הזו עוררה ייצור אינטרפרונים מסוג I — מולקולות אזעקה עוצמתיות — דרך מסלול שתלוי בחלבון המאמצע MyD88. אינטרפרונים אלה, בתורם, הפעלו תאי דנדריט, הגדילו את יכולתם להציג שברי גידול ועודדו את הניוד שלהם לקשרי לימפה. שם הם יזמו גל של תאי CD8+ ציטוטוקסיים, במיוחד תת‑אוכלוסיה בעלת פעילות גבוהה המסומנת במולקולות אפקטור חזקות, שחזרו אחר כך אל הגידול לתקוף.
חשיפת מעצור מוסתר בתוך תאי ה‑CD4 המסייעים
בעוד 6C5 עורר תגובה אנטי‑גידולית עזה, הוא גם חשף צורה בלתי צפויה של sabotaage חיסוני פנימי. הטיפול הרחיב אוכלוסייה של תאי CD4+ שלא נשאו את הסמן הקלאסי של Treg, Foxp3, אך התנהגו באופן דמוי‑מעכב דומה. תאים אלה הביעו רמות גבוהות מאוד של מולקולות נקודת ביקורת כגון PD‑1 ו‑CTLA‑4, ייצרו פחות מהצמיחין IL‑2 ויצרו איתותים מדכאים יותר. כריתת כל תאי ה‑CD4 שיפרה את שליטת הגידול אך הקריבה את הזיכרון החיסוני לטווח ארוך, מה שמדגיש שלא כל תאי המסייע מסוכנים. במקום זאת, המחברים טירגטו את תת‑הקבוצה ה"דמוית‑Treg" וגבוהת ה‑PD‑1 בצורה בלתי ישירה. שילוב 6C5 עם חסימת נקודות ביקורת כפולה (נוגד‑PD‑1 יחד עם נוגד‑CTLA‑4) הקטין באופן סלקטיבי תאים מדכאים אלה בגידולים, תוך שמירה על תאי T מועילים ושיפור נוסף בשליטת הגידול.
בניית הגנה ממושכת באמצעות טיפול משולב
מכיוון ששני Treg ותאי המסייעים הגבוהים ב‑PD‑1 צורכים IL‑2 בשפע, הצוות גם בדק תרופה מדור הבא שמחברת אות IL‑2 מותאמת ל‑PD‑1, וממקדת את הפעולה שלה בתאי T עייפים שחדרו לגידול. כאשר 6C5 צומד לאיחוי IL‑2 המכוון ל‑PD‑1, כ‑חצי מהעכברים ניקו את גידולם לחלוטין. מרשים שכל בעלי החיים שהוכרו החליפו דחיית שתל של גידול חוזר מאוחר יותר, מה שמעיד על זיכרון חיסוני חזק ומתמשך. לעומת זאת, הסרה פשוטה של תאי CD4 לא סיפקה הגנה ברת‑קיימא זו. יחד, תוצאות אלה מראות כי כוונון ולא חיסול של מחלקת ה‑CD4 יכול לשחרר חיסון אנטי‑סרטן חזק מבלי לפגוע ביכולת המערכת החיסונית "לזכור" את הגידול.
מה זה יכול להציע לעתיד טיפול בסרטן
מחקר זה מדגים כי המקום בו נוגדן נקשר על מולקולה סרטנית יכול לשנות באופן יסודי כיצד הוא מגייס את המערכת החיסונית. על‑ידי מיקוד אתר קרוב לממברנה על AXL, 6C5 פועל פחות כחוסם אותות ויותר כמגבר חיסוני — מזין ניקוי מאקרופגים, אזעקות אינטרפרון, הפעלת תאי דנדריט והתקפות חזקות של תאי ה‑T הצורבים. במקביל, העבודה חושפת תאים מדכאים חדשים ולא‑קלאסיים שעולים במהלך הטיפול ומציגה כיצד שילובים מותאמים עם מעכבי נקודות ביקורת או סוכני IL‑2 יכולים לנטרל את הבלמים האלה. אם נוגדנים ואסטרטגיות דומות יגלו בטיחות ויעילות בבני אדם, הם עשויים להציע דרך להמיר גידולים עיקשים וקרירים לגידולים חמים חיסונית שמגיבים סוף‑סוף לאימונותרפיה.
ציטוט: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
מילות מפתח: אימונותרפיה לסרטן, מיקרוסביבת הגידול, נוגדן ל-AXL, פגוציטוזה של מאקרופגים, עמידות לנקודות ביקורת חיסוניות