Clear Sky Science · fr
Reprogrammer le microenvironnement tumoral avec un anticorps dirigé contre l’AXL proche de la membrane pour surmonter la résistance aux inhibiteurs de point de contrôle immunitaire
Pourquoi certains tumeurs se cachent du système immunitaire
L’immunothérapie anticancéreuse a transformé le traitement de nombreux patients, mais elle échoue encore dans une grande proportion de tumeurs que le système immunitaire remarque à peine. Ces tumeurs dites « froides » contiennent peu de cellules immunitaires effectrices et résistent souvent aux puissants médicaments inhibiteurs de points de contrôle actuels. Cette étude explore un nouvel anticorps capable de réveiller les défenses de première ligne au sein de ces tumeurs, aidant à transformer un cancer froid et silencieux en une lésion envahie par des cellules immunitaires tueuses de tumeurs.
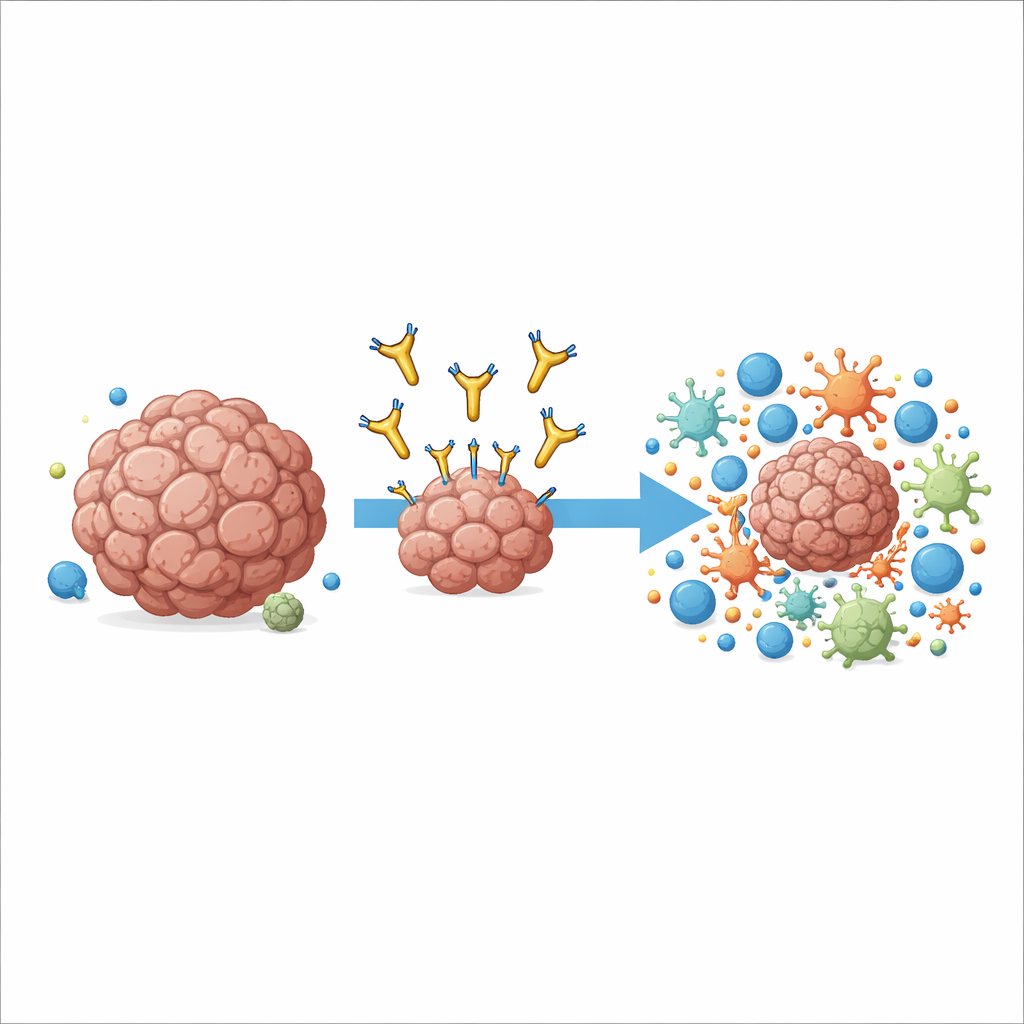
Une nouvelle façon de viser une cible tumorale familière
Les travaux se concentrent sur une molécule appelée AXL, qui se trouve à la surface de nombreuses cellules cancéreuses et de certaines cellules immunitaires dans la tumeur. Des niveaux élevés d’AXL sont associés à une forme agressive de la maladie, à des métastases et à la résistance aux immunothérapies standards. Les traitements antérieurs ont essayé de bloquer le signal de croissance d’AXL en s’attachant à son extrémité la plus exposée, mais ils n’ont montré que des bénéfices modestes en essais cliniques et ont parfois provoqué des effets secondaires. Les auteurs ont adopté une approche différente : ils ont conçu un anticorps, nommé 6C5, qui saisit AXL très près de la membrane cellulaire plutôt qu’à l’extrémité distante. Ce déplacement subtil du point d’ancrage s’est avéré crucial pour la manière dont le système immunitaire peut utiliser l’anticorps comme levier.
Recruter les « balayeurs » du corps
Plutôt que d’empoisonner directement les cellules cancéreuses, 6C5 agit en appelant et en redirigeant des cellules immunitaires spécialisées dans l’engloutissement et le traitement des débris, en particulier les macrophages et certains cellules dendritiques. Dans des modèles murins de mélanome et de cancer du côlon exprimant AXL humain, 6C5 a fortement ralenti voire réduit les tumeurs, y compris les métastases pulmonaires, mais seulement lorsque les cellules tumorales présentaient AXL. L’anticorps avait peu d’effet chez des souris dépourvues de cellules T et B, montrant que le contrôle tumoral durable dépendait d’une réponse immunitaire adaptative complète. Des analyses en cellules uniques détaillées des tumeurs traitées ont révélé que 6C5 augmentait de façon spectaculaire le nombre et l’activité des macrophages, des cellules dendritiques et des lymphocytes T cytotoxiques infiltrant la masse tumorale, convertissant un désert immunitaire clairsemé en un champ de bataille encombré.
Comment le nettoyage guidé par l’anticorps déclenche une attaque immunitaire plus large
Des expériences mécanistiques ont montré que le succès de 6C5 dépend de la manière dont il relie les macrophages aux cellules tumorales. En se liant à AXL proche de la membrane, 6C5 forme des grappes compactes que les récepteurs des macrophages peuvent saisir efficacement, renforçant un processus appelé phagocytose cellulaire dépendante d’anticorps. Les macrophages engloutissaient plus facilement les cellules tumorales recouvertes d’anticorps en présence de 6C5, mais pas lorsque la région Fc de l’anticorps était modifiée pour empêcher l’engagement des récepteurs des macrophages. Cet engloutissement déclenchait la production d’interférons de type I — des molécules d’alerte puissantes — via une voie dépendante de la protéine adaptatrice MyD88. Ces interférons, à leur tour, activaient les cellules dendritiques, augmentaient leur capacité à présenter des fragments tumoraux et favorisaient leur migration vers les ganglions lymphatiques. Là, elles amorçaient des vagues de lymphocytes T CD8+ cytotoxiques, en particulier un sous-ensemble très actif marqué par de fortes molécules effectrices, qui retournaient ensuite à la tumeur pour attaquer.
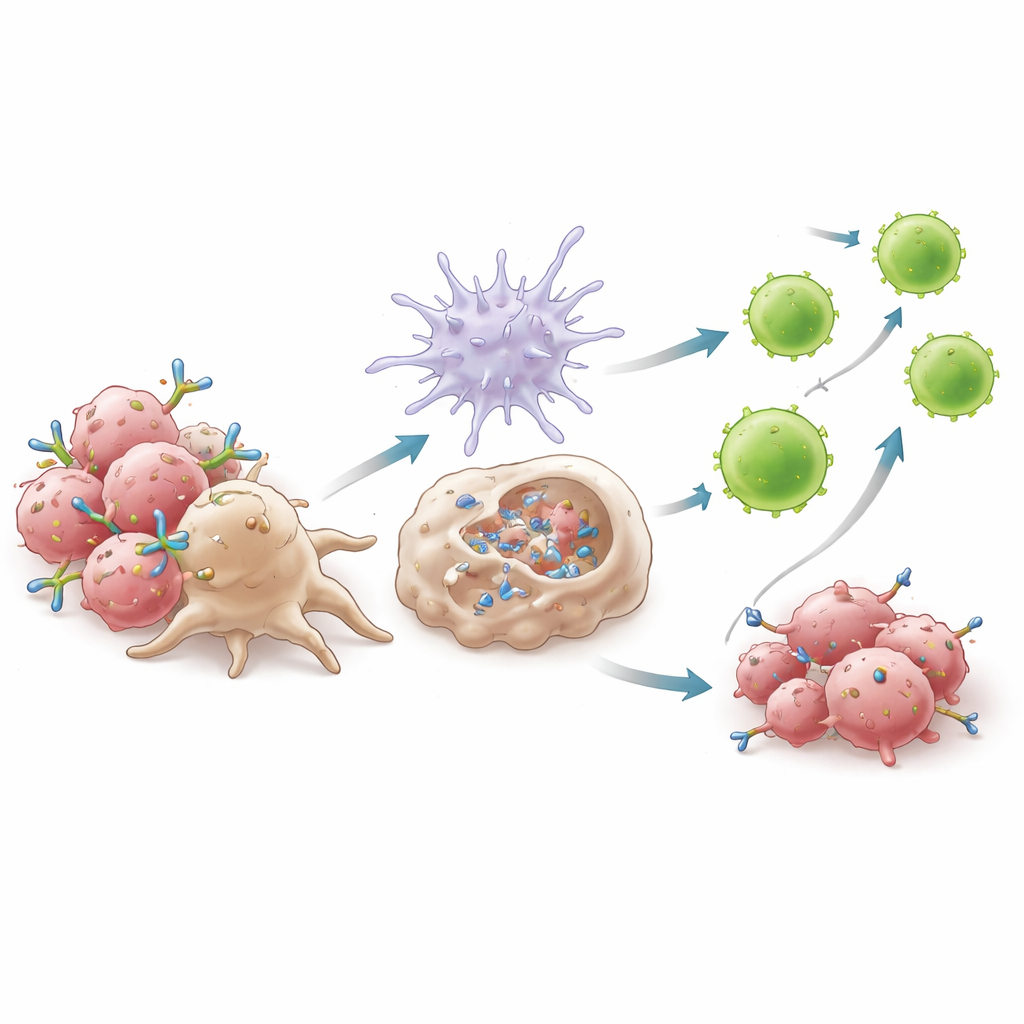
Dégager un frein caché au sein des cellules T auxiliaires
Alors que 6C5 suscitait une réponse antitumorale vigoureuse, il a aussi révélé une forme inattendue d’auto-sabotage immunitaire. Le traitement a élargi une population de lymphocytes T CD4+ qui ne portaient pas le marqueur Treg classique Foxp3 mais se comportaient d’une manière tout aussi suppressive. Ces cellules exprimaient des niveaux très élevés de molécules de point de contrôle telles que PD-1 et CTLA-4, produisaient moins du facteur de croissance IL-2 et émettaient davantage de signaux immunosuppressifs. L’élimination de toutes les cellules CD4+ améliorait le contrôle tumoral mais sacrifiait la mémoire immunitaire à long terme, soulignant que toutes les cellules auxiliaires ne sont pas nuisibles. Les auteurs ont donc ciblé indirectement ce sous-ensemble « Treg-like » PD-1–élevé. La combinaison de 6C5 avec un double blocage des points de contrôle (anti–PD-1 plus anti–CTLA-4) a réduit sélectivement ces cellules suppressives dans les tumeurs, tout en préservant les cellules T bénéfiques et en améliorant davantage le contrôle tumoral.
Construire une protection durable avec une thérapie combinée
Parce que les Tregs et ces cellules auxiliaires PD-1–élevées consomment abondamment l’IL-2, l’équipe a également testé un médicament de nouvelle génération qui couple un signal IL-2 modifié à PD-1, focalisant son action sur les cellules T épuisées infiltrant la tumeur. Lorsque 6C5 a été associé à cette fusion IL-2 ciblant PD-1, environ la moitié des souris ont complètement éradiqué leurs tumeurs. De manière remarquable, tous les animaux guéris ont rejeté une rechallenge tumorale ultérieure, indiquant une mémoire immunitaire robuste et durable. En revanche, la simple suppression des cellules CD4+ ne conférait pas cette protection durable. Ensemble, ces résultats montrent que régler plutôt qu’éradiquer le compartiment CD4+ peut libérer une forte immunité anticancéreuse sans compromettre la capacité du système immunitaire à « se souvenir » de la tumeur.
Ce que cela pourrait signifier pour les traitements du cancer à venir
Cette étude démontre que l’endroit où un anticorps se lie sur une molécule tumorale peut changer fondamentalement la façon dont il mobilise le système immunitaire. En ciblant un site proche de la membrane sur AXL, 6C5 agit moins comme un bloqueur de signal et davantage comme un amplificateur immunitaire — stimulant le nettoyage par les macrophages, les alertes aux interférons, l’activation des cellules dendritiques et des attaques puissantes des lymphocytes T tueurs. Parallèlement, le travail met au jour de nouvelles cellules T suppressives non classiques qui émergent pendant la thérapie et montre comment des combinaisons adaptées avec des inhibiteurs de points de contrôle ou des agents à base d’IL-2 peuvent neutraliser ces freins. Si des anticorps et stratégies similaires s’avèrent sûrs et efficaces chez l’humain, ils pourraient offrir un moyen de convertir des tumeurs récalcitrantes et immunologiquement froides en tumeurs immuno-chaudes qui répondent enfin à l’immunothérapie.
Citation: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Mots-clés: immunothérapie du cancer, microenvironnement tumoral, anticorps anti-AXL, phagocytose par les macrophages, résistance aux inhibiteurs de point de contrôle