Clear Sky Science · sv
Omdanande tumörmikromiljön med antikropp mot membran-nära AXL för att övervinna resistens mot checkpoint-hämning
Varför vissa tumörer gömmer sig från immunsystemet
Cancerimmunoterapi har förändrat behandlingen för många patienter, men den misslyckas fortfarande i en stor andel tumörer som immunsystemet nästan inte känner igen. Dessa så kallade ”kalla” tumörer innehåller få angripande immunceller och är ofta resistenta mot dagens kraftfulla checkpoint-läkemedel. Denna studie undersöker en ny typ av antikropp som väcker kroppens förstalinjeförsvar inne i sådana tumörer och hjälper till att förvandla en kall, tyst cancer till en som myllrar av tumördödande immunceller.
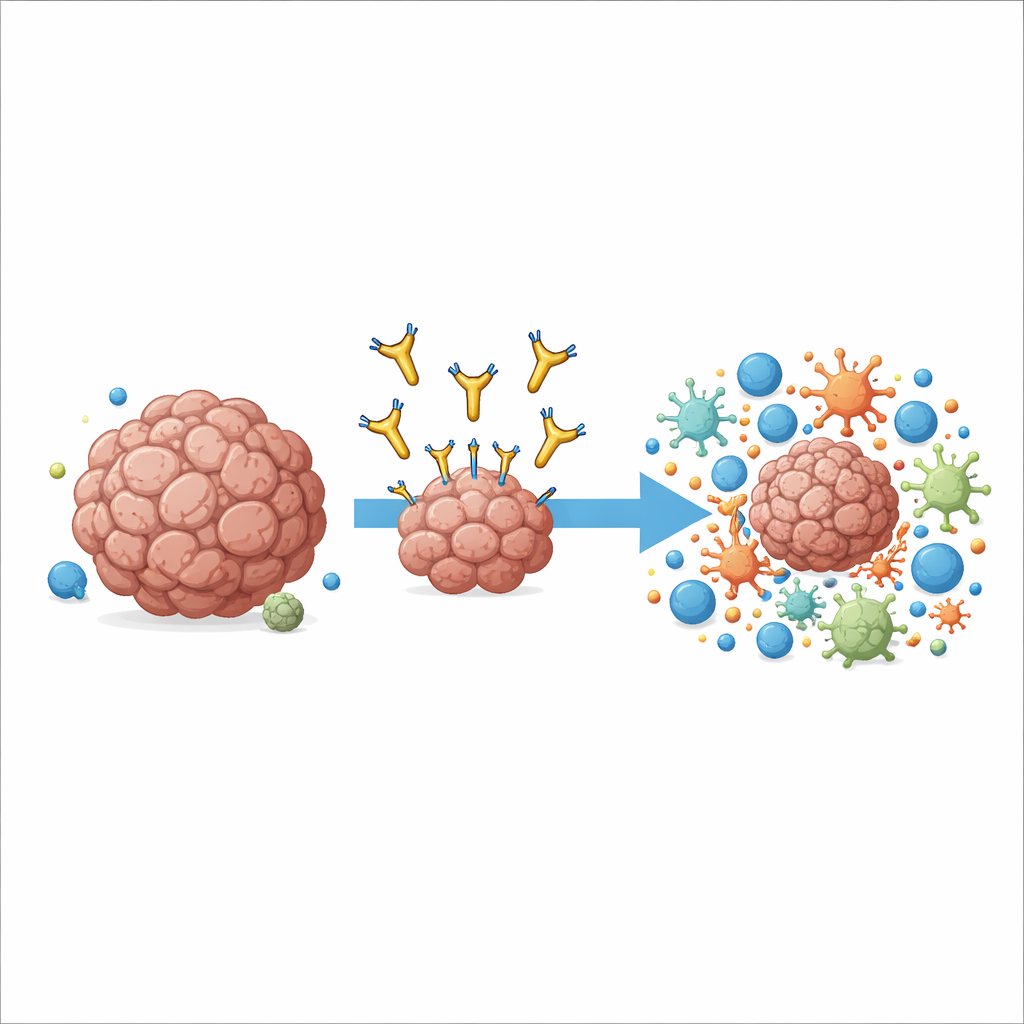
Ett nytt sätt att sikta på ett välkänt cancermål
Arbetet fokuserar på ett molekylärt mål kallat AXL, som finns på ytan av många cancerceller och vissa immunceller i tumören. Höga nivåer av AXL är kopplade till aggressiv sjukdom, spridning till andra organ och resistens mot standardimmunoterapier. Tidigare läkemedel försökte blockera AXL:s tillväxtsignal genom att fästa vid dess yttersta spets, men de visade endast måttliga fördelar i kliniska prövningar och orsakade ibland biverkningar. Författarna valde en annan strategi: de utvecklade en antikropp, kallad 6C5, som griper AXL mycket nära cellmembranet i stället för vid den avlägsna spetsen. Denna subtila förskjutning i bindningsposition visade sig vara avgörande för hur immunsystemet kunde använda antikroppen som ett handtag.
Att rekrytera kroppens sopuppsamlare
Istället för att direkt förgifta cancerceller fungerar 6C5 genom att kalla in och omdirigera immunceller som specialiserat sig på att omsluka och bearbeta skräp, framför allt makrofager och vissa dendritiska celler. I musmodeller av melanom och koloncancer som konstruerats för att bära human AXL, saktade 6C5 kraftigt ner tumörtillväxt eller krympte tumörer, inklusive lungmetastaser, men endast när tumörcellerna visade AXL. Antikroppen hade liten effekt i möss utan T- och B-celler, vilket visar att varaktig tumörkontroll berodde på ett fullt adaptivt immunsvar. Detaljerade singelcellsanalyser av behandlade tumörer avslöjade att 6C5 dramatiskt ökade antalet och aktiviteten hos makrofager, dendritiska celler och cytotoxiska T-celler som infiltrerade tumörmassan, och förvandlade en gles immunöken till en välbefolkad slagfält.
Hur antikroppsledd städning sätter igång ett bredare immunsvar
Mekanistiska experiment visade att 6C5:s framgång vilar på hur den länkar makrofager till tumörceller. Genom att binda AXL nära membranet bildar 6C5 kompakta kluster som makrofagreceptorer effektivt kan greppa, vilket ökar en process kallad antikroppsberoende cellulär fagocytos. Makrofager svalt lättare antikroppstäckta tumörceller när 6C5 var närvarande, men inte när dess svansregion var förändrad så att den inte kunde engagera makrofagreceptorer. Denna omslutning utlöste produktion av typ I-interferoner — potenta alarmsubstanser — via en väg som krävde adaptorproteinet MyD88. Dessa interferoner aktiverade i sin tur dendritiska celler, ökade deras förmåga att presentera tumörfragment och uppmuntrade deras migration till lymfkörtlar. Där primade de vågor av cytotoxiska CD8+ T-celler, särskilt en mycket aktiv undergrupp märkt av starka effektormolekyler, som sedan återvände till tumören för att attackera.
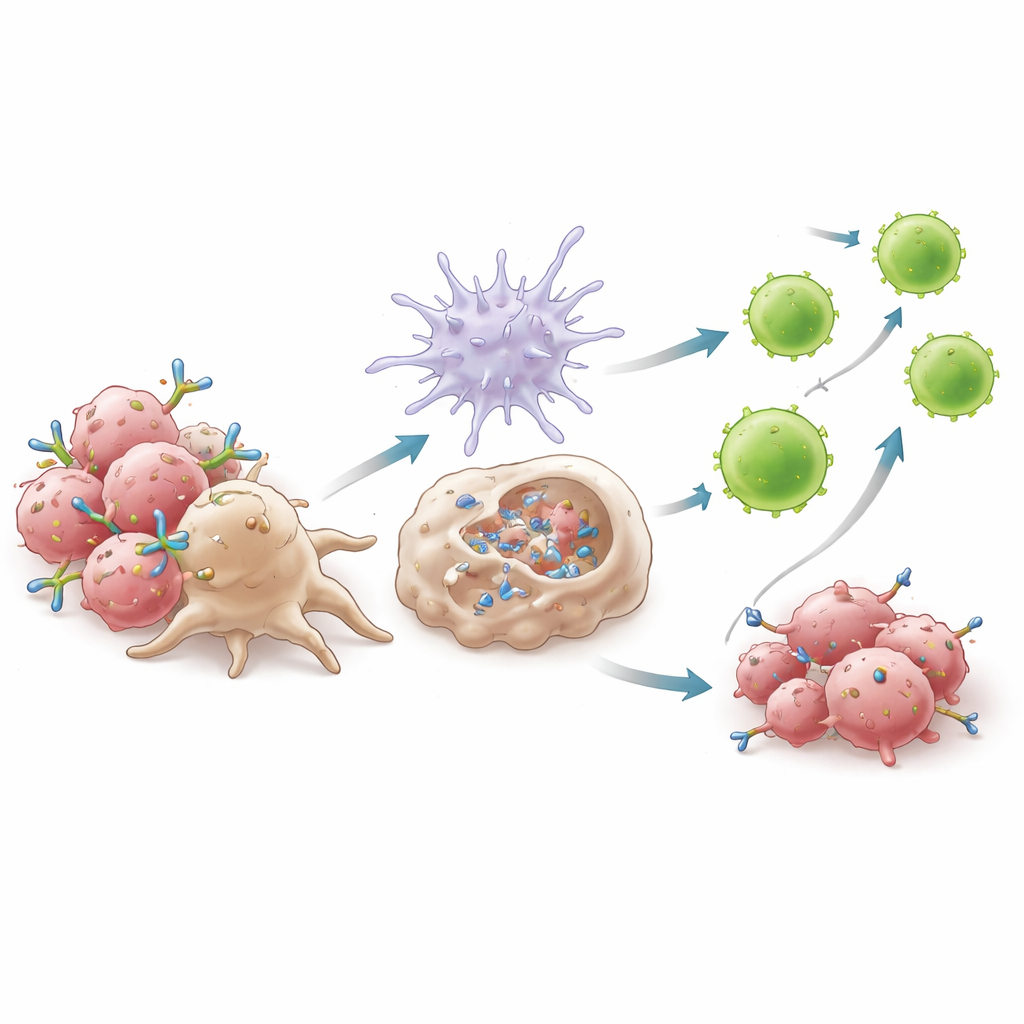
Avslöjandet av en dold broms i hjälpar-T-celler
Medan 6C5 väckte ett kraftfullt antitumörsvar avslöjade behandlingen också en oväntad form av immun själv-sabotage. Behandlingen utökade en population av CD4+ T-celler som inte bar den klassiska Treg-markören Foxp3 men som betedde sig på ett liknande hämmande sätt. Dessa celler uttryckte mycket höga nivåer av checkpoint-molekyler såsom PD-1 och CTLA-4, producerade mindre av tillväxtfaktorn IL-2 och gav mer immunosuppressiva signaler. Att avlägsna alla CD4+ T-celler förbättrade tumörkontrollen men gick miste om långsamt immuminne, vilket betonar att inte alla hjälparceller är skadliga. I stället riktade författarna in sig indirekt på denna ’Treg-liknande’ PD-1–höga undergrupp. Kombinationen av 6C5 med dubbel checkpoint-blockad (anti–PD-1 plus anti–CTLA-4) reducerade selektivt dessa hämmande celler i tumörer, samtidigt som gynnsamma T-celler bevarades och tumörkontrollen förbättrades ytterligare.
Bygga hållbart skydd med kombinationsbehandling
Där både Tregs och dessa PD-1–höga hjälparceller är glupska konsumenter av IL-2 testade teamet också ett nästa generations läkemedel som kopplar en modifierad IL-2-signal till PD-1 för att fokusera dess verkan på utmattade tumörinfiltrerande T-celler. När 6C5 kombinerades med denna PD-1–riktade IL-2-fusion rensade ungefär hälften av mössen sina tumörer helt. Anmärkningsvärt nog avvisade alla botade djur vid senare tumöråterutmaning, vilket indikerar robust och bestående immuminne. I kontrast saknade enkel borttagning av CD4+ T-celler detta varaktiga skydd. Tillsammans visar dessa resultat att justering snarare än utsläckning av CD4+-kompartmentet kan frigöra stark antikancerimmunitet utan att underminera immunsystemets förmåga att ”minnas” tumören.
Vad detta kan innebära för framtida cancerbehandling
Denna studie visar att var en antikropp binder på en tumörmolekyl kan förändra fundamentalt hur den rekryterar immunsystemet. Genom att rikta mot ett membran-nära site på AXL agerar 6C5 mindre som en signalblockerare och mer som en immunförstärkare — den driver makrofagstädning, interferonalarm, aktivering av dendritiska celler och potenta cytotoxiska T-cellsattacker. Samtidigt blottlägger arbetet nya, icke-klassiska suppressiva T-celler som uppstår under behandlingen och visar hur skräddarsydda kombinationer med checkpoint-hämmare eller IL-2–baserade medel kan neutralisera dessa bromsar. Om liknande antikroppar och strategier visar sig säkra och effektiva hos människor kan de erbjuda ett sätt att omvandla envisa, immunkalla tumörer till immunvarma som slutligen svarar på immunoterapi.
Citering: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Nyckelord: cancerimmunoterapi, tumörmikromiljö, AXL-antikropp, makrofagfagocytos, resistens mot immuncheckpoint