Clear Sky Science · pl
Reprogramowanie mikrośrodowiska guza przeciwciałem przeciwko błonowo‑bliskiemu AXL w celu pokonania oporności na blokadę punktów kontrolnych
Dlaczego niektóre guzy chowają się przed układem odpornościowym
Immunoterapia nowotworów zrewolucjonizowała leczenie wielu pacjentów, ale nadal zawodzi w dużej części guzów, które układ odpornościowy praktycznie ignoruje. Tak zwane guzy „zimne” mają niewiele napadających komórek odpornościowych i często opierają się obecnym silnym lekom blokującym punkty kontrolne. W tym badaniu badacze analizują nowy rodzaj przeciwciała, które pobudza linię obrony pierwszego rzutu wewnątrz takich guzów, pomagając przemienić zimny, cichy nowotwór w taki, który jest zapełniony komórkami odpornościowymi zabijającymi guz.
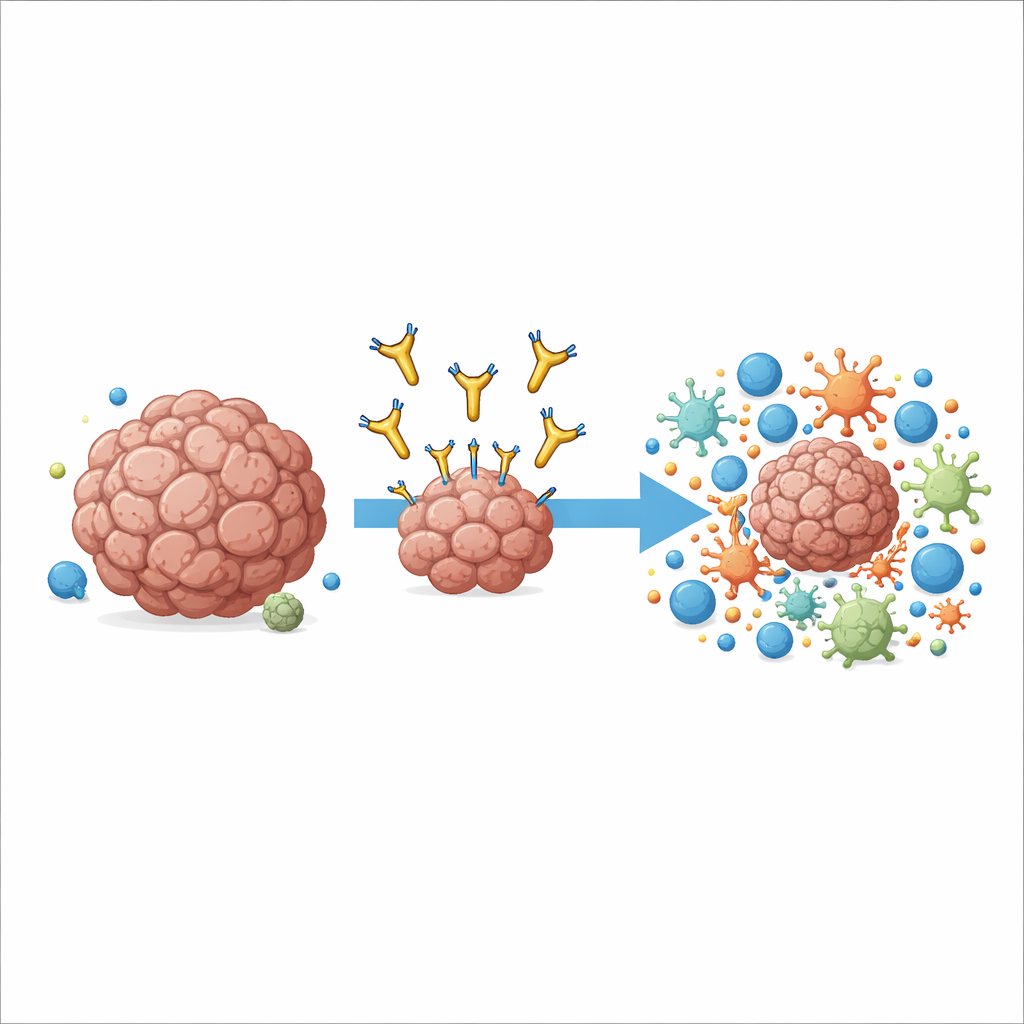
Nowy sposób celowania w dobrze znany cel nowotworowy
Praca koncentruje się na cząsteczce zwanej AXL, która znajduje się na powierzchni wielu komórek nowotworowych oraz niektórych komórek odpornościowych w guzie. Wysokie poziomy AXL wiążą się z agresywnym przebiegiem choroby, przerzutami i opornością na standardowe immunoterapie. Wcześniejsze leki próbowały zablokować sygnał wzrostowy AXL poprzez przyczepienie się do jego najbardziej zewnętrznego końca, ale w badaniach klinicznych przynosiły tylko umiarkowane korzyści i czasem powodowały działania niepożądane. Autorzy wybrali inne podejście: skonstruowali przeciwciało o nazwie 6C5, które chwyta AXL bardzo blisko błony komórkowej zamiast przy odległym końcu. Ta subtelna zmiana miejsca przyłączenia okazała się kluczowa dla tego, jak układ odpornościowy mógł wykorzystać przeciwciało jako uchwyt.
Przywoływanie „śmieciarzy” organizmu
Zamiast bezpośrednio truć komórki nowotworowe, 6C5 działa przez przyciąganie i przekierowywanie komórek odpornościowych wyspecjalizowanych w pochłanianiu i przetwarzaniu resztek, przede wszystkim makrofagów i niektórych komórek dendrytycznych. W modelach mysich czerniaka i raka okrężnicy, zmodyfikowanych tak, by ekspresowały ludzki AXL, 6C5 silnie spowalniało, a nawet zmniejszało guzy, w tym przerzuty do płuc, jednak wyłącznie gdy komórki nowotworowe prezentowały AXL. Przeciwciało miało niewielki efekt u myszy pozbawionych komórek T i B, co wskazuje, że trwała kontrola guza zależała od pełnej adaptacyjnej odpowiedzi immunologicznej. Szczegółowe analizy pojedynczych komórek w leczonych guzach ujawniły, że 6C5 dramatycznie zwiększało liczbę i aktywność makrofagów, komórek dendrytycznych oraz zabójczych komórek T infiltrujących masę guza, przekształcając ubogie immunologicznie pustkowie w zatłoczone pole walki.
Jak prowadzone przez przeciwciało sprzątanie wywołuje szerszy atak immunologiczny
Badania mechanistyczne wykazały, że sukces 6C5 zależy od sposobu, w jaki łączy makrofagi z komórkami guza. Poprzez wiązanie AXL blisko błony, 6C5 tworzy zwarte klastry, które receptory makrofagów mogą skutecznie chwycić, wzmacniając proces zwany przeciwciałozależną fagocytozą komórkową. Makrofagi chętniej połykały otoczone przeciwciałem komórki nowotworowe, gdy obecne było 6C5, ale nie wtedy, gdy zmieniono region ogonowy przeciwciała, uniemożliwiając zaangażowanie receptorów makrofagów. To pochłanianie uruchamiało produkcję interferonów typu I — silnych cząsteczek alarmowych — przez szlak zależny od białka adaptorowego MyD88. Te interferony aktywowały z kolei komórki dendrytyczne, zwiększały ich zdolność prezentacji fragmentów guza i sprzyjały migracji do węzłów chłonnych. Tam inicjowały fale cytotoksycznych komórek CD8+ T, zwłaszcza wysoce aktywnego podtypu z silnymi molekułami efektorowymi, które następnie wracały do guza, by atakować.
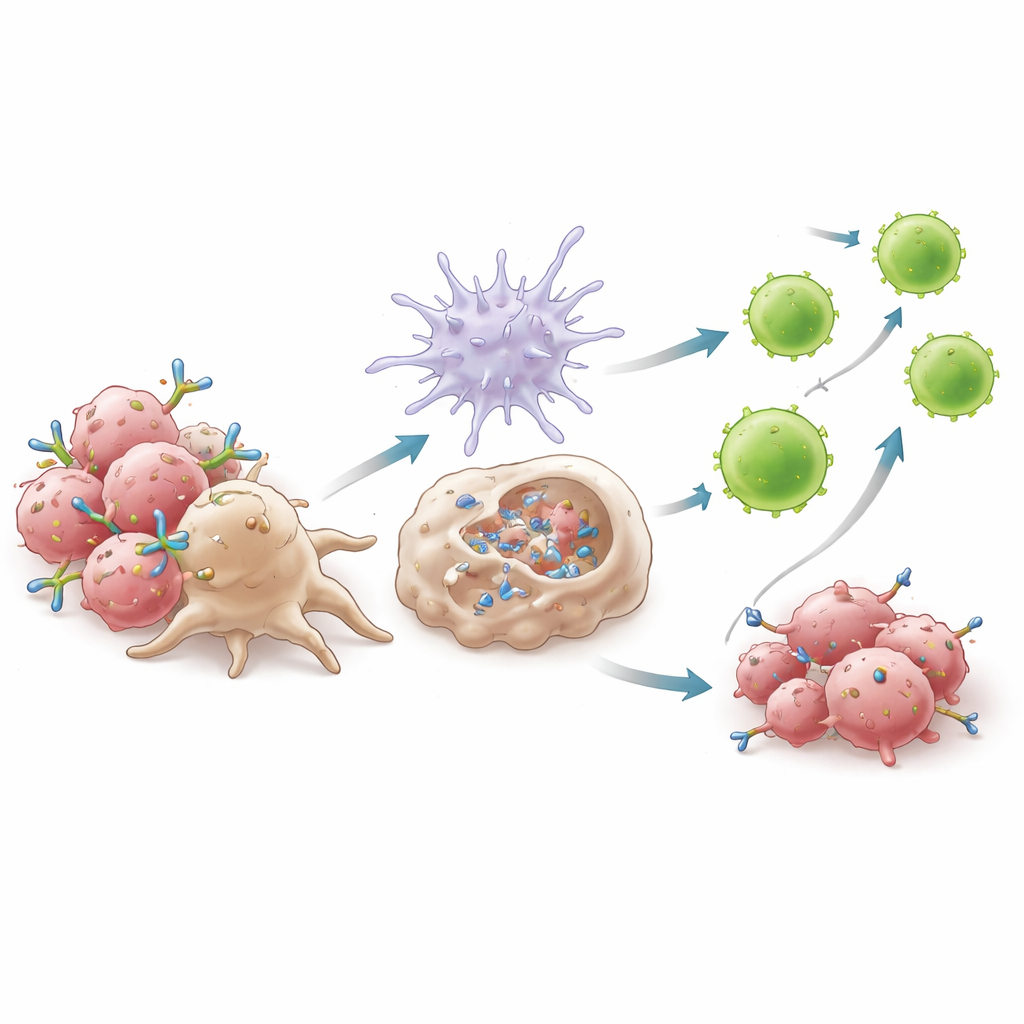
Odkrycie ukrytego hamulca w pomocniczych komórkach T
Choć 6C5 wywołało gwałtowną odpowiedź przeciwnowotworową, ujawniło też nieoczekiwaną formę auto‑sabotażu immunologicznego. Leczenie poszerzyło populację komórek CD4+ T, które nie nosiły klasycznego markera Treg Foxp3, lecz zachowywały się w sposób podobnie supresyjny. Komórki te wykazywały bardzo wysoką ekspresję cząsteczek punktów kontrolnych, takich jak PD‑1 i CTLA‑4, produkowały mniej czynnika wzrostu IL‑2 i wydzielały więcej sygnałów immunosupresyjnych. Usunięcie wszystkich komórek CD4+ T poprawiło kontrolę guza, ale kosztem długotrwałej pamięci immunologicznej, co podkreśla, że nie wszystkie komórki pomocnicze są szkodliwe. Zamiast tego autorzy celowali pośrednio w ten „Treg‑podobny” podtyp z wysokim PD‑1. Połączenie 6C5 z podwójną blokadą punktów kontrolnych (anty‑PD‑1 plus anty‑CTLA‑4) selektywnie zmniejszyło te supresyjne komórki w guzach, zachowując korzystne komórki T i jeszcze bardziej poprawiając kontrolę nowotworu.
Budowanie trwałej ochrony za pomocą terapii skojarzonej
Ponieważ zarówno Tregi, jak i te PD‑1‑wysokie komórki pomocnicze intensywnie wykorzystują IL‑2, zespół przetestował także lek następnej generacji, łączący zmodyfikowany sygnał IL‑2 z PD‑1, koncentrując jego działanie na wyczerpanych infiltrujących guz komórkach T. Gdy 6C5 połączono z tą fuzycją IL‑2 ukierunkowaną na PD‑1, około połowa myszy całkowicie oczyściła się z guzów. Co godne uwagi, wszystkie wyleczone osobniki odrzuciły późniejsze ponowne wszczepienie guza, co świadczy o odpornej i trwałej pamięci immunologicznej. W przeciwieństwie do tego, samo usunięcie komórek CD4+ T nie zapewniało tej długotrwałej ochrony. Razem wyniki te pokazują, że dostrojenie, a nie wykorzenienie, przedziału CD4+ może uwolnić silną odporność przeciwnowotworową bez osłabienia zdolności układu odpornościowego do „zapamiętania” guza.
Co to może znaczyć dla przyszłego leczenia nowotworów
To badanie pokazuje, że miejsce wiązania przeciwciała z cząsteczką guza może zasadniczo zmienić sposób, w jaki rekrutuje ono układ odpornościowy. Celując w miejsce błonowo‑bliskie na AXL, 6C5 działa mniej jak blokator sygnału, a bardziej jak wzmacniacz immunologiczny — napędzając sprzątanie przez makrofagi, alarmy interferonowe, aktywację komórek dendrytycznych i potężne ataki cytotoksycznych komórek T. Jednocześnie praca ta odsłania nowe, nieklasyczne supresorowe komórki T, które pojawiają się podczas terapii, i pokazuje, jak dopasowane kombinacje z inhibitorami punktów kontrolnych lub środkami opartymi na IL‑2 mogą zneutralizować te hamulce. Jeśli podobne przeciwciała i strategie okażą się bezpieczne i skuteczne u ludzi, mogą dać sposób na przekształcenie opornych, immunologicznie „zimnych” guzów w „gorące”, które wreszcie zareagują na immunoterapię.
Cytowanie: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Słowa kluczowe: immunoterapia nowotworów, mikrośrodowisko guza, przeciwciało przeciw AXL, fagocytoza przez makrofagi</keyword:f> <keyword>oporność na blokadę punktów kontrolnych