Clear Sky Science · tr
Tümör mikroçevresini, membrana yakın AXL’e karşı antikorla yeniden programlayarak immün kontrol noktası blokajı direncini aşmak
Bazı tümörlerin immün sistemden neden saklandığı
Kanser immünoterapisi birçok hasta için tedaviyi dönüştürdü, ancak immün sistemin neredeyse hiç fark etmediği geniş bir tümör kesiminde hâlâ başarısız oluyor. Bu so-called “soğuk” tümörler az sayıda saldırgan immün hücre içerir ve sıklıkla günümüzün güçlü kontrol noktası ilaçlarına direnç gösterir. Bu çalışma, böyle tümörlerin içine vücudun birinci savunma hattını uyandıran yeni bir antikor türünü araştırıyor; bu antikor soğuk, sessiz bir kanseri tümör öldürücü immün hücrelerle dolup taşan bir hâle dönüştürmeye yardımcı oluyor.
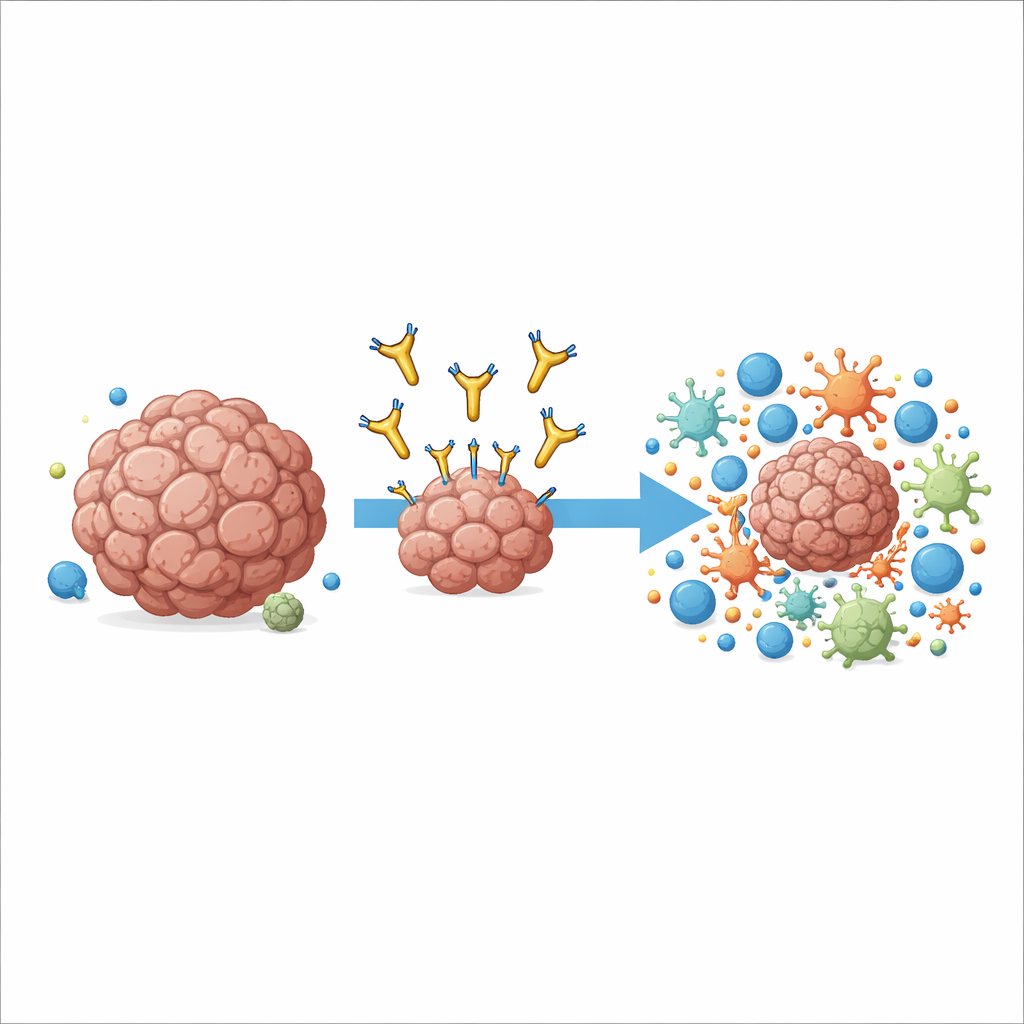
Aşina olunan bir kanser hedefini hedeflemenin yeni bir yolu
Çalışma, birçok kanser hücresinin yüzeyinde ve tümörde bazı immün hücrelerde bulunan AXL adlı bir molekül etrafında yoğunlaşıyor. Yüksek AXL düzeyleri agresif hastalık, uzak organlara yayılım ve standart immünoterapilere dirençle ilişkilidir. Önceki ilaçlar AXL’in büyüme sinyalini, dıştaki en uç noktaya tutunarak bloke etmeye çalıştı, ancak klinik deneylerde sadece sınırlı fayda gösterdiler ve bazen yan etkilere neden oldular. Yazarlar farklı bir yol izlediler: AXL’i hücre zarına çok yakın bir noktadan yakalayan 6C5 adlı bir antikor geliştirdiler; uzak uçtan değil. Bağlanma konumundaki bu ince kayma, antikoru immün sistemin kullanabileceği bir tutamaç haline getirme konusunda belirleyici oldu.
Vücudun çöp toplayıcılarını işe almak
6C5 doğrudan kanser hücrelerini zehirlemek yerine, özellikle makrofajlar ve belirli dendritik hücreler gibi enkazı yutup işleme uzmanı immün hücreleri çağırıp yönlendirerek çalışır. İnsan AXL’i taşıyacak şekilde mühendislik yapılan melanom ve kolon kanseri fare modellerinde 6C5 tümörleri, hatta akciğer metastazlarını güçlü biçimde yavaşlattı veya küçülttü; ancak bu etki yalnızca tümör hücreleri AXL sergilediğinde görüldü. Antikor, T ve B hücrelerinden yoksun farelerde fazla etki göstermedi; bu da kalıcı tümör kontrolünün eksiksiz bir adaptif immün yanıta bağlı olduğunu gösterdi. Tedavi edilen tümörlerin ayrıntılı tek hücre analizleri, 6C5’in makrofaj, dendritik hücre ve öldürücü T hücrelerinin sayısını ve aktivitesini dramatik biçimde artırdığını ortaya koydu; böylece seyrek bir immün çöl, kalabalık bir savaş alanına dönüştü.
Antikor yönlendirmeli temizlik nasıl daha geniş immün saldırıyı tetikler
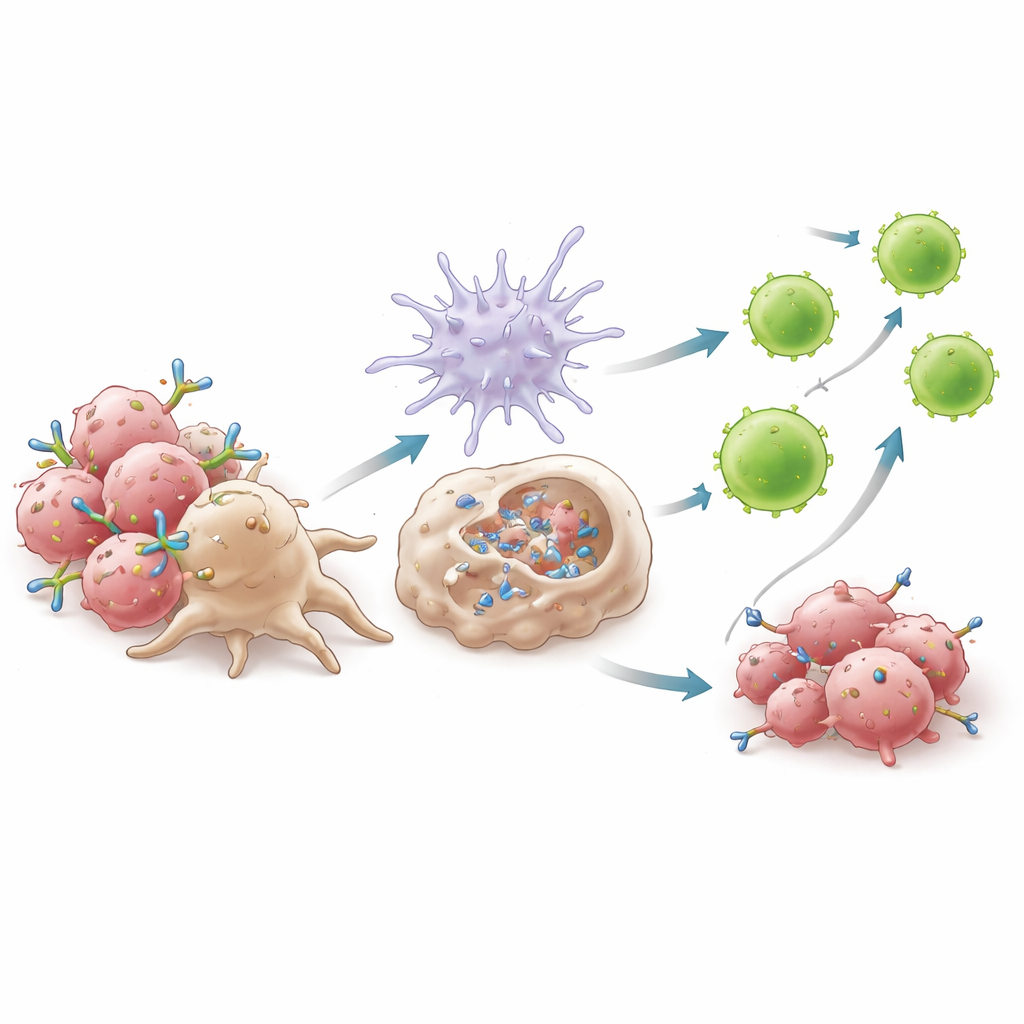
Mekanik deneyler, 6C5’in başarısının makrofajları tümör hücrelerine nasıl bağladığına dayandığını gösterdi. 6C5, AXL’e membrana yakın bağlanarak makrofaj reseptörlerinin etkin biçimde kavrayabileceği kompakt kümeleşmeler oluşturuyor ve antikora bağımlı hücresel fagositoz adı verilen süreci güçlendiriyordu. Makrofajlar, 6C5 varlığında antikorla kaplı tümör hücrelerini daha kolay yuttu; ancak antikorun kuyruk bölgesi makrofaj reseptörleriyle etkileşimi engelleyecek şekilde değiştirildiğinde bu gerçekleşmedi. Bu yutma olayı, adaptör proteini MyD88’e bağımlı bir yol aracılığıyla güçlü alarm molekülleri olan tip I interferonların üretimini tetikledi. Bu interferonlar dendritik hücreleri aktive etti, onların tümör parçalarını sunma yeteneğini artırdı ve lenf düğümlerine göçlerini teşvik etti. Orada, sitotoksik CD8+ T hücrelerinin dalgalarını hazırladılar; özellikle güçlü efektör moleküllerle işaretlenmiş yüksek etkinliğe sahip bir alt grup, daha sonra tümöre geri dönüp saldırdı.
Yardımcı T hücrelerinde gizli bir freni açığa çıkarmak
6C5 güçlü bir antitümör yanıtı uyandırırken, aynı zamanda beklenmedik bir immün öz-kötüleme biçimini de ortaya çıkardı. Tedavi, klasik Treg belirteci Foxp3 taşımayan ancak benzer şekilde baskılayıcı davranan bir CD4+ T hücresi popülasyonunu genişletti. Bu hücreler PD-1 ve CTLA-4 gibi kontrol noktası moleküllerini çok yüksek düzeyde ifade etti, büyüme faktörü IL-2 üretimini azalttı ve daha fazla immünsüpresif sinyal üretti. Tüm CD4+ T hücrelerinin bertaraf edilmesi tümör kontrolünü artırdı fakat uzun vadeli immün belleği feda etti; bu da her yardımcı hücrenin zararlı olmadığını vurguluyor. Bunun yerine yazarlar bu “Treg-benzeri” PD-1–yüksek alt kümeye dolaylı yoldan hedeflendiler. 6C5’i çift kontrol noktası blokajı (anti–PD-1 artı anti–CTLA-4) ile birleştirmek, tümörlerde bu baskılayıcı hücreleri seçici olarak azalttı; yararlı T hücrelerini koruyarak tümör kontrolünü daha da iyileştirdi.
Kombinasyon tedavisiyle kalıcı koruma inşa etmek
Treg’ler ve bu PD-1–yüksek yardımcı hücreler IL-2 tüketicileri olduğundan, ekip ayrıca modifiye edilmiş bir IL-2 sinyalini PD-1’e bağlayarak eylemini tükenmiş tümör infiltre eden T hücrelerine odaklayan yeni nesil bir ilacı test etti. 6C5 bu PD-1 hedefli IL-2 füzyonuyla eşleştirildiğinde, farelerin yaklaşık yarısı tümörlerini tamamen temizledi. İyileşen tüm hayvanlar daha sonra yapılan tümör yeniden meydan okumasını reddetti; bu da sağlam ve kalıcı immün bellek gösteriyordu. Buna karşılık, basitçe CD4+ T hücrelerini ortadan kaldırmak bu dayanıklı korumayı sağlamadı. Birlikte bu sonuçlar, CD4+ bölmesini silmek yerine ince ayar yapmanın immün sistemin tümörü “hatırlama” yeteneğini zedelemeden güçlü antikanser bağışıklığı açığa çıkarabileceğini gösteriyor.
Geleceğin kanser tedavisi için olası çıkarımlar
Bu çalışma, bir antikorun tümör molekülü üzerinde nereden bağlandığının, onu immün sistemi nasıl devreye soktuğunu kökten değiştirebileceğini gösteriyor. AXL’in membrana yakın bir bölgesini hedefleyerek 6C5, bir sinyal engelleyiciden çok bir immün yükseltici gibi davranıyor—makrofaj temizliğini, interferon alarmlarını, dendritik hücre aktivasyonunu ve güçlü öldürücü T hücresi saldırılarını besliyor. Aynı zamanda çalışma, tedavi sırasında ortaya çıkan yeni, klasik olmayan baskılayıcı T hücreleri ifşa ediyor ve kontrol noktası inhibitörleri veya IL-2 bazlı ajanlarla uyarlanmış kombinasyonların bu frenleri nasıl nötralize edebileceğini gösteriyor. Benzer antikorlar ve stratejiler insanlarda güvenli ve etkili olduğunu kanıtlayabilirse, inatçı immün-soğuk tümörleri immün-sıcak hâle getirerek immünoterapilere yanıt verebilir hâle getirme yolunu açabilirler.
Atıf: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Anahtar kelimeler: kanser immünoterapisi, tümör mikroçevresi, AXL antikoru, makrofaj fagositozu, immün kontrol noktası direnci