Clear Sky Science · ar
إعادة برمجة البيئة المجهرية للورم بواسطة جسم مضاد ضد AXL القريب من الغشاء لتجاوز مقاومة حجب نقاط التفتيش المناعية
لماذا تختبئ بعض الأورام من الجهاز المناعي
غيّر العلاج المناعي للسرطان مسار علاج كثير من المرضى، لكنه لا يزال يفشل في نسبة كبيرة من الأورام التي يكاد الجهاز المناعي يتجاهلها. تحتوي هذه الأورام «الباردة» على عدد ضئيل من الخلايا المناعية المهاجمة وغالبًا ما تقاوم أدوية نقاط التفتيش القوية الحالية. تستكشف هذه الدراسة نوعًا جديدًا من الأجسام المضادة يوقظ خطوط الدفاع الأولى في داخل مثل هذه الأورام، ويساعد على تحويل السرطان البارد الصامت إلى ورم يعجّ بخلايا مناعية قاتلة للأورام.
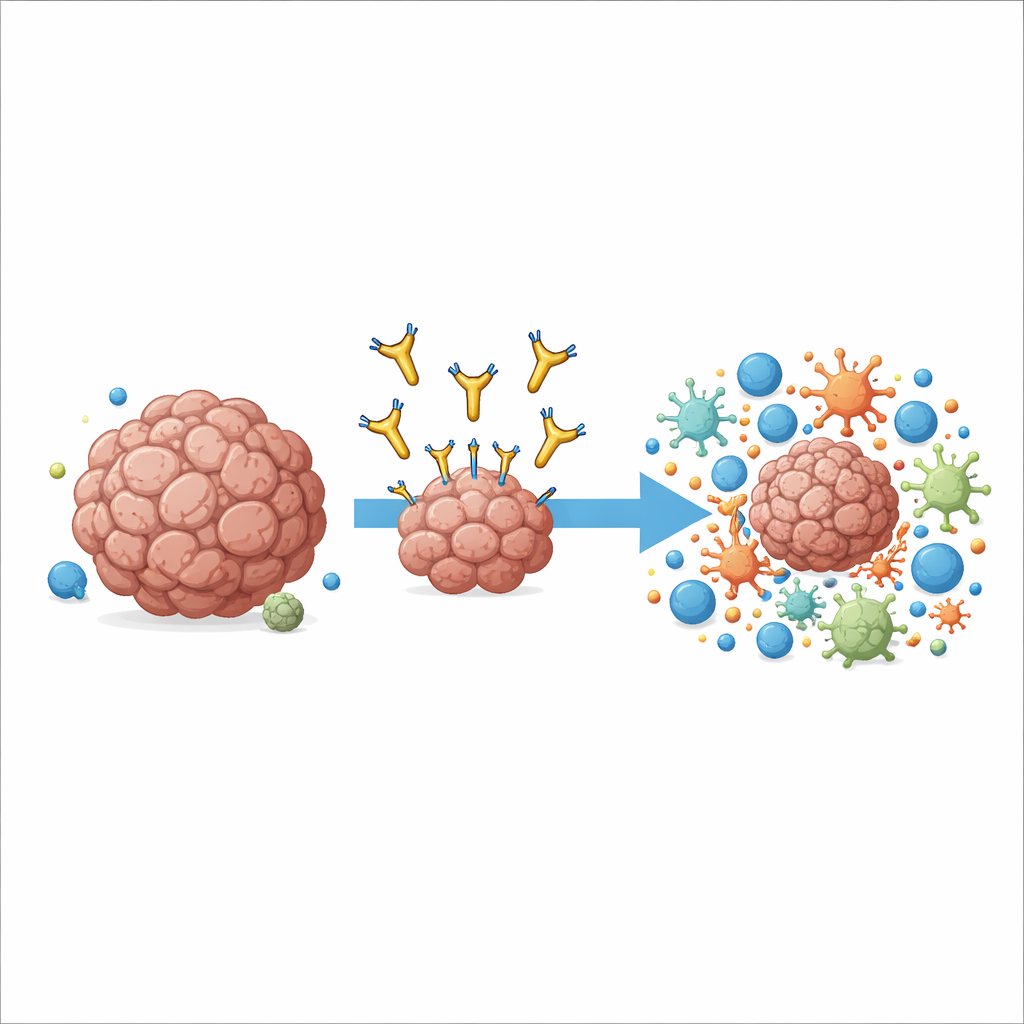
طريقة جديدة لاستهداف هدف سرطاني مألوف
تركز العمل على جزيء يسمى AXL، الموجود على سطح العديد من الخلايا السرطانية وببعض الخلايا المناعية داخل الورم. يرتبط ارتفاع مستوى AXL بمرض عدواني، وانتشار إلى أعضاء أخرى، ومقاومة للعلاجات المناعية القياسية. حاولت أدوية سابقة حجب إشارة النمو الخاصة بـAXL عبر الالتصاق بالطرف الخارجي البعيد منه، لكنها أظهرت فوائد متواضعة في التجارب الإكلينيكية وأحيانًا سببت آثارًا جانبية. اتخذ المؤلفون نهجًا مختلفًا: صمموا جسمًا مضادًا باسم 6C5 يلتقط AXL بالقرب من غشاء الخلية بدلًا من الطرف البعيد. هذا التغيير الدقيق في مكان الالتحام تبين أنه حاسم لكيفية استخدام الجهاز المناعي للجسم المضاد كمقبض.
استدعاء جامعي القمامة في الجسم
بدلًا من تسميم الخلايا السرطانية مباشرة، يعمل 6C5 عن طريق استدعاء وإعادة توجيه الخلايا المناعية المتخصصة في ابتلاع ومعالجة الحطام، لا سيما البالعات وبعض الخلايا المتغصنة. في نماذج فئران للملانوما وسرطان القولون معدّلة لحمل AXL البشري، أبطأ 6C5 الأورام بقوة أو حتى قلّصها، بما في ذلك نقائل الرئة، لكنه كان فعالًا فقط عندما كانت خلايا الورم تعرض AXL. كان للجسم المضاد تأثير ضئيل في الفئران الخالية من الخلايا التائية والبائية، مما يبيّن أن السيطرة الدائمة على الورم اعتمدت على استجابة مناعية تكيّفية كاملة. كشفت تحليلات خلوية مفردة مفصلة للأورام المعالجة أن 6C5 زاد بدرجة كبيرة عدد ونشاط البالعات، والخلايا المتغصنة، والخلايا التائية القاتلة التي اخترقت كتلة السرطان، محولًا صحراء مناعية شحيحة إلى ساحة معركة مكتظة.
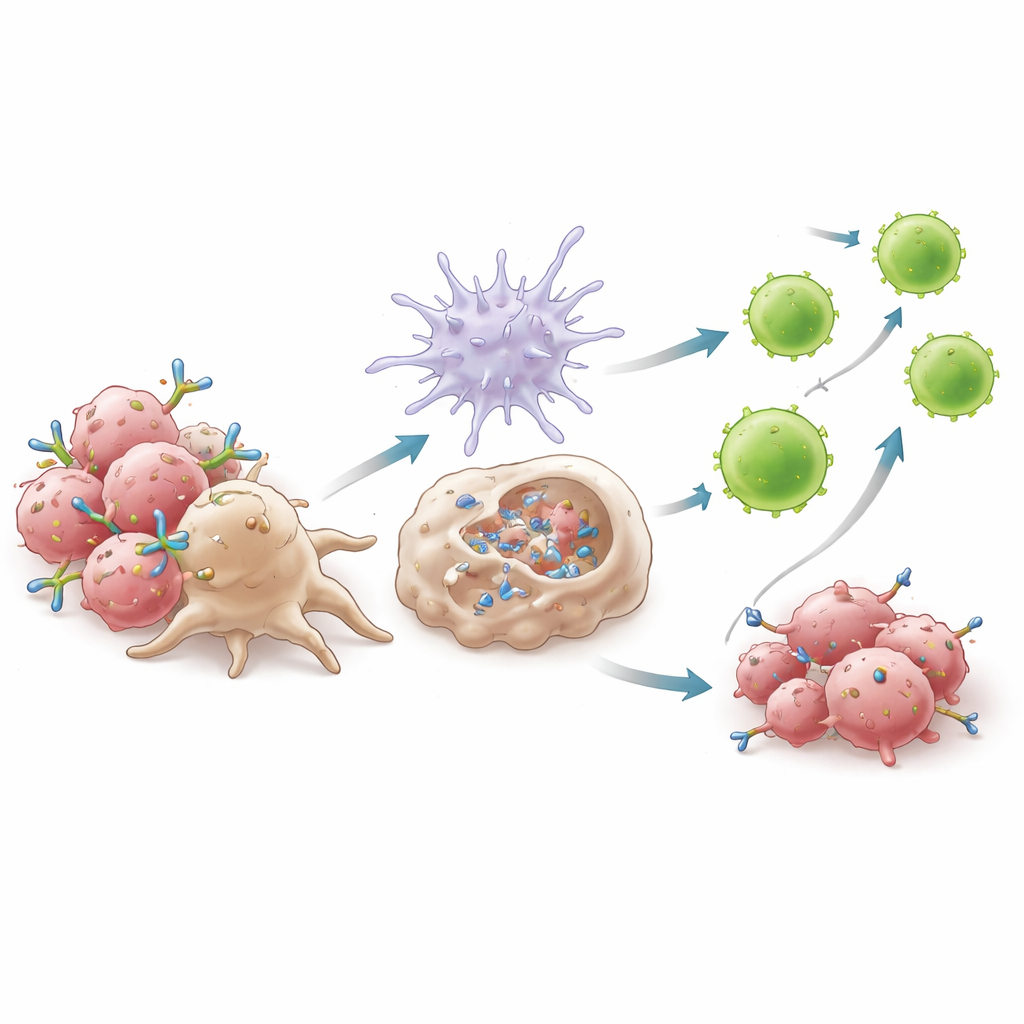
كيف تُشعل عملية التنظيف الموجّهة بالأجسام المضادة هجومًا مناعيًا أوسع
أظهرت تجارب آلية أن نجاح 6C5 يعتمد على كيف يربط البالعات بخلايا الورم. عبر الارتباط بـAXL قرب الغشاء، يشكل 6C5 عناقيد مدمجة تستطيع مستقبلات البالعات الإمساك بها بكفاءة، مما يعزز عملية تسمى البلع الخلوي المعتمدة على الأجسام المضادة. كانت البالعات تبتلع الخلايا المغطاة بالأجسام المضادة بسهولة أكبر بوجود 6C5، لكن ليس عندما غُيِّر جزء ذي الذيل للجسم المضاد لمنع تفاعل مستقبلات البالعات. أدى هذا الابتلاع إلى إنتاج الإنترفيرونات من النوع الأول — جزيئات إنذار قوية — عبر مسار اعتمد على بروتين الربط MyD88. هذه الإنترفيرونات بدورها فعّلت الخلايا المتغصنة، وزادت من قدرتها على عرض شظايا الورم، وشجعت هجرتها إلى العقد اللمفاوية. هناك، هيّأت موجات من الخلايا التائية السامة CD8+، ولا سيما فئة عالية النشاط موسومة بجزيئات فعالة قوية، والتي عادت بعد ذلك إلى الورم للهجوم.
كشف فرامل مخفية داخل الخلايا التائية المساعدة
بينما حفّز 6C5 استجابة مضادة للورم قوية، كشف أيضًا عن شكل غير متوقع من التخريب الذاتي المناعي. وسّع العلاج مجموعة من الخلايا التائية CD4+ التي لم تحمل العلامة التقليدية للخلايا التنظيمية Treg المعروفة باسم Foxp3 لكنها تصرفت بطريقة مثبطة مشابهة. عبّرت هذه الخلايا عن مستويات مرتفعة للغاية من جزيئات نقاط التفتيش مثل PD-1 وCTLA-4، أنتجت كمية أقل من عامل النمو IL-2، وأصدرت إشارات أكثر قمعية مناعيًا. عزّل كل الخلايا CD4+ حسن السيطرة على الورم لكنه ضحي بالذاكرة المناعية طويلة الأمد، مما يؤكد أن ليس كل خلايا المساعدة ضارة. بدلًا من ذلك، استهدف المؤلفون هذه الفئة الشبيهة بـTreg عالية التعبير عن PD-1 بشكل غير مباشر. قلل الجمع بين 6C5 وحجب نقاط تفتيش مزدوج (مضاد PD-1 بالإضافة إلى مضاد CTLA-4) هذه الخلايا الكابحة في الأورام بشكل انتقائي، مع الحفاظ على الخلايا التائية المفيدة وتحسين السيطرة على الورم.
بناء حماية دائمة عبر العلاج التوافقي
نظرًا لأن كلًا من الخلايا التنظيمية وتلك الخلايا المساعدة عالية التعبير عن PD-1 تتغذي على IL-2، اختبر الفريق أيضًا دواءً من الجيل التالي يربط إشارة IL-2 معدّلة بـPD-1، مركزًا عمله على الخلايا التائية المنهكة النافذة للورم. عندما تم إقران 6C5 بهذا الاندماج المستهدف لـPD-1 وIL-2، تخلص نحو نصف الفئران تمامًا من أورامها. والأهم أن كل الحيوانات المُشفاة رفضت تحديًا ورميًا لاحقًا، مما يشير إلى ذاكرة مناعية قوية ودائمة. بالمقابل، لم يمنح الاستئصال البسيط للخلايا CD4+ هذه الحماية الدائمة. توضح هذه النتائج معًا أن ضبط قسم CD4+ بدل محوه يمكن أن يطلق مناعة مضادة للسرطان قوية دون تقويض قدرة الجهاز المناعي على «تذكر» الورم.
ما الذي قد يعنيه هذا لعلاج السرطان في المستقبل
تُظهر هذه الدراسة أن موضع ارتباط الجسم المضاد بجزيء الورم يمكن أن يغيّر جذريًا كيف يستقطب الجهاز المناعي. باستهداف موقع قريب من الغشاء على AXL، يعمل 6C5 أقل كمُعكِس إشارة وأكثر كمُعزّز مناعي — يغذي تنظيف البالعات، وصفارات الإنترفيرون، وتنشيط الخلايا المتغصنة، وهجمات قوية للخلايا التائية القاتلة. في الوقت نفسه، يكشف العمل عن خلايا تائية كابحة غير نمطية تظهر أثناء العلاج ويبيّن كيف يمكن للمجموعات المصممة بعناية مع مثبطات نقاط التفتيش أو عوامل قائمة على IL-2 أن تعطل هذه الفرامل. إذا برهنت أجسام مضادة واستراتيجيات مماثلة على أمانها وفعاليتها في البشر، فقد توفر طريقة لتحويل الأورام العنيدة الباردة مناعيًا إلى أورام ساخنة مناعيًا تستجيب أخيرًا للعلاج المناعي.
الاستشهاد: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
الكلمات المفتاحية: العلاج المناعي للسرطان, البيئة المجهرية للورم, جسم مضاد ضد AXL, البلعمة بواسطة البالعات, مقاومة نقاط التفتيش المناعية