Clear Sky Science · de
Umprogrammierung des Tumormikromilieus mit einem Antikörper gegen membrannahes AXL zur Überwindung der Resistenz gegen Immun-Checkpoint-Blockaden
Warum einige Tumoren sich dem Immunsystem entziehen
Die Krebsimmuntherapie hat die Behandlung vieler Patienten revolutioniert, versagt aber nach wie vor bei einem großen Teil der Tumoren, die das Immunsystem kaum wahrnimmt. Diese sogenannten „kalten" Tumoren enthalten wenige angreifende Immunzellen und sind oft gegen die heute starken Checkpoint-Medikamente resistent. Die vorliegende Studie untersucht eine neue Art von Antikörper, die die erste Verteidigungslinie des Körpers innerhalb solcher Tumoren weckt und so dazu beiträgt, einen kalten, stillen Tumor in einen umzuwandeln, der von tumorvernichtenden Immunzellen wimmelt.
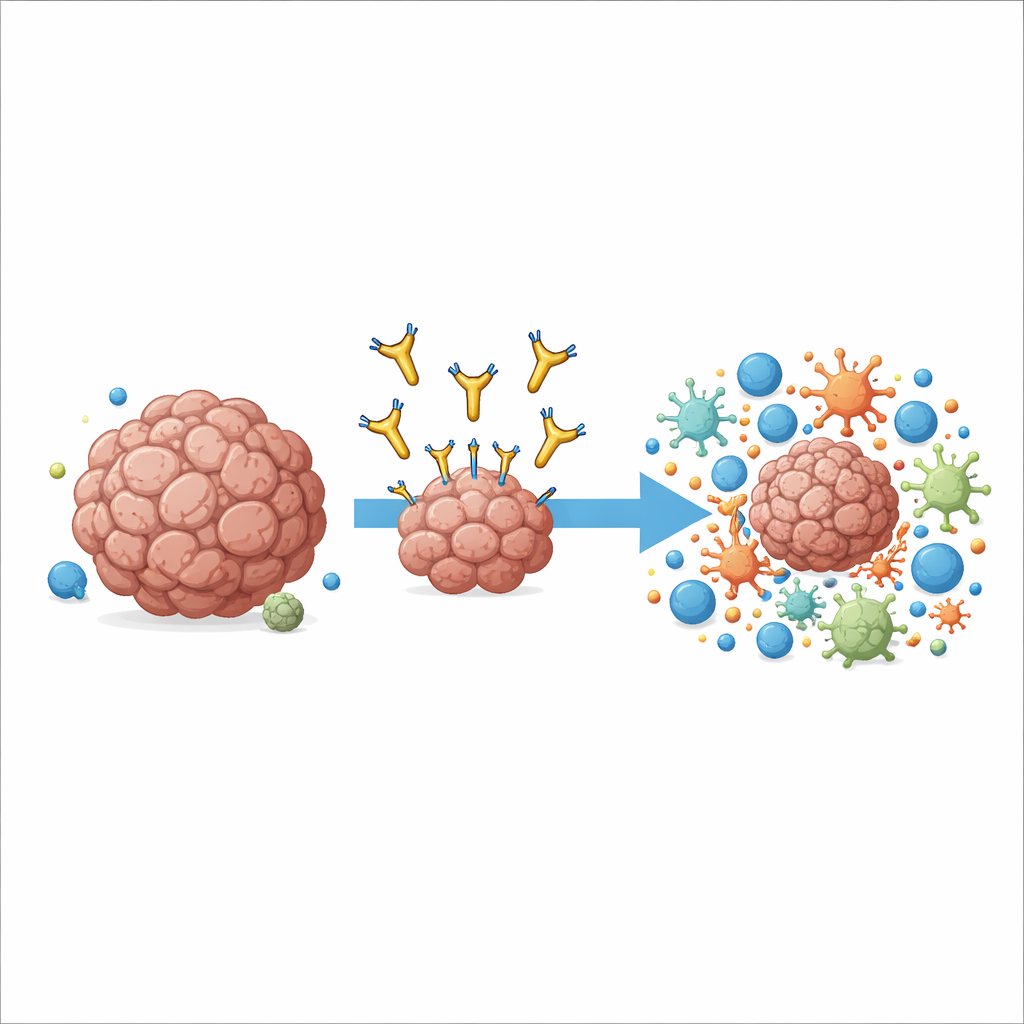
Ein neuer Weg, ein bekanntes Krebsziel anzuvisieren
Im Mittelpunkt der Arbeit steht ein Molekül namens AXL, das auf der Oberfläche vieler Krebszellen und einiger Immunzellen im Tumor sitzt. Hohe AXL-Level korrelieren mit aggressivem Krankheitsverlauf, Metastasenbildung und Resistenz gegenüber etablierten Immuntherapien. Frühere Wirkstoffe versuchten, AXLs Wachstumssignal zu blockieren, indem sie an seiner äußersten Spitze ansetzten, zeigten in klinischen Studien jedoch nur mäßige Vorteile und verursachten mitunter Nebenwirkungen. Die Autoren verfolgten einen anderen Ansatz: Sie entwickelten einen Antikörper namens 6C5, der AXL sehr nah an der Zellmembran statt an der entfernten Spitze ergreift. Dieser feine Unterschied in der Andockposition erwies sich als entscheidend dafür, wie das Immunsystem den Antikörper als Griff nutzen konnte.
Die Müllabfuhr des Körpers herbeirufen
Statt Krebszellen direkt zu vergiften, wirkt 6C5, indem es Immunzellen herbeiruft und umlenkt, die auf das Verschlingen und Verarbeiten von Zelltrümmern spezialisiert sind, insbesondere Makrophagen und bestimmte dendritische Zellen. In Mausmodellen von Melanom und Darmkrebs, die humanes AXL tragen, verlangsamte oder verkleinerte 6C5 Tumoren nachdrücklich, einschließlich Lungenmetastasen — allerdings nur, wenn Tumorzellen AXL zeigten. Der Antikörper hatte wenig Wirkung in Mäusen ohne T- und B-Zellen, was zeigt, dass eine anhaltende Tumorkontrolle eine vollständige adaptive Immunantwort benötigte. Detaillierte Einzelzellanalysen behandelter Tumoren zeigten, dass 6C5 die Zahl und Aktivität von Makrophagen, dendritischen Zellen und zytotoxischen T-Zellen im Tumor massiv erhöhte und so eine spärliche Immunwüste in ein dicht bevölkertes Schlachtfeld verwandelte.
Wie antikörpergeführtes Aufräumen eine breitere Immunattacke auslöst
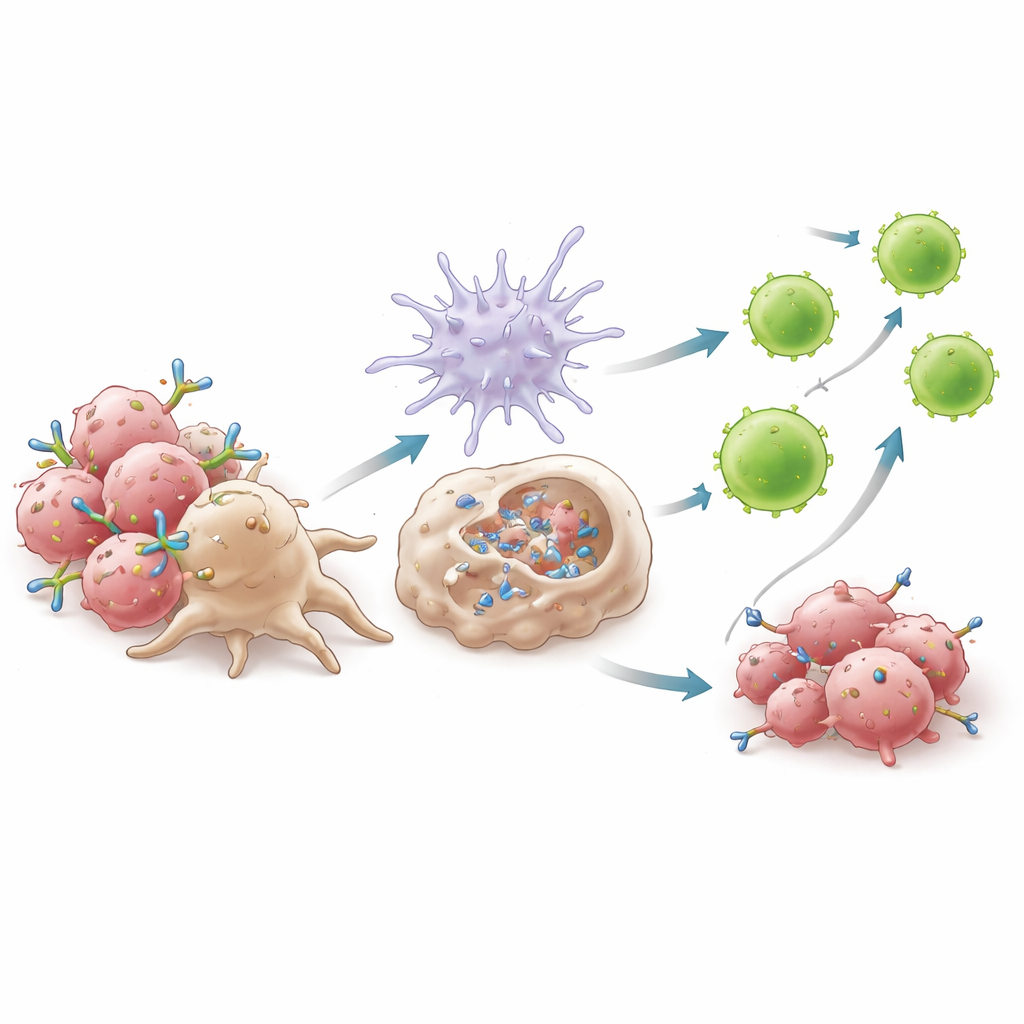
Mechanistische Experimente zeigten, dass der Erfolg von 6C5 davon abhängt, wie es Makrophagen an Tumorzellen bindet. Durch die Bindung an AXL nahe der Membran bildet 6C5 kompakte Cluster, die Makrophagenrezeptoren effizient greifen können, wodurch ein Prozess namens antikörperabhängige zelluläre Phagozytose verstärkt wird. Makrophagen verschlangen antikörperbeschichtete Tumorzellen deutlich leichter, wenn 6C5 vorhanden war — nicht jedoch, wenn dessen Fc-Region so verändert wurde, dass eine Interaktion mit Makrophagenrezeptoren verhindert war. Diese Aufnahme löste die Produktion von Typ-I-Interferonen aus — starke Alarmmoleküle — über einen Weg, der auf dem Adapterprotein MyD88 beruhte. Diese Interferone aktivierten wiederum dendritische Zellen, steigerten ihre Fähigkeit, Tumorfragmente zu präsentieren, und förderten ihre Wanderung zu den Lymphknoten. Dort bereiteten sie Wellen zytotoxischer CD8+-T-Zellen vor, insbesondere eine hochaktive Untergruppe mit starken Effektormolekülen, die dann zurück in den Tumor strömten, um anzugreifen.
Eine versteckte Bremse in Helfer-T-Zellen enttarnen
Obwohl 6C5 eine kräftige Anti-Tumor-Antwort auslöste, legte es auch eine unerwartete Form der Immun-Selbstsabotage offen. Die Behandlung vergrößerte eine Population von CD4+-T-Zellen, die nicht das klassische Treg-Markerprotein Foxp3 trug, sich aber ähnlich unterdrückend verhielt. Diese Zellen exprimierten sehr hohe Mengen an Checkpoint-Molekülen wie PD-1 und CTLA-4, produzierten weniger des Wachstumsfaktors IL-2 und gaben mehr immunsuppressive Signale ab. Die Depletion aller CD4+-T-Zellen verbesserte die Tumorkontrolle, opferte jedoch die langfristige immunologische Erinnerung, was verdeutlicht, dass nicht alle Helferzellen schädlich sind. Die Autoren zielten stattdessen indirekt auf diese „Treg-ähnliche" PD-1-hohe Untergruppe ab. Die Kombination von 6C5 mit dualer Checkpoint-Blockade (anti–PD-1 plus anti–CTLA-4) verringerte diese suppressiven Zellen selektiv in den Tumoren, während nützliche T-Zellen erhalten blieben und die Tumorkontrolle weiter verbessert wurde.
Beständige Schutzwirkung durch Kombinationstherapie aufbauen
Da sowohl regulatorische T-Zellen als auch diese PD-1-hohen Helferzellen intensive Verbraucher von IL-2 sind, testete das Team außerdem ein Next‑Generation‑Präparat, das ein modifiziertes IL-2-Signal an PD-1 koppelt und seine Wirkung auf erschöpfte, tumorinfiltrierende T‑Zellen fokussiert. Als 6C5 mit dieser PD-1‑gerichteten IL-2-Fusion kombiniert wurde, beseitigten etwa die Hälfte der Mäuse ihre Tumoren vollständig. Bemerkenswerterweise wiesen alle geheilten Tiere bei einer späteren Tumorneuinfektion eine Abwehr auf, was auf eine robuste und langanhaltende immunologische Erinnerung hindeutet. Im Gegensatz dazu bot die bloße Entfernung von CD4+-T-Zellen keinen solchen dauerhaften Schutz. Zusammen zeigen diese Ergebnisse, dass das Feinjustieren statt vollständige Auslöschen des CD4+-Kompartiments eine starke Anti-Tumor-Immunität freisetzen kann, ohne die Fähigkeit des Immunsystems zu untergraben, sich an den Tumor zu „erinnern".
Was das für die künftige Krebstherapie bedeuten könnte
Die Studie demonstriert, dass der Bindungsort eines Antikörpers an einem Tumormolekül grundlegend verändern kann, wie er das Immunsystem rekrutiert. Durch das Anvisieren einer membrannahen Stelle von AXL wirkt 6C5 weniger wie ein Signalblocker und mehr wie ein Immunverstärker — es fördert Makrophagenaufräumen, Interferon‑Alarmsignale, Aktivierung dendritischer Zellen und starke Angriffe zytotoxischer T‑Zellen. Gleichzeitig deckt die Arbeit neue, nicht‑klassische suppressive T‑Zellen auf, die während der Therapie entstehen, und zeigt, wie maßgeschneiderte Kombinationen mit Checkpoint‑Inhibitoren oder IL‑2‑basierten Wirkstoffen diese Bremsen neutralisieren können. Falls ähnliche Antikörper und Strategien beim Menschen sicher und wirksam sind, könnten sie einen Weg bieten, hartnäckig immun‑kalte Tumoren in immun‑heiße Tumoren zu verwandeln, die schließlich auf Immuntherapien ansprechen.
Zitation: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Schlüsselwörter: Krebsimmuntherapie, Tumormikromilieu, AXL-Antikörper, Phagozytose durch Makrophagen, Resistenz gegen Immun-Checkpoints