Clear Sky Science · es
Reprogramar el microambiente tumoral con un anticuerpo contra AXL cercano a la membrana para superar la resistencia al bloqueo de puntos de control inmunitario
Por qué algunos tumores se ocultan al sistema inmunitario
La inmunoterapia contra el cáncer ha transformado el tratamiento de muchos pacientes, pero aún falla en una gran proporción de tumores que el sistema inmunitario prácticamente no detecta. Estos llamados tumores “fríos” contienen pocas células inmunitarias atacantes y con frecuencia resisten los potentes fármacos de bloqueo de puntos de control actuales. Este estudio explora un nuevo tipo de anticuerpo que despierta las defensas de primera línea del organismo dentro de esos tumores, ayudando a convertir un cáncer frío y silencioso en uno repleto de células inmunitarias que matan tumores.
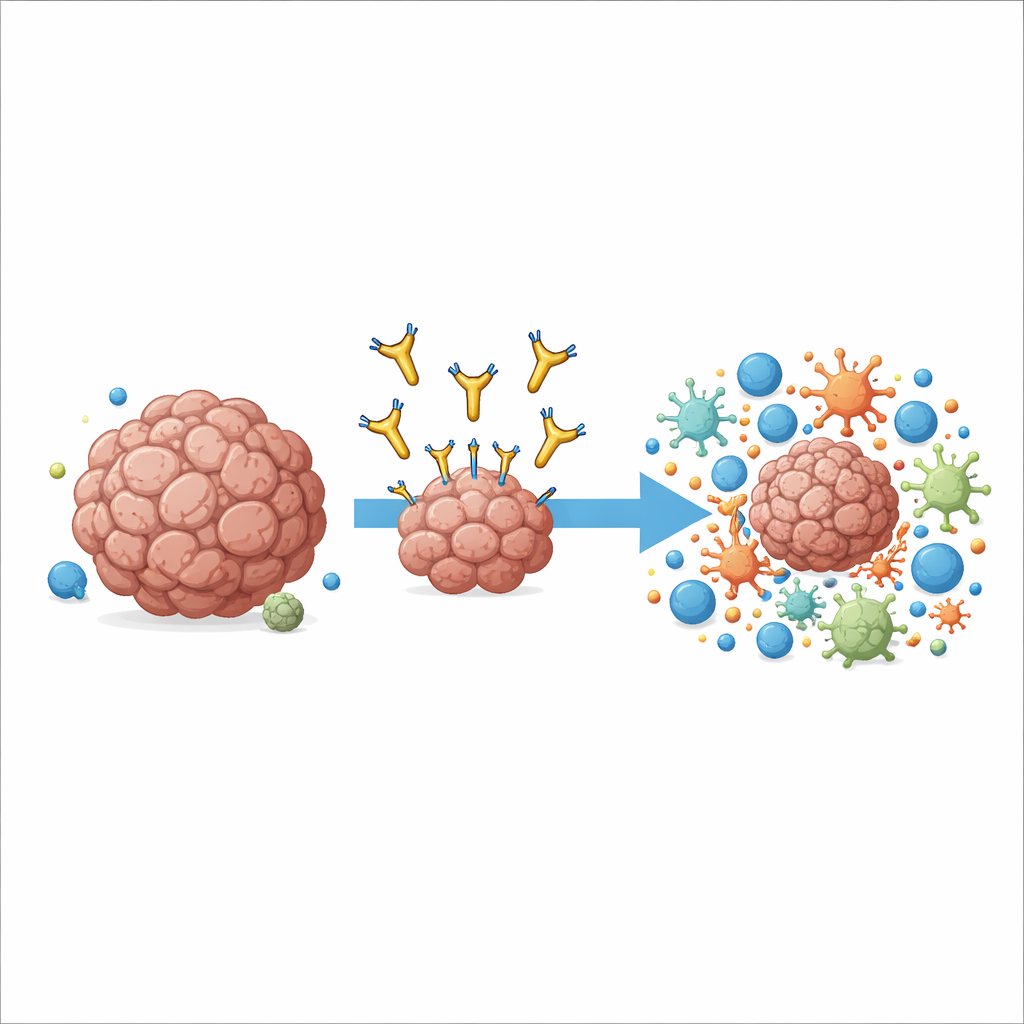
Una nueva forma de apuntar a un objetivo conocido en el cáncer
El trabajo se centra en una molécula llamada AXL, que se sitúa en la superficie de muchas células cancerosas y de algunas células inmunitarias en el tumor. Niveles altos de AXL se asocian con enfermedad agresiva, diseminación a otros órganos y resistencia a las inmunoterapias estándar. Fármacos anteriores intentaron bloquear la señal de crecimiento de AXL enganchándose a su extremo más externo, pero mostraron solo beneficios modestos en ensayos clínicos y a veces causaron efectos secundarios. Los autores adoptaron un enfoque distinto: diseñaron un anticuerpo, llamado 6C5, que agarra AXL muy cerca de la membrana celular en lugar de en la punta distante. Este sutil cambio en el punto de anclaje resultó crucial para que el sistema inmunitario pudiera utilizar el anticuerpo como un mango.
Reclutar a los ‘basureros’ del organismo
En lugar de envenenar directamente las células cancerosas, 6C5 actúa atrayendo y redirigiendo células inmunitarias especializadas en engullir y procesar restos, especialmente macrófagos y ciertas células dendríticas. En modelos de ratón de melanoma y cáncer de colon diseñados para expresar AXL humano, 6C5 frenó vigorosamente o incluso redujo los tumores, incluidas metástasis pulmonares, pero solo cuando las células tumorales mostraban AXL. El anticuerpo tuvo poco efecto en ratones carentes de células T y B, lo que demuestra que el control tumoral duradero dependía de una respuesta inmune adaptativa completa. Análisis detallados a nivel de célula única de tumores tratados revelaron que 6C5 aumentó de forma drástica el número y la actividad de macrófagos, células dendríticas y células T citotóxicas que infiltraban la masa tumoral, convirtiendo un desierto inmunitario escaso en un campo de batalla abarrotado.
Cómo la limpieza guiada por anticuerpos desencadena un ataque inmune más amplio
Experimentos mecanísticos mostraron que el éxito de 6C5 depende de cómo ancla a los macrófagos a las células tumorales. Al unirse a AXL cerca de la membrana, 6C5 forma grupos compactos que los receptores de los macrófagos pueden agarrar con eficacia, potenciando un proceso llamado fagocitosis celular dependiente de anticuerpos. Los macrófagos engulleron con más facilidad células tumorales recubiertas por anticuerpos cuando 6C5 estaba presente, pero no cuando su región de cola se alteró para impedir el compromiso con los receptores de macrófagos. Esta fagocitosis desencadenó la producción de interferones de tipo I —potentes moléculas de alarma— a través de una vía que dependía de la proteína adaptadora MyD88. Estos interferones, a su vez, activaron las células dendríticas, aumentaron su capacidad para presentar fragmentos tumorales y favorecieron su migración a los nódulos linfáticos. Allí, primaron oleadas de células T CD8+ citotóxicas, en particular un subconjunto muy activo marcado por fuertes moléculas efectoras, que luego regresaron al tumor para atacar.
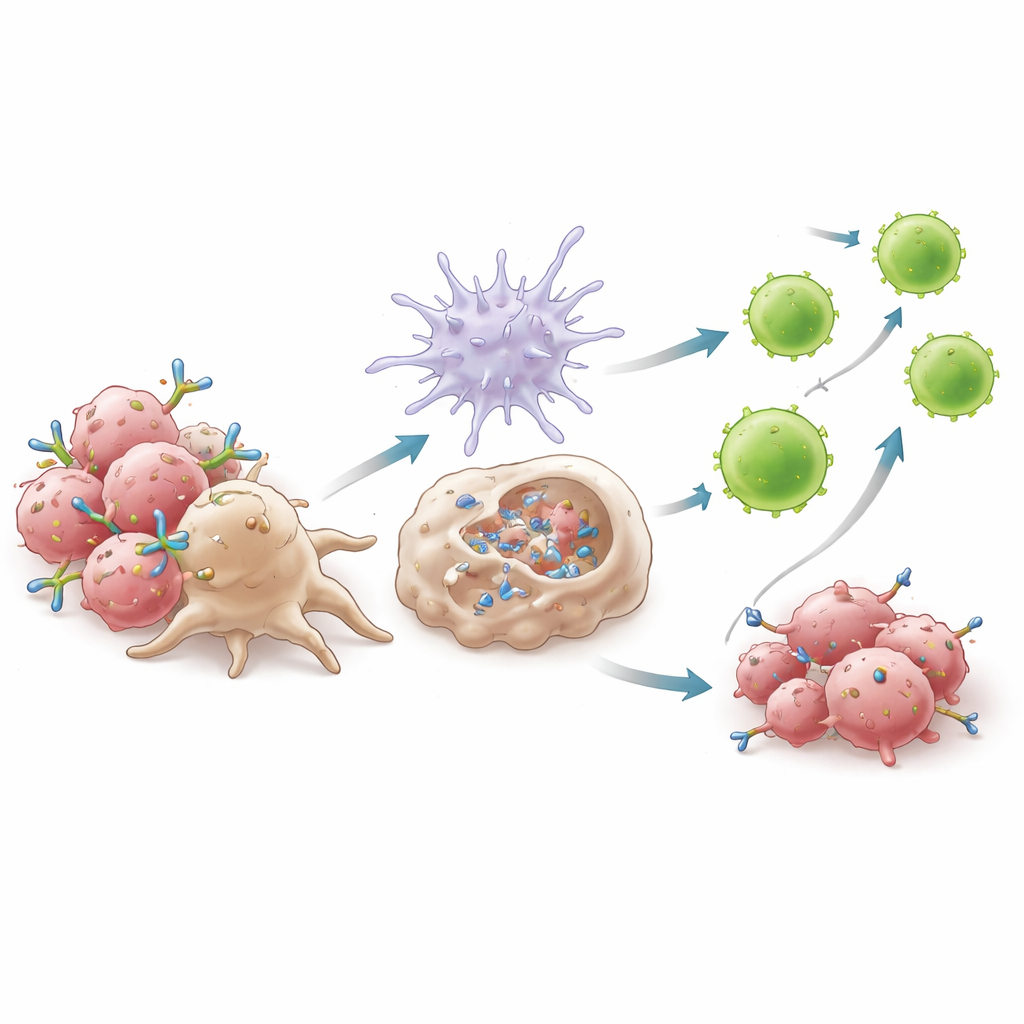
Desenmascarando un freno oculto dentro de las células T colaboradoras
Si bien 6C5 estimuló una vigorosa respuesta antitumoral, también reveló una forma inesperada de auto-sabotaje inmunitario. El tratamiento expandió una población de células T CD4+ que no portaban el marcador clásico de Treg Foxp3 pero que se comportaban de manera igualmente supresiva. Estas células expresaban niveles muy altos de moléculas de control como PD-1 y CTLA-4, producían menos del factor de crecimiento IL-2 y generaban más señales inmunosupresoras. La eliminación de todas las células CD4+ mejoró el control tumoral pero sacrificó la memoria inmune a largo plazo, subrayando que no todas las células colaboradoras son dañinas. En lugar de ello, los autores se dirigieron indirectamente a este subconjunto “tipo Treg” con alta expresión de PD-1. La combinación de 6C5 con bloqueo dual de puntos de control (anti–PD-1 más anti–CTLA-4) redujo selectivamente estas células supresoras en los tumores, preservando al mismo tiempo las células T beneficiosas y mejorando aún más el control tumoral.
Construir protección duradera con terapia combinada
Dado que tanto las Treg como estas células colaboradoras con alta expresión de PD-1 consumen intensamente IL-2, el equipo probó también un fármaco de nueva generación que acopla una señal de IL-2 modificada a PD-1, focalizando su acción en las células T agotadas que infiltran el tumor. Cuando 6C5 se combinó con esta fusión de IL-2 dirigida a PD-1, aproximadamente la mitad de los ratones eliminó completamente sus tumores. De forma notable, todos los animales curados rechazaron un reimplante tumoral posterior, lo que indica una memoria inmune robusta y duradera. En contraste, la simple eliminación de células CD4+ careció de esta protección duradera. En conjunto, estos resultados muestran que afinar en lugar de eliminar el compartimento CD4+ puede desatar una potente inmunidad antitumoral sin minar la capacidad del sistema inmunitario para “recordar” el tumor.
Qué podría significar esto para el futuro del tratamiento del cáncer
Este estudio demuestra que el lugar donde un anticuerpo se une a una molécula tumoral puede cambiar fundamentalmente cómo recluta al sistema inmunitario. Al dirigirse a un sitio proximal a la membrana en AXL, 6C5 actúa menos como un bloqueador de señales y más como un amplificador inmunitario: fomenta la limpieza por macrófagos, las alarmas por interferón, la activación de células dendríticas y poderosos ataques de células T citotóxicas. Al mismo tiempo, el trabajo expone nuevas células T supresoras no clásicas que emergen durante la terapia y muestra cómo combinaciones a medida con inhibidores de puntos de control o agentes basados en IL-2 pueden neutralizar estos frenos. Si anticuerpos y estrategias similares resultan seguros y eficaces en humanos, podrían ofrecer una forma de convertir tumores obstinadamente inmunológicamente fríos en tumores inmunológicamente calientes que finalmente respondan a la inmunoterapia.
Cita: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Palabras clave: inmunoterapia del cáncer, microambiente tumoral, anticuerpo contra AXL, fagocitosis por macrófagos, resistencia a puntos de control inmunitario