Clear Sky Science · it
Riprogrammare il microambiente tumorale con un anticorpo contro AXL prossimo alla membrana per superare la resistenza al blocco dei checkpoint immunitari
Perché alcuni tumori si nascondono dal sistema immunitario
L’immunoterapia del cancro ha trasformato il trattamento per molti pazienti, ma fallisce ancora in una larga fetta di tumori che il sistema immunitario nota a malapena. Questi cosiddetti tumori “freddi” contengono poche cellule immunitarie attaccanti e spesso resistono agli attuali potenti farmaci anti-checkpoint. Questo studio esplora un nuovo tipo di anticorpo che risveglia le difese di prima linea dell’organismo all’interno di tali tumori, aiutando a trasformare un cancro freddo e silenzioso in uno popolato da cellule immunitarie che uccidono il tumore.
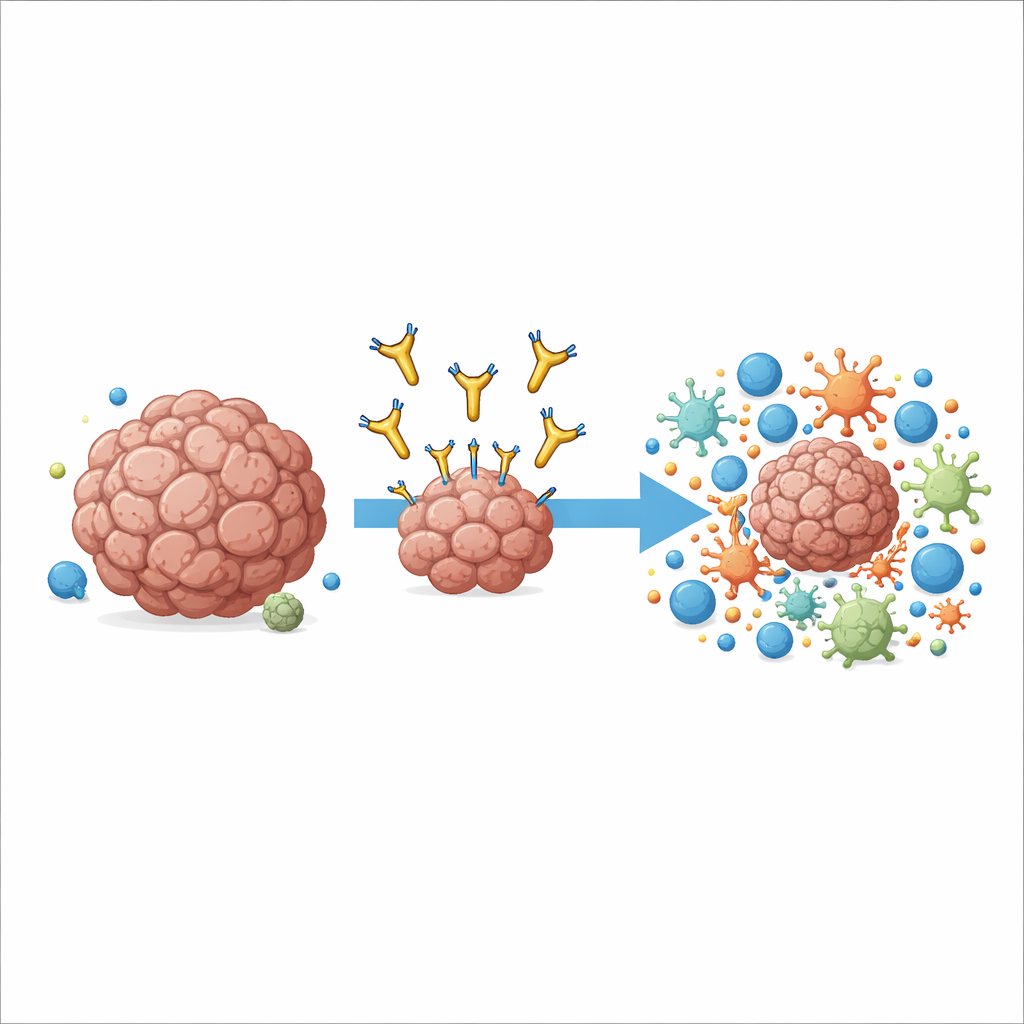
Un nuovo modo di mirare a un bersaglio tumorale noto
Il lavoro si concentra su una molecola chiamata AXL, che si trova sulla membrana di molte cellule tumorali e di alcune cellule immunitarie nel tumore. Livelli elevati di AXL sono associati a malattia aggressiva, diffusione ad altri organi e resistenza alle immunoterapie standard. Farmaci precedenti hanno cercato di bloccare il segnale di crescita di AXL legandosi alla sua estremità più esterna, ma hanno mostrato benefici modesti nelle sperimentazioni cliniche e talvolta effetti collaterali. Gli autori hanno seguito un approccio diverso: hanno costruito un anticorpo, chiamato 6C5, che afferra AXL molto vicino alla membrana cellulare invece che alla punta distante. Questo sottile spostamento nel punto di aggancio si è rivelato cruciale per il modo in cui il sistema immunitario può usare l’anticorpo come punto di presa.
Reclutare i netturbini dell’organismo
Piuttosto che avvelenare direttamente le cellule tumorali, 6C5 agisce richiamando e rimodulando cellule immunitarie specializzate nell’inglobare e processare detriti, in particolare macrofagi e alcuni dendritici. In modelli murini di melanoma e tumore del colon ingegnerizzati per esprimere AXL umano, 6C5 ha rallentato potentemente o addirittura ridotto i tumori, comprese le metastasi polmonari, ma solo quando le cellule tumorali esponevano AXL. L’anticorpo ha avuto scarso effetto in topi privi di cellule T e B, mostrando che il controllo duraturo del tumore dipendeva da una risposta adattativa completa. Analisi dettagliate a singola cellula dei tumori trattati hanno rivelato che 6C5 aumentava drasticamente il numero e l’attività di macrofagi, cellule dendritiche e linfociti T killer infiltranti la massa tumorale, convertendo un deserto immunitario in un campo di battaglia affollato.
Come la pulizia guidata dall’anticorpo scatena un attacco immunitario più ampio
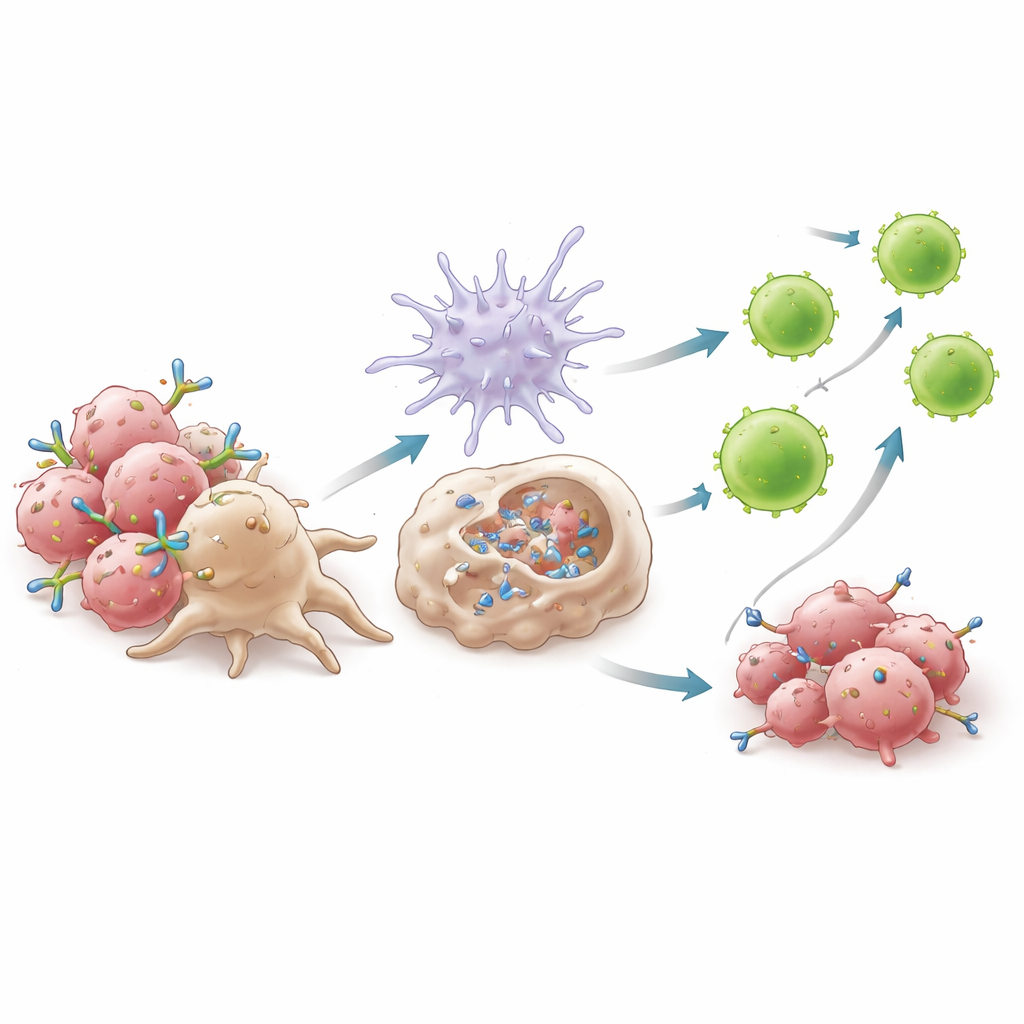
Esperimenti meccanicistici hanno dimostrato che il successo di 6C5 dipende dal modo in cui esso lega i macrofagi alle cellule tumorali. Legandosi ad AXL vicino alla membrana, 6C5 forma aggregati compatti che i recettori dei macrofagi possono afferrare in modo efficiente, potenziando un processo chiamato fagocitosi cellulare dipendente da anticorpi. I macrofagi inglobavano più facilmente le cellule tumorali rivestite dall’anticorpo quando era presente 6C5, ma non quando la regione Fc dell’anticorpo era modificata per impedire l’ingaggio dei recettori dei macrofagi. Questa ingestione ha innescato la produzione di interferoni di tipo I — potenti molecole d’allarme — attraverso una via che dipendeva dalla proteina adattatrice MyD88. Questi interferoni, a loro volta, hanno attivato le cellule dendritiche, aumentandone la capacità di presentare frammenti tumorali e favorendone la migrazione verso i linfonodi. Lì esse hanno primato ondate di linfociti T citotossici CD8+, in particolare un sottogruppo altamente attivo marcato da forti molecole effettrici, che poi sono tornati al tumore per attaccare.
Smascherare un freno nascosto nei linfociti T helper
Pur suscitando una vigorosa risposta anti-tumorale, 6C5 ha anche rivelato una forma inaspettata di autosabotaggio immunitario. Il trattamento ha espanso una popolazione di linfociti CD4+ che non portavano il classico marcatore Treg Foxp3 ma si comportavano in modo altrettanto soppressivo. Queste cellule esprimevano livelli molto alti di molecole checkpoint come PD-1 e CTLA-4, producevano meno del fattore di crescita IL-2 e inviavano più segnali immunosoppressivi. La deplezione di tutti i CD4+ migliorava il controllo del tumore ma sacrificava la memoria immunitaria a lungo termine, sottolineando che non tutti i linfociti helper sono nocivi. Gli autori hanno quindi mirato indirettamente a questo sottogruppo «simile a Treg» PD-1–alto. La combinazione di 6C5 con un doppio blocco dei checkpoint (anti–PD-1 più anti–CTLA-4) ha ridotto selettivamente queste cellule soppressive nei tumori, preservando le cellule T benefiche e migliorando ulteriormente il controllo tumorale.
Costruire una protezione duratura con la terapia combinata
Poiché sia i Treg sia questi linfociti helper PD-1–alti consumano avidamente IL-2, il gruppo ha testato anche un farmaco di nuova generazione che accoppia un segnale IL-2 modificato al PD-1, focalizzandone l’azione sulle cellule T esauste infiltranti il tumore. Quando 6C5 è stato abbinato a questa fusione IL-2 mirata al PD-1, circa la metà dei topi ha eliminato completamente i tumori. In modo notevole, tutti gli animali guariti hanno respinto una successiva nuova inoculazione tumorale, indicando una memoria immunitaria robusta e duratura. Al contrario, la sola rimozione dei CD4+ non ha fornito questa protezione duratura. Nel complesso, questi risultati mostrano che sintonizzare piuttosto che eliminare il compartimento CD4+ può scatenare una forte immunità anti-tumorale senza compromettere la capacità del sistema immunitario di «ricordare» il tumore.
Cosa potrebbe significare per i futuri trattamenti del cancro
Questo studio dimostra che il punto di ancoraggio di un anticorpo su una molecola tumorale può cambiare profondamente il modo in cui recluta il sistema immunitario. Mirando a un sito prossimo alla membrana su AXL, 6C5 agisce meno come bloccante del segnale e più come amplificatore immunitario — alimentando la pulizia da parte dei macrofagi, gli allarmi a interferone, l’attivazione delle cellule dendritiche e potenti attacchi dei linfociti T citotossici. Allo stesso tempo, il lavoro mette in luce nuove cellule T soppressive non classiche che emergono durante la terapia e mostra come combinazioni mirate con inibitori dei checkpoint o agenti a base di IL-2 possano neutralizzare questi freni. Se anticorpi e strategie simili risultassero sicuri ed efficaci nell’uomo, potrebbero offrire un modo per convertire tumori finora refrattari e immunologicamente freddi in tumori immuno-caldi che finalmente rispondono all’immunoterapia.
Citazione: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Parole chiave: immunoterapia del cancro, microambiente tumorale, anticorpo contro AXL, fagocitosi da parte dei macrofagi, resistenza ai checkpoint immunitari