Clear Sky Science · pt
Reprogramando o microambiente tumoral com anticorpo contra AXL proximal à membrana para superar a resistência ao bloqueio de ponto de verificação imune
Por que alguns tumores se escondem do sistema imunológico
A imunoterapia contra o câncer transformou o tratamento de muitos pacientes, mas ainda fracassa em uma grande parcela dos tumores que o sistema imunológico mal percebe. Esses chamados tumores “frios” contêm poucas células imunes atacantes e frequentemente resistem aos potentes medicamentos de ponto de verificação atuais. Este estudo explora um novo tipo de anticorpo que desperta as defesas de primeira linha do corpo dentro desses tumores, ajudando a transformar um câncer frio e silencioso em um alvo repleto de células imunes capazes de matar o tumor.
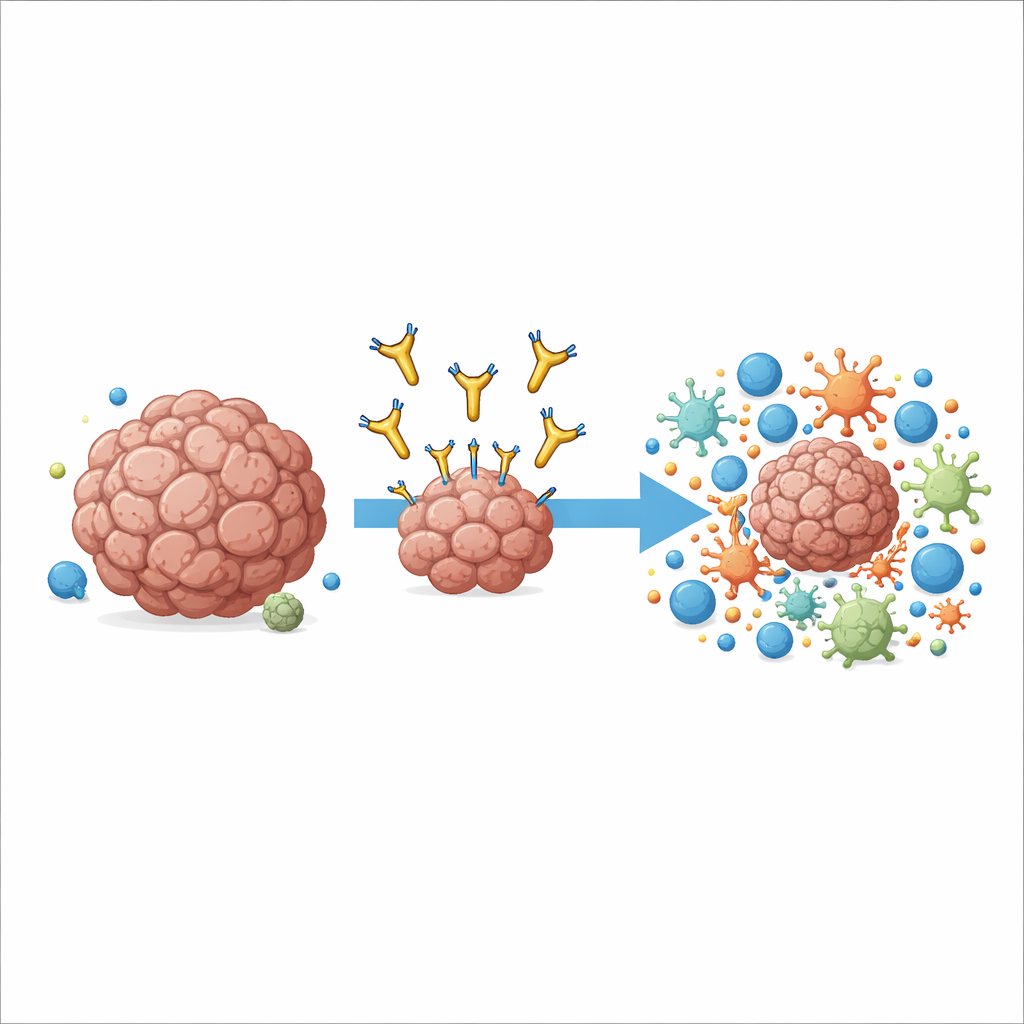
Uma nova maneira de mirar um alvo conhecido no câncer
O trabalho centra-se em uma molécula chamada AXL, presente na superfície de muitas células cancerosas e em algumas células imunes no tumor. Níveis altos de AXL estão associados a doença agressiva, metástase e resistência às imunoterapias padrão. Drogas anteriores tentaram bloquear o sinal de crescimento da AXL fixando-se em sua ponta mais externa, mas mostraram benefícios modestos em ensaios clínicos e às vezes causaram efeitos colaterais. Os autores adotaram uma abordagem diferente: construíram um anticorpo, chamado 6C5, que se liga à AXL muito próximo à membrana celular em vez da ponta distante. Essa mudança sutil na posição de ancoragem revelou-se crucial para a forma como o sistema imunológico pôde usar o anticorpo como um ponto de pega.
Recrutando os coletores de lixo do corpo
Em vez de envenenar diretamente as células cancerosas, o 6C5 atua atraindo e redirecionando células imunes especializadas em engolir e processar detritos, em especial macrófagos e certos tipos de células dendríticas. Em modelos murinos de melanoma e câncer de cólon engenheirados para expressar AXL humano, o 6C5 retardou poderosamente ou até reduziu tumores, inclusive metástases pulmonares, mas somente quando as células tumorais exibiam AXL. O anticorpo teve pouco efeito em camundongos desprovidos de células T e B, mostrando que o controle duradouro do tumor dependia de uma resposta imune adaptativa completa. Análises detalhadas em nível de célula única dos tumores tratados revelaram que o 6C5 aumentou dramaticamente o número e a atividade de macrófagos, células dendríticas e células T assassinas infiltrando a massa tumoral, convertendo um deserto imune esparso em um campo de batalha lotado.
Como a limpeza guiada por anticorpo desencadeia um ataque imune mais amplo
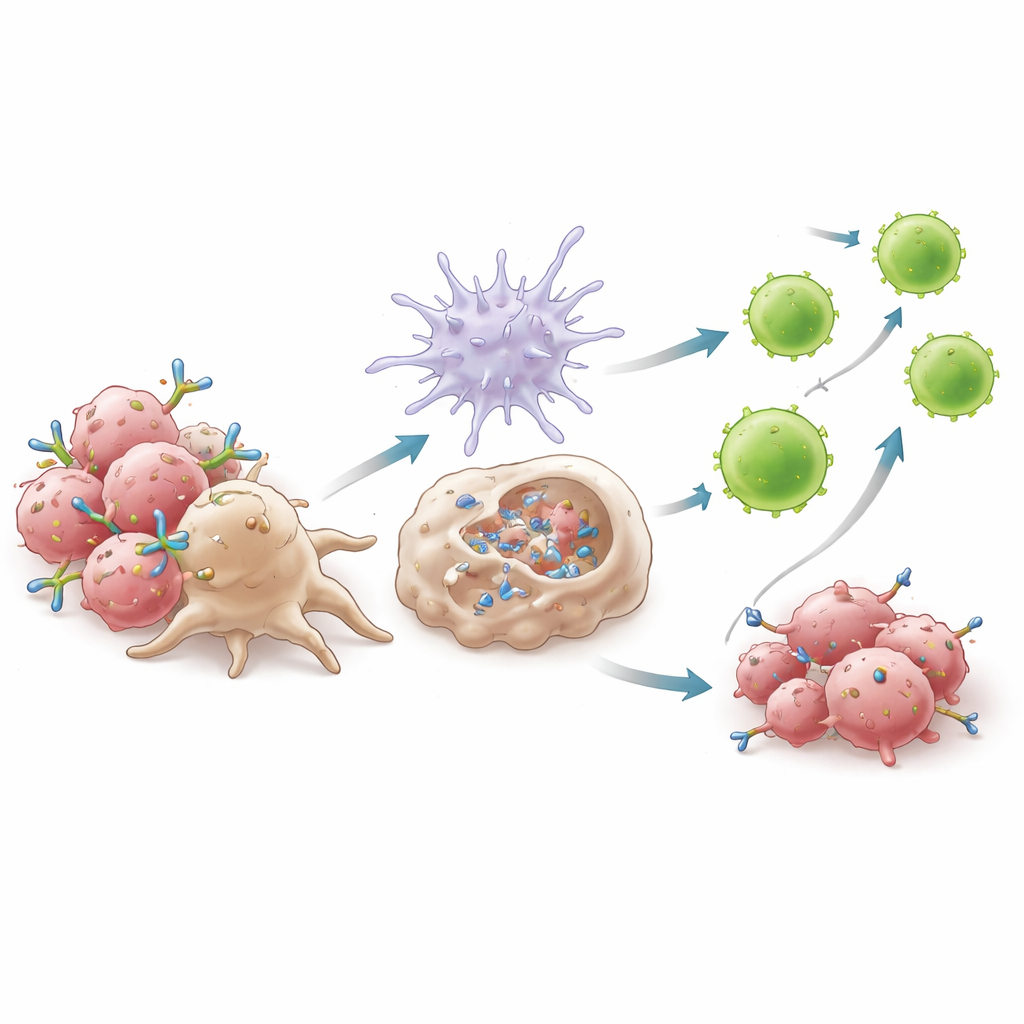
Experimentos mecanísticos mostraram que o sucesso do 6C5 depende de como ele prende os macrófagos às células tumorais. Ao se ligar à AXL próxima à membrana, o 6C5 forma aglomerados compactos que os receptores dos macrófagos conseguem agarrar com eficiência, potencializando um processo chamado fagocitose celular dependente de anticorpo. Os macrófagos engoliram com mais facilidade células tumorais revestidas pelo anticorpo quando o 6C5 estava presente, mas não quando a região Fc do anticorpo foi alterada para impedir o engajamento dos receptores dos macrófagos. Essa fagocitose desencadeou a produção de interferons do tipo I — moléculas de alarme potentes — por meio de uma via que dependia da proteína adaptadora MyD88. Esses interferons, por sua vez, ativaram células dendríticas, aumentaram sua capacidade de apresentar fragmentos tumorais e incentivaram sua migração para os linfonodos. Lá, elas primaram ondas de células T citotóxicas CD8+, particularmente um subconjunto altamente ativo marcado por fortes moléculas efetoras, que então retornaram ao tumor para atacar.
Desmascarando um freio oculto nas células T auxiliares
Embora o 6C5 tenha provocado uma resposta antitumoral vigorosa, também revelou uma forma inesperada de autossabotagem imune. O tratamento expandiu uma população de células T CD4+ que não carregavam o marcador clássico de Treg Foxp3, mas se comportavam de maneira suprimidora semelhante. Essas células expressavam níveis muito altos de moléculas de ponto de verificação como PD-1 e CTLA-4, produziam menos do fator de crescimento IL-2 e geravam mais sinais imunossupressores. A depleção de todas as células CD4+ melhorou o controle tumoral, mas sacrificou a memória imune de longo prazo, ressaltando que nem todas as células auxiliares são prejudiciais. Em vez disso, os autores alvejaram indiretamente esse subconjunto “semelhante a Treg” com alta expressão de PD-1. Combinar 6C5 com bloqueio duplo de pontos de verificação (anti–PD-1 mais anti–CTLA-4) reduziu seletivamente essas células supressoras nos tumores, preservando as células T benéficas e melhorando ainda mais o controle tumoral.
Construindo proteção duradoura com terapia combinada
Como tanto as Tregs quanto essas células auxiliares PD-1–altas consomem avidamente IL-2, a equipe também testou um fármaco de próxima geração que acopla um sinal modificado de IL-2 ao PD-1, focalizando sua ação em células T exauridas que infiltram o tumor. Quando o 6C5 foi combinado com essa fusão de IL-2 direcionada ao PD-1, cerca de metade dos camundongos eliminou completamente seus tumores. Notavelmente, todos os animais curados rejeitaram um novo desafio tumoral posterior, indicando memória imune robusta e duradoura. Em contraste, simplesmente remover as células CD4+ não produziu essa proteção duradoura. Em conjunto, esses resultados mostram que ajustar, em vez de erradicar, o compartimento de CD4+ pode desencadear uma imunidade anticâncer forte sem minar a capacidade do sistema imunológico de “lembrar” o tumor.
O que isso pode significar para o tratamento futuro do câncer
Este estudo demonstra que onde um anticorpo se liga a uma molécula tumoral pode mudar fundamentalmente a forma como ele recruta o sistema imunológico. Ao mirar um sítio proximal à membrana na AXL, o 6C5 age menos como um bloqueador de sinal e mais como um amplificador imune — impulsionando a limpeza pelos macrófagos, alarmes por interferon, ativação de células dendríticas e ataques potentes de células T assassinas. Ao mesmo tempo, o trabalho expõe novos linfócitos T supressores não clássicos que surgem durante a terapia e mostra como combinações sob medida com inibidores de ponto de verificação ou agentes à base de IL-2 podem neutralizar esses freios. Se anticorpos e estratégias semelhantes se mostrarem seguros e eficazes em humanos, eles poderão oferecer uma forma de converter tumores teimosos e imuno-frios em tumores imuno-quentes que finalmente respondem à imunoterapia.
Citação: Yang, Z., Cao, S., Zhang, J. et al. Reprogramming the tumor microenvironment with antibody against membrane-proximal AXL to overcome immune checkpoint blockade resistance. Sig Transduct Target Ther 11, 139 (2026). https://doi.org/10.1038/s41392-026-02664-x
Palavras-chave: imunoterapia contra o câncer, microambiente tumoral, anticorpo contra AXL, fagocitose por macrófagos, resistência ao bloqueio de pontos de verificação imune