Clear Sky Science · zh
针对损伤相关巨噬细胞的GPR34可增强抗肿瘤免疫并提高苏鲁法替尼在胰腺癌中的疗效
本研究的重要性
胰腺癌是致死率极高的癌症之一,部分原因在于肿瘤被一层“免疫力场”所包围,阻挡了免疫系统的攻击。本文揭示了一类构建该防护屏障的关键免疫细胞,并显示仅禁用这些细胞上的一个分子开关,就能显著提升标准治疗的效果。对于患者而言,这项研究指向了更聪明的药物组合,有望最终使机体自身防御占上风。
肿瘤周围的隐形帮手
胰腺肿瘤生长在由免疫细胞和结缔组织细胞密集构成的肿瘤微环境中。其中最具影响力的居民之一是巨噬细胞——一种通常负责清除坏死组织并协调修复的白细胞。在胰腺癌中,这些肿瘤相关巨噬细胞常常倒向另一方,抑制免疫反应并帮助癌症抵抗治疗。一种名为苏鲁法替尼的药物,已用于其他癌症,能够抑制维持这些巨噬细胞生存的主要生长信号之一。但其在胰腺癌中的效果一直有限,这提示巨噬细胞可能有备用通路来维持其保护肿瘤的作用。
在治疗过程中追踪单个细胞
研究人员开展了一项临床试验,让胰腺癌患者在手术前接受苏鲁法替尼与标准化疗的联合治疗。通过单细胞RNA测序——一种读取数千个单细胞基因活性的技术——他们绘制了切除肿瘤中的所有细胞类型图谱,并将对治疗有反应的患者与肿瘤持续生长的患者进行了比较。无反应者总体上有更多的巨噬细胞,且其中一种亚型尤为占主导地位。这类细胞携带高水平的受体GPR34,并展现出与组织损伤反应、垃圾清除和形成免疫抑制环境相关的基因程序。与此同时,无反应者肿瘤中还含有更多衰竭的“疲惫”杀伤性T细胞,它们已失去高效攻击癌细胞的能力。
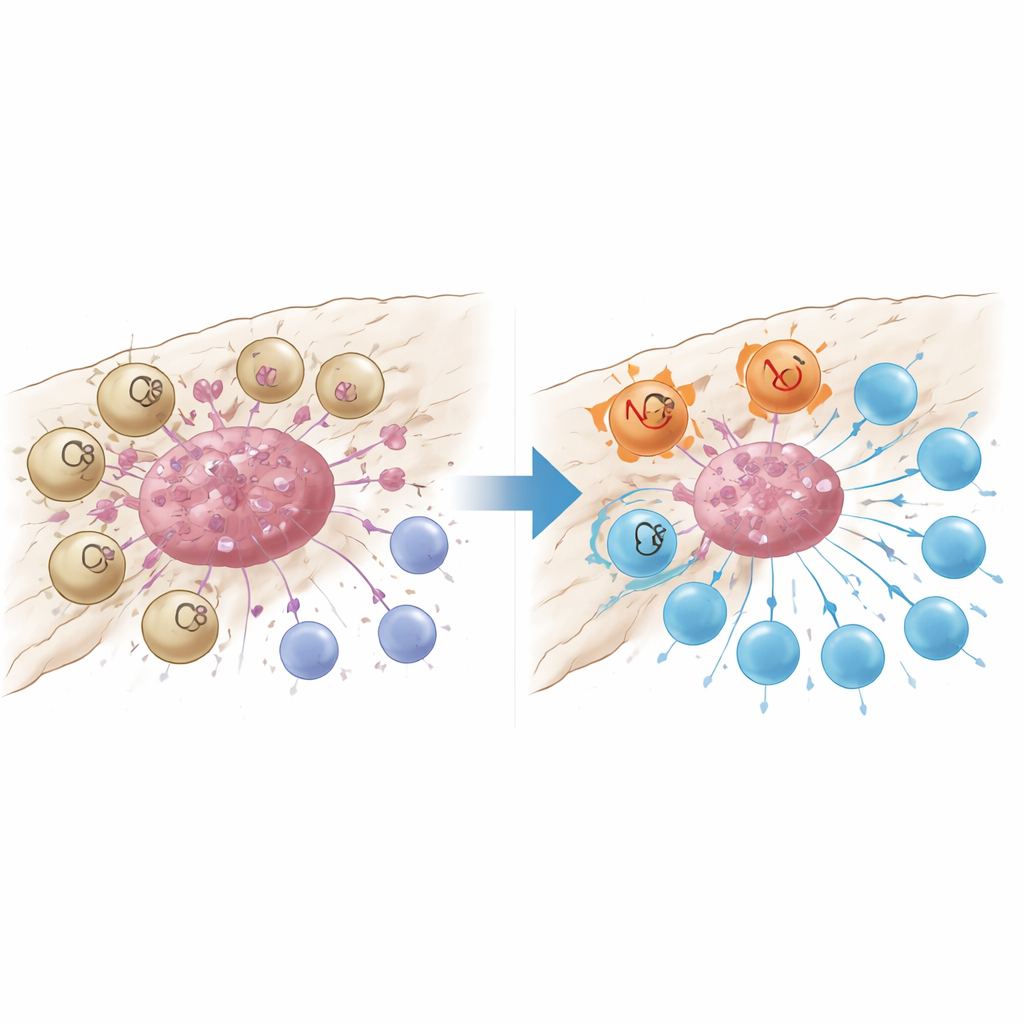
能关闭T细胞的损伤感应器
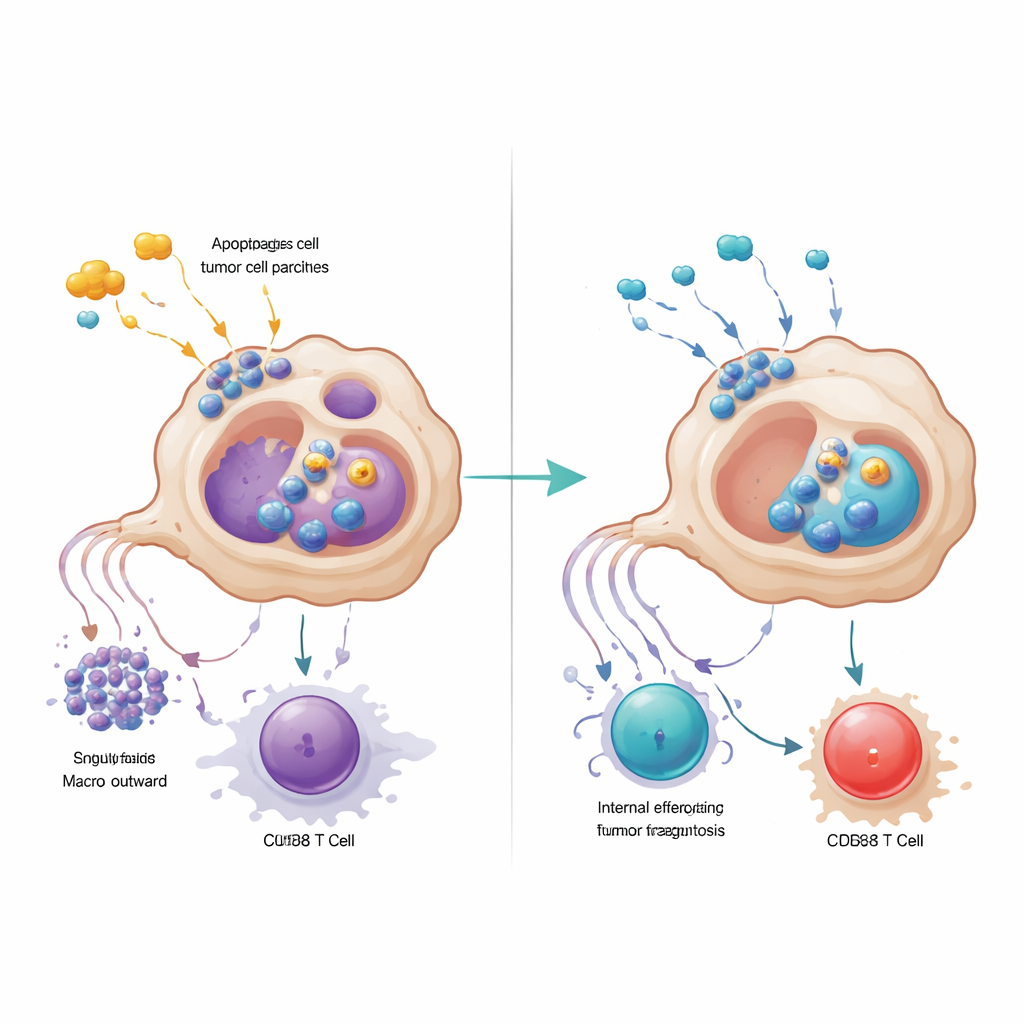
更深入的分析显示,被GPR34标记的巨噬细胞在肿瘤巢内紧密聚集,而在周围正常组织或炎症但非癌变的胰腺中则很少见。肿瘤中这类细胞更多的患者,抗癌的CD8 T细胞更少,抑制免疫的调节性T细胞更多,且生存期更短。在仅在巨噬细胞中敲除GPR34的小鼠模型中,化疗突然变得更有效:肿瘤明显缩小,肿瘤内的T细胞数量增多且不那么疲惫。体外共培养实验解释了原因。当携带GPR34的巨噬细胞感知到由凋亡肿瘤细胞释放的分子“危险信号”——尤其是一种名为溶血磷脂酰丝氨酸的脂质时,它们会增强一种称为清除性吞噬(efferocytosis)的过程,通过该过程吞噬死亡细胞碎片。这不仅提高了它们吞噬肿瘤碎片的能力,还激活了内部的溶酶体通路,分解它们向T细胞呈递肿瘤抗原所需的关键分子。
使免疫攻击失效的两种方式
GPR34驱动的巨噬细胞通过第二种方式削弱T细胞:在摄取受损肿瘤物质后分泌大量趋化因子CXCL16。CXCL16作为一种持续的刺激信号,推动CD8 T细胞进入一种疲惫状态,使其在细胞表面表达抑制分子并丧失杀伤力。阻断GPR34减少了CXCL16的释放,恢复了巨噬细胞的抗原呈递,并重振了T细胞功能。研究团队追踪了从损伤信号脂质,经由GPR34和细胞内常见生长通路,直到启动清除性吞噬和溶酶体的事件链。当他们用药理手段阻断下游的吞噬或溶酶体步骤时,巨噬细胞保留了更多用于呈递抗原的分子,并支持更强的T细胞反应,这强调了过度清理反而会使肿瘤在免疫监视下“消失”的悖论。
让现有药物更有效
基于这一机制图谱,研究者在多个小鼠模型以及带有免疫细胞的患者来源肿瘤类器官中测试了一种小分子GPR34抑制剂。将该GPR34拮抗剂加入化疗和苏鲁法替尼中,始终使肿瘤更小、肿瘤细胞死亡更多、CD8 T细胞活性更强,且T细胞疲惫的迹象更少,且在主要器官或血液指标中未见明显额外毒性。相比之下,单独直接中和CXCL16并未复制这些益处,这凸显出关键的杠杆点在于巨噬细胞的损伤感应器及其对清除性吞噬和抗原呈递的影响。简而言之,这项研究表明,胰腺癌中的某些巨噬细胞像过度热心的街道清道夫,不仅清除碎片,还抹去免疫系统所需的线索。关闭它们的GPR34开关能够让化疗造成的损伤暴露肿瘤,而非将其隐藏,从而为更持久有效的治疗组合打开了道路。
引用: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
关键词: 胰腺癌, 肿瘤微环境, 巨噬细胞, 免疫治疗, 苏鲁法替尼