Clear Sky Science · fr
Cibler GPR34 dans les macrophages associés aux lésions renforce l’immunité anti-tumorale et l’efficacité du Surufatinib dans le cancer du pancréas
Pourquoi cette étude est importante
Le cancer du pancréas est l’un des cancers les plus mortels, en partie parce qu’il est entouré d’un « champ de force » immunitaire qui protège la tumeur des attaques. Cet article met au jour un groupe clé de cellules immunitaires qui contribuent à bâtir ce bouclier et montre que désactiver un seul interrupteur moléculaire sur ces cellules peut améliorer sensiblement l’efficacité des traitements standards. Pour les patients, ces travaux ouvrent la voie à des combinaisons de médicaments plus intelligentes qui pourraient enfin renverser la balance en faveur des défenses naturelles de l’organisme.
Les aides cachées autour de la tumeur
Les tumeurs pancréatiques se développent au sein d’un voisinage dense de cellules immunitaires et de cellules conjonctives appelé microenvironnement tumoral. Parmi les résidents les plus influents figurent les macrophages—cellules sanguines blanches qui nettoient normalement les tissus morts et coordonnent la réparation. Dans le cancer du pancréas, ces macrophages associés à la tumeur prennent souvent le parti du cancer, atténuant les réponses immunitaires et aidant la tumeur à résister aux traitements. Un médicament, le Surufatinib, déjà employé pour d’autres cancers, cible l’un des signaux de croissance principaux qui maintiennent ces macrophages en vie. Mais son impact dans le cancer du pancréas a été limité, ce qui suggère que les macrophages disposent de voies de secours qui préservent leurs rôles protecteurs pour la tumeur.
Suivre des cellules individuelles pendant le traitement
Les chercheurs ont lancé un essai clinique dans lequel des personnes atteintes d’un cancer du pancréas ont reçu du Surufatinib en association avec une chimiothérapie standard avant chirurgie. À l’aide du séquençage ARN unicellulaire—une technique qui lit l’activité génétique de milliers de cellules individuelles—ils ont cartographié tous les types cellulaires des tumeurs retirées et comparé les patients répondant au traitement à ceux dont les tumeurs continuaient de croître. Les non-répondeurs présentaient globalement beaucoup plus de macrophages, et un sous-type en particulier dominait. Ces cellules portaient de hauts niveaux d’un récepteur appelé GPR34 et montraient des programmes géniques liés aux réponses aux lésions tissulaires, à l’élimination des déchets et à la création d’un environnement immunosuppresseur. Parallèlement, les tumeurs des non-répondeurs contenaient davantage de cellules T tueuses « épuisées » qui avaient perdu leur capacité d’attaquer efficacement les cellules cancéreuses.
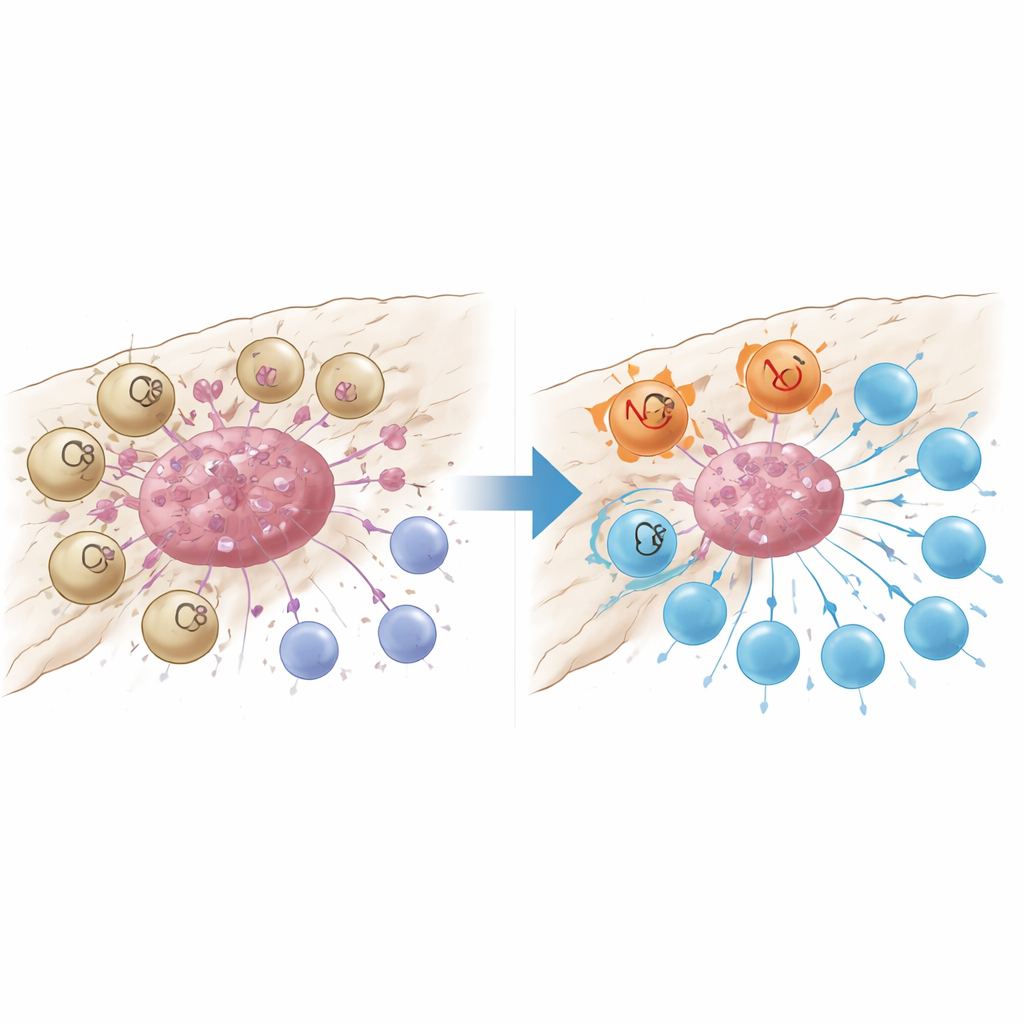
Un capteur de dégâts qui désactive les cellules T
Une analyse plus approfondie a révélé que les macrophages marqués par GPR34 se regroupaient étroitement à l’intérieur des nids tumoraux et étaient rares dans le tissu normal environnant ou dans le pancréas enflammé mais non cancéreux. Les patients dont les tumeurs contenaient davantage de ces cellules avaient moins de lymphocytes CD8 combattant le cancer, plus de lymphocytes T régulateurs qui freinent l’immunité, et des survies plus courtes. Chez des modèles murins modifiés pour être dépourvus de GPR34 uniquement dans les macrophages, la chimiothérapie est devenue soudainement beaucoup plus efficace : les tumeurs ont régressé davantage, et les cellules T présentes dans la tumeur étaient plus nombreuses et moins épuisées. Des expériences de co-culture en laboratoire ont expliqué ce phénomène. Quand des macrophages exprimant GPR34 détectaient des « signaux de danger » moléculaires libérés par les cellules tumorales mourantes—en particulier un lipide appelé lysophosphatidylsérine—ils amplifiaient un processus nommé efférocytose, par lequel ils engloutissent les débris cellulaires. Cela augmentait non seulement leur capacité à absorber les débris tumoraux, mais déclenchait aussi des voies lysosomales internes qui dégradaient des molécules clés nécessaires à la présentation d’antigènes tumoraux aux cellules T.
Deux manières de faire taire l’attaque immunitaire
Les macrophages activés par GPR34 ont sapé l’action des cellules T d’une seconde manière : en sécrétant de fortes quantités de la protéine de signalisation CXCL16 après avoir internalisé le matériel tumoral endommagé. CXCL16 agissait comme un signal de stimulation chronique, poussant les lymphocytes CD8 vers un état d’épuisement où ils expriment des freins à leur surface et perdent leur pouvoir cytotoxique. Bloquer GPR34 réduisait la libération de CXCL16, restaurant l’exposition des antigènes sur les macrophages et revitalisant la fonction des cellules T. L’équipe a retracé la chaîne d’événements depuis le lipide signal de dommage, via GPR34 et une voie de croissance intracellulaire commune, jusqu’à l’activation des machines d’efférocytose et des lysosomes. Lorsqu’ils ont bloqué pharmacologiquement les étapes d’engloutissement ou lysosomales en aval, les macrophages conservaient davantage leurs molécules de présentation d’antigènes et soutenaient des réponses T plus puissantes, soulignant que le nettoyage excessif peut paradoxalement dissimuler la tumeur à la surveillance immunitaire.
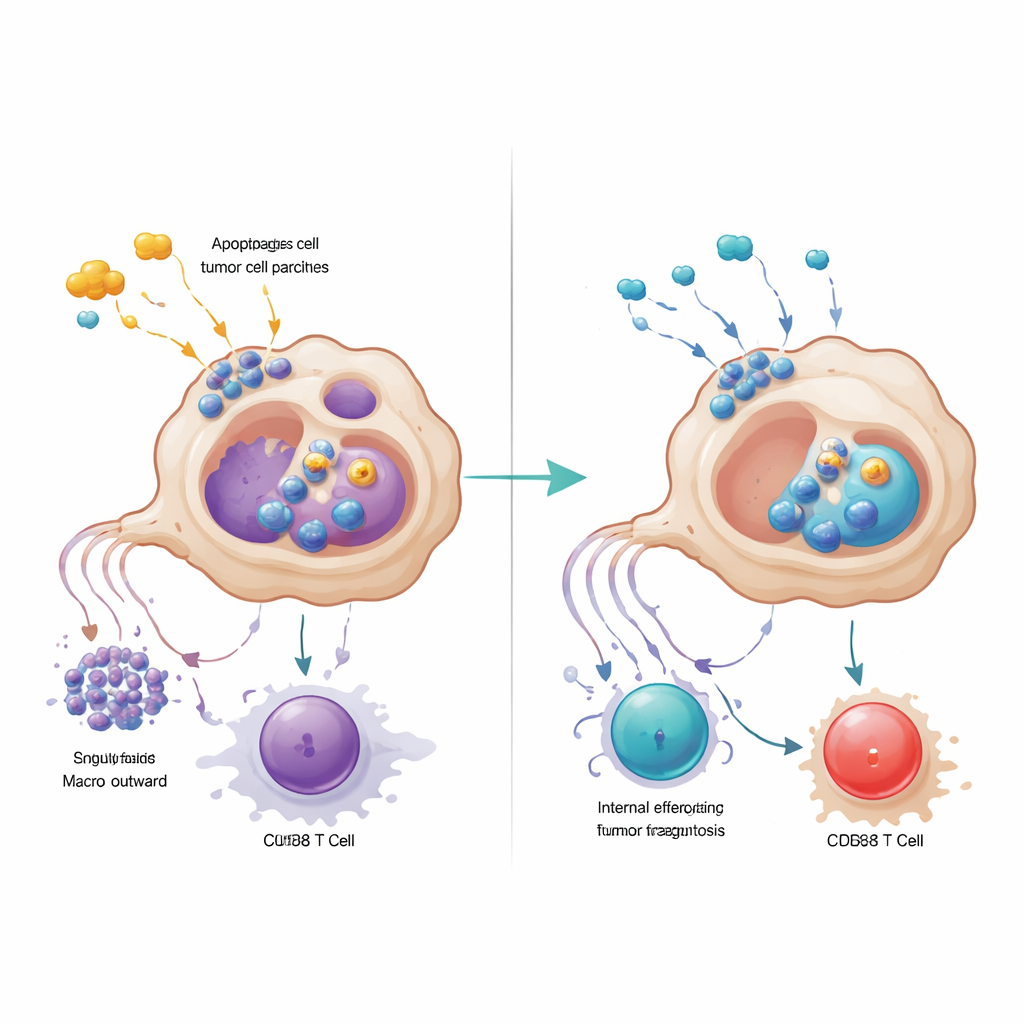
Faire mieux fonctionner les médicaments existants
Munis de cette carte mécanistique, les chercheurs ont testé un petit inhibiteur moléculaire de GPR34 dans plusieurs modèles murins et dans des organoïdes tumoraux dérivés de patients cultivés avec des cellules immunitaires. L’ajout de l’antagoniste de GPR34 à la chimiothérapie et au Surufatinib a systématiquement entraîné des tumeurs plus petites, davantage de mort cellulaire tumorale, une activité renforcée des lymphocytes CD8 et moins de signes d’épuisement des cellules T, sans toxicité ajoutée évidente sur les organes majeurs ou les paramètres sanguins. En revanche, neutraliser directement CXCL16 seul n’a pas reproduit ces bénéfices, ce qui met en relief que le point d’appui central est le capteur de dommage des macrophages et son impact à la fois sur l’efférocytose et la présentation d’antigènes. En termes simples, l’étude suggère que certains macrophages dans le cancer du pancréas agissent comme des nettoyeurs de rue zélés qui, non seulement enlèvent les débris, mais effacent aussi les indices nécessaires au système immunitaire. Désactiver leur interrupteur GPR34 permet à l’atteinte chimio-induite d’exposer la tumeur plutôt que de la cacher, ouvrant la voie à des combinaisons de traitements plus durables et plus efficaces.
Citation: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Mots-clés: cancer du pancréas, microenvironnement tumoral, macrophages, immunothérapie, Surufatinib