Clear Sky Science · pt
Direcionar GPR34 em macrófagos associados a dano aumenta a imunidade antitumoral e a eficácia do Surufatinibe no câncer de pâncreas
Por que este estudo importa
O câncer de pâncreas é um dos mais letais, em parte porque está envolto por um “campo de força” imune que protege o tumor de ataques. Este artigo identifica um grupo-chave de células imunes que ajudam a construir esse escudo e mostra que desativar um único interruptor molecular nessas células pode tornar os tratamentos padrão muito mais eficazes. Para os pacientes, essa pesquisa aponta para combinações de medicamentos mais inteligentes que podem, finalmente, favorecer as defesas do próprio organismo.
Os auxiliares ocultos ao redor do tumor
Os tumores pancreáticos crescem dentro de um ambiente denso de células imunes e conjuntivas conhecido como microambiente tumoral. Entre os residentes mais influentes estão os macrófagos — glóbulos brancos que normalmente removem tecidos mortos e ajudam a coordenar a reparação. No câncer de pâncreas, esses macrófagos associados ao tumor frequentemente mudam de lado, suprimindo respostas imunes e ajudando o câncer a resistir ao tratamento. Um fármaco chamado Surufatinibe, já usado para outros tumores, mira um dos sinais de crescimento principais que mantém esses macrófagos vivos. Mas seu impacto no câncer de pâncreas tem sido modesto, o que sugere que os macrófagos podem dispor de rotas alternativas que preservam suas funções protetoras ao tumor.
Seguindo células individuais durante o tratamento
Os pesquisadores conduziram um ensaio clínico no qual pessoas com câncer de pâncreas receberam Surufatinibe junto com quimioterapia padrão antes da cirurgia. Usando sequenciamento de RNA em célula única — técnica que lê a atividade gênica em milhares de células individuais — eles mapearam todos os tipos celulares nos tumores removidos e compararam pacientes que responderam ao tratamento com aqueles cujos tumores continuaram a crescer. Os não respondedores tinham muito mais macrófagos no geral, e um subtipo em particular predominava. Essas células exibiam altos níveis de um receptor chamado GPR34 e programas gênicos ligados a respostas a danos teciduais, limpeza de resíduos e criação de um ambiente imunossupressor. Ao mesmo tempo, tumores de não respondedores continham mais células T citotóxicas “exaustas” que haviam perdido a capacidade de atacar eficientemente as células cancerígenas.
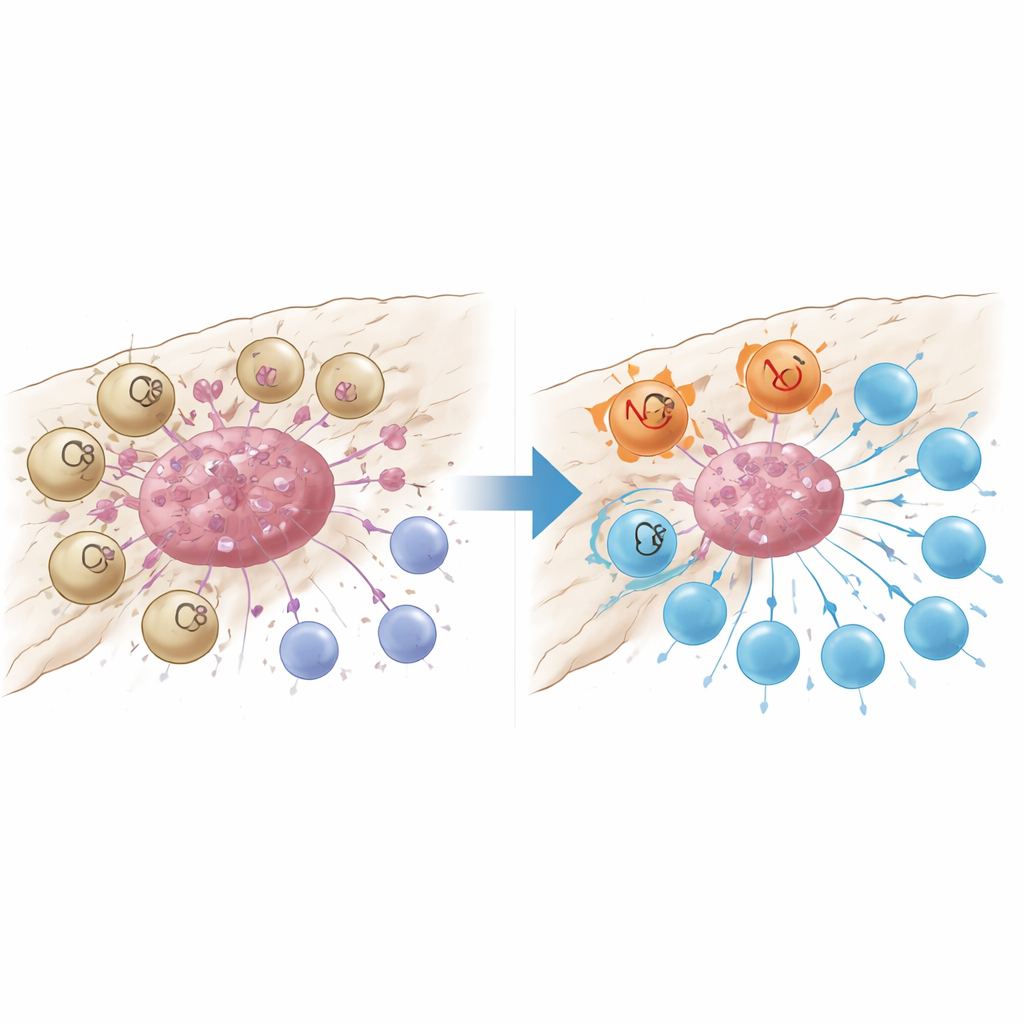
Um sensor de dano que desliga as células T
Análises mais detalhadas revelaram que os macrófagos marcados por GPR34 estavam agrupados dentro dos ninhos tumorais e eram raros no tecido normal adjacente ou no pâncreas inflamado não canceroso. Pacientes cujos tumores continham mais dessas células tinham menos células T CD8 que combatem o câncer, mais células T reguladoras que restringem a imunidade e tempo de sobrevivência mais curto. Em modelos murinos geneticamente modificados para não expressar GPR34 apenas nos macrófagos, a quimioterapia tornou-se subitamente muito mais eficaz: os tumores encolheram mais, e as células T dentro do tumor eram mais numerosas e menos exaustas. Experimentos de co-cultura em laboratório elucidaram o porquê. Quando macrófagos com GPR34 detectavam sinais moleculares de “perigo” liberados por células tumorais moribundas — especialmente um lipídio chamado lisofosfatidilserina — eles aumentavam um processo chamado eferocitose, no qual englobam fragmentos de células mortas. Isso não apenas aumentava sua capacidade de engolir detritos tumorais, mas também ativava vias lisossomais internas que degradavam moléculas essenciais para apresentar antígenos tumorais às células T.
Duas maneiras de silenciar o ataque imune
Os macrófagos dirigidos por GPR34 também minavam as células T de uma segunda forma: ao secretarem altos níveis da proteína sinalizadora CXCL16 após capturar material tumoral danificado. CXCL16 atuava como um sinal de estimulação crônica, empurrando as células T CD8 para um estado exausto em que passam a expressar freios na superfície e perdem poder citotóxico. Bloquear GPR34 reduziu a liberação de CXCL16, restaurou a apresentação de antígeno nos macrófagos e revitalizou a função das células T. A equipe rastreou a cadeia de eventos desde o lipídio sinalizador de dano, passando por GPR34 e uma via de crescimento comum dentro das células, até a ativação da maquinaria de eferocitose e dos lisossomos. Quando bloquearam farmacologicamente as etapas posteriores de englobamento ou lisossomal, os macrófagos retiveram mais moléculas de apresentação de antígeno e favoreceram respostas de células T mais potentes, ressaltando que a limpeza exagerada pode, paradoxalmente, esconder o tumor da vigilância imune.
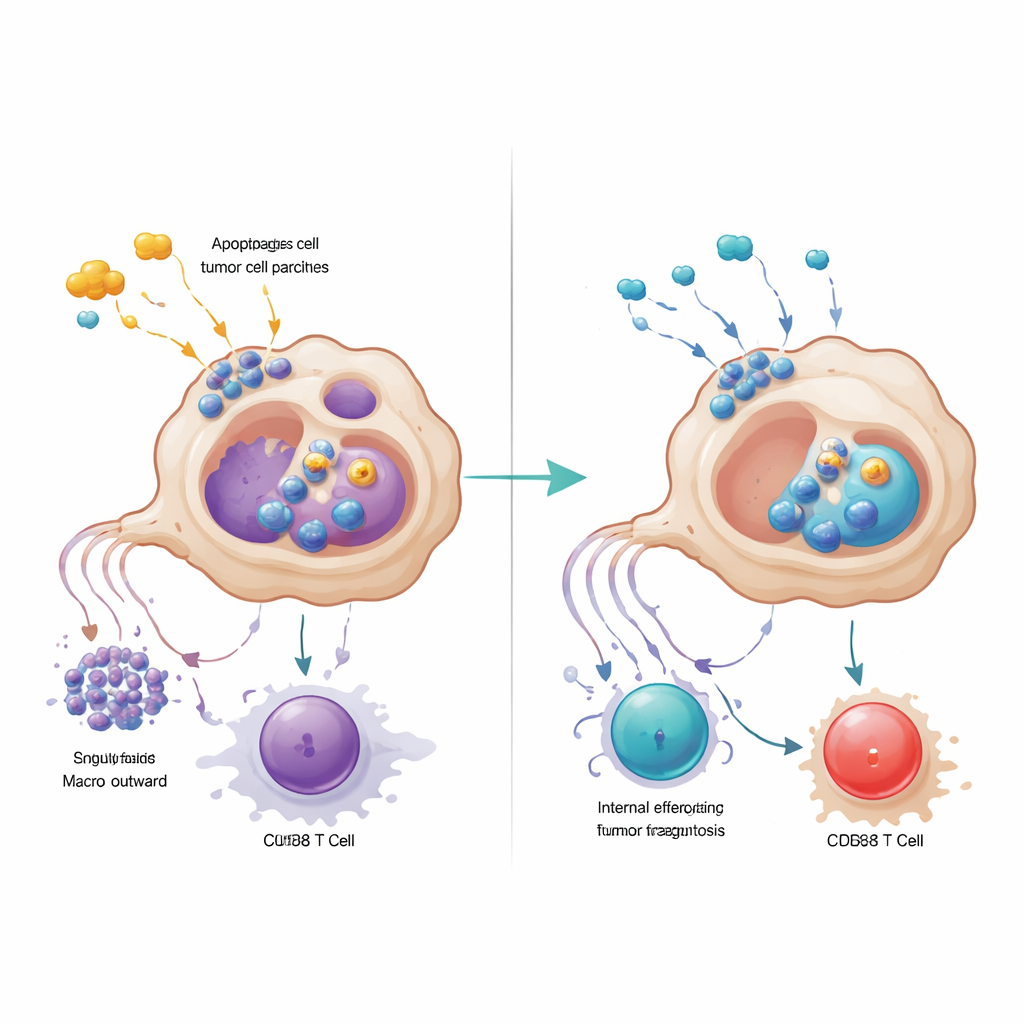
Fazendo medicamentos existentes funcionarem melhor
Munidos desse mapa mecanístico, os pesquisadores testaram um bloqueador de pequeno porte de GPR34 em diversos modelos murinos e em organoides tumorais derivados de pacientes cultivados com células imunes. Adicionar o antagonista de GPR34 à quimioterapia e ao Surufatinibe levou consistentemente a tumores menores, mais morte de célula tumoral, atividade mais forte de células T CD8 e menos sinais de exaustão das células T, sem toxicidade adicional óbvia em órgãos principais ou na contagem sanguínea. Em contraste, neutralizar diretamente CXCL16 isoladamente não reproduziu esses benefícios, destacando que o ponto de alavancagem central é o sensor de dano dos macrófagos e seu impacto tanto na eferocitose quanto na apresentação de antígeno. Em termos simples, o estudo sugere que alguns macrófagos no câncer de pâncreas agem como varredores urbanos excessivamente zelosos que não apenas removem detritos, mas também apagam as pistas que o sistema imune precisa. Desligar seu interruptor GPR34 permite que o dano causado pela quimioterapia exponha o tumor em vez de escondê-lo, abrindo caminho para combinações de tratamento mais duradouras e eficazes.
Citação: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Palavras-chave: câncer de pâncreas, microambiente tumoral, macrófagos, imunoterapia, Surufatinibe