Clear Sky Science · he
מיקוד ב-GPR34 במקרופאגים הקשורים לנזק משפר את החיסוניות נגד הגידול ואת האפקטיביות של סורופאטיניב בסרטן הלבלב
למה המחקר הזה חשוב
סרטן הלבלב הוא אחד מהסרטנים הקטלניים ביותר, בחלקו משום שהוא מוקף ב"שדה כוחות" חיסוני שמגן על הגידול מפני התקפה. מאמר זה חושף קבוצה מרכזית של תאי חיסון שעוזרים לבנות את המגן הזה ומראה כי נטרול מתג מולקולרי יחיד בתאים אלה יכול להפוך טיפולים סטנדרטיים ליעילים הרבה יותר. עבור מטופלים, המחקר מצביע על שילובי תרופות חכמים שיכולים סוף־כל־סוף להטות את הכף לטובת המערכה ההגנתית הטבעית של הגוף.
העוזרים הנסתרים סביב הגידול
גידולי לבלב צומחים בתוך שכונה צפופה של תאים חיסוניים וקישוריים המוכרת כסביבת הגידול. בין התושבים המשפיעים ביותר נמצאים מקרופאגים — תאי דם לבנים שבדרך כלל מנקים רקמה מתה ועוזרים לתאם תיקון. בסרטן הלבלב, מקרופאגים הקשורים לגידול לעתים קרובות משנים צד, מדכאים תגובות חיסוניות ועוזרים לסרטן לעמוד בפני טיפול. תרופה בשם סורופאטיניב, שכבר בשימוש בסרטנים אחרים, פוגעת באחד האותות המרכזיים שמחזיקים את המקרופאגים בחיים. אך השפעתה בסרטן הלבלב הייתה מתונה, מה שמרמז שלמקרופאגים יש מסלולי גיבוי השומרים על תפקידם המגן.
מעקב אחרי תאים בודדים במהלך הטיפול
החוקרים יזמו ניסוי קליני שבו חולי סרטן לבלב קיבלו סורופאטיניב יחד עם כימותרפיה סטנדרטית לפני הניתוח. באמצעות רצף RNA בתא יחיד — טכניקה שקוראת פעילות גנים באלפי תאים בודדים — הם מיפו את כל סוגי התאים בגידולים שהוסרו והשוו בין מטופלים שהגיבו לטיפול לבין אלה שבהם הגידולים המשיכו לגדול. אצל הלא־מגיבים היו מקרופאגים רבים יותר בסך הכל, ותת־סוג אחד במיוחד דומיננטי. תאים אלה נשאו רמות גבוהות של קולטן בשם GPR34 והציגו תכניות גנטיות הקשורות לתגובות לנזק רקמתי, לפינוי פסולת וליצירת סביבה מדכאת חיסון. באותו זמן, בגידולים של הלא־מגיבים נמצאו תאי T קילר "עייפים" רבים יותר שאיבדו את יכולתם לתקוף תאים סרטניים ביעילות.
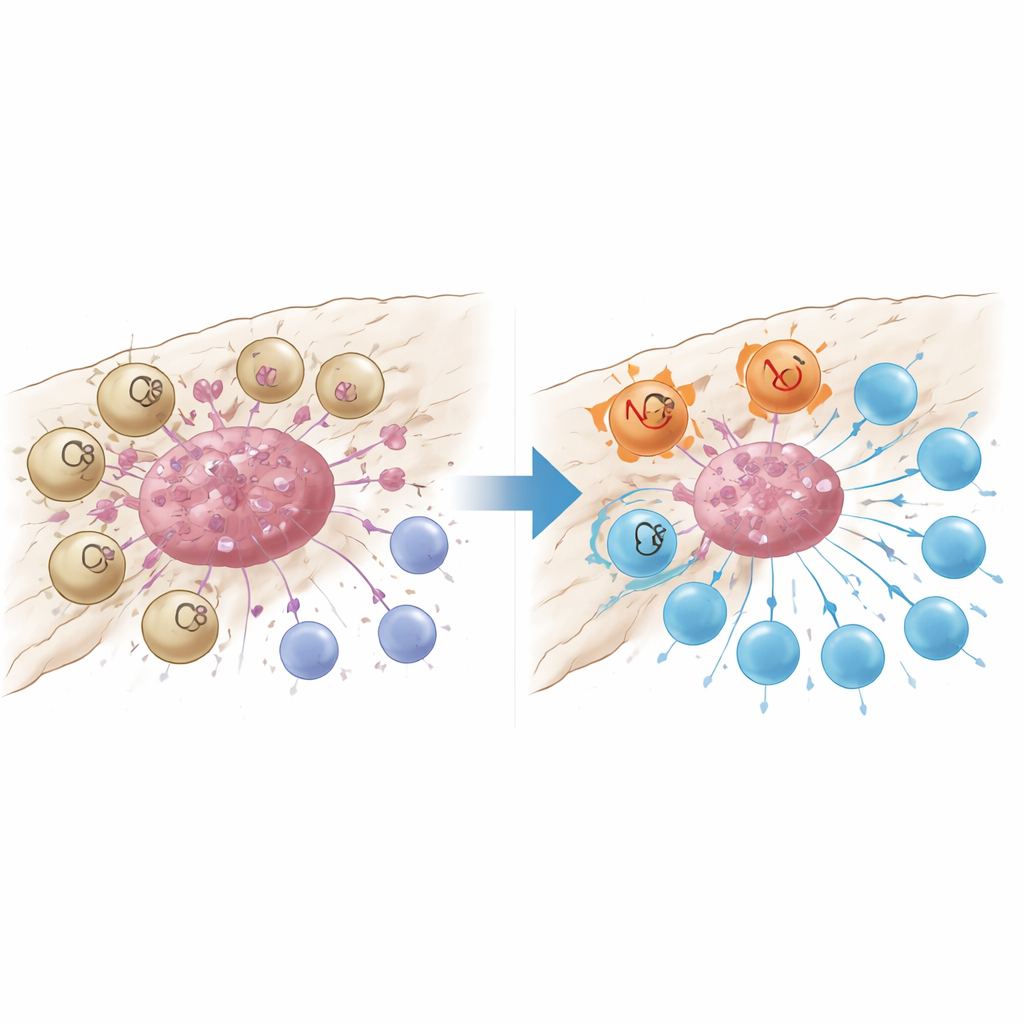
חיישן נזק שמכבּה את תאי ה-T
ניתוח מעמיק הראה שמקרופאגים המסומנים ב-GPR34 היו מרוכזים בצפיפות בתוך קיני הגידול והיו נדירים ברקמה נשאית רגילה או בלבלב מודלק שאינו סרטני. אצל מטופלים שגידוליהם הכילו יותר תאים אלה היו פחות תאי CD8 לוחמים נגד סרטן, יותר תאי T רגולטוריים שמגבילים חיסון וזמני השרדות קצרים יותר. במודלים עכבריים בהם GPR34 נעדר רק במקרופאגים, הכימותרפיה הפכה לפתע ליעילה הרבה יותר: הגידולים התכווצו יותר, ותאי ה-T בתוך הגידול היו רבים פחות ועייפים פחות. ניסויי קוא־קולטורה במעבדה הראו מדוע. כאשר מקרופאגים עם GPR34 זיהו "אותות סכנה" מולקולריים המשוחררים מתאים גידול מתים — במיוחד ליפיד בשם ליזופוספטידילסרין — הם הגבירו תהליך בשם אפרווציטוזיס, שבו הם בולעים שברי תאים מתים. פעולה זו לא רק הגדילה את יכולתם לבלוע פסולת גידול אלא גם הפעלה של מסלולי ליזוזום פנימיים ששברו מולקולות מרכזיות שהם זקוקים להן כדי להציג אנטיגנים של גידול בפני תאי T.
שתי דרכים להשתקת ההתקפה החיסונית
מקרופאגים מונעי GPR34 החלישו את תאי ה-T גם בדרך שנייה: על ידי הפרשת רמות גבוהות של חלבון אותות בשם CXCL16 לאחר קליטת חומר גידולי פגוע. CXCL16 פעל כאות גירוי כרוני, דוחף תאי CD8 למצב עייפות שבו הם מבטאים מעצורים על פני השטח ומאבדים כוח הרג. חסימת GPR34 הפחיתה שחרור CXCL16, שיקמה הצגת אנטיגן במקרופאגים והחייה את תפקוד תאי ה-T. הצוות עקב אחרי שרשרת האירועים מהליפיד האות לנזק, דרך GPR34 ומסלול גדילה תאי שכיח, להפעלת מכונת האפרווציטוזיס וליזוזומים. כאשר חסמו תרופתית את שלבי הבליעה או הליזוזום בתחתית השרשרת, מקרופאגים שמרו יותר ממולקולות הצגת האנטיגן שלהם ותמכו בתגובות חזקות יותר של תאי T, מה שהדגיש כי ניקוי יתר על המידה יכול באופן פרדוקסלי להסתיר את הגידול ממערכות המעקב החיסוני.
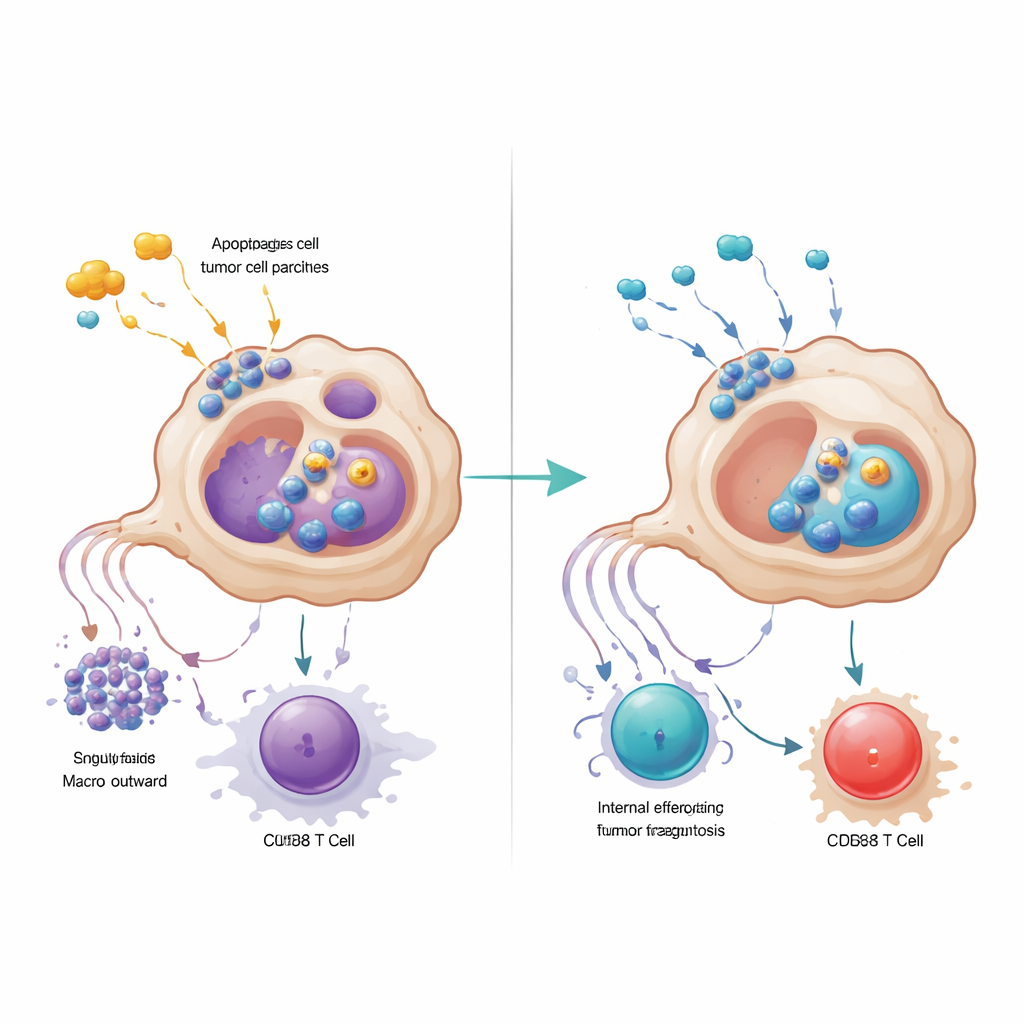
להפוך תרופות קיימות ליעילות יותר
מצוידים במפת המנגנון הזו, החוקרים בחנו מעכב קטן של GPR34 בכמה מודלים עכבריים ובאורגנואידים של גידול שמקורם בחולים שגודלו עם תאים חיסוניים. הוספת האנטגוניסט של GPR34 לכימותרפיה ולסורופאטיניב הובילה בעקביות לגידולים קטנים יותר, ליותר מוות של תאי גידול, לפעילות מוגברת של תאי CD8 ולממצא פחות של עייפות תאי T, ללא רעילות נוספת גלויה באיברים מרכזיים או בספירות דם. לעומת זאת, נטרול ישיר של CXCL16 לבדו לא שחזר את היתרונות הללו, מה שמבליט שנקודת המנוף המרכזית היא חיישן הנזק של המקרופאג והשפעתו הן על אפרווציטוזיס והן על הצגת אנטיגן. במלים פשוטות, המחקר מציע שמספר מקרופאגים בסרטן הלבלב מתנהגים כמו מנקים רחוב נלהבים מדי שלא רק מסירים פסולת אלא גם מוחקים רמזים שהמערכת החיסונית זקוקה להם. כיבוי מתג ה-GPR34 שלהם מאפשר לנזק שנוצר על ידי הכימותרפיה לחשוף את הגידול במקום להסתירו, ובכך לפתוח פתח לשילובים טיפוליים עמידים ויעילים יותר.
ציטוט: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
מילות מפתח: סרטן הלבלב, סביבת הגידול, מקרופאגים, אימונותרפיה, סורופאטיניב