Clear Sky Science · sv
Riktning mot GPR34 i skadaassocierade makrofager förbättrar antitumörimmunitet och effektiviteten hos Surufatinib vid pankreascancer
Varför denna studie är viktig
Pankreascancer är en av de dödligaste cancerformerna, delvis för att tumören omgives av ett immunologiskt ”skyddsfält” som skyddar den från angrepp. Denna artikel identifierar en nyckelgrupp av immunceller som hjälper till att bygga detta skydd och visar att avstängning av en enda molekylär brytare på dessa celler kan göra standardbehandlingar avsevärt mer effektiva. För patienter pekar forskningen mot smartare läkemedelskombinationer som slutligen skulle kunna gynna kroppens egna försvar.
De dolda hjälparna runt tumören
Pankreastumörer växer i ett tätt kvarter av immunceller och bindvävsceller, kallat tumörmikromiljön. Bland de mest inflytelserika invånarna finns makrofager — vita blodkroppar som normalt städar upp död vävnad och hjälper till att samordna reparation. I pankreascancer byter dessa tumörassocierade makrofager ofta sida, dämpar immunsvar och hjälper cancern att motstå behandling. Ett läkemedel kallat Surufatinib, som redan används vid andra cancerformer, riktar in sig på en av de huvudtillväxtsignaler som håller dessa makrofager vid liv. Men dess effekt mot pankreascancer har varit måttlig, vilket tyder på att makrofagerna kan ha reservvägar som bevarar deras tumörskyddande roller.
Spåra enskilda celler under behandling
Forskarna startade en klinisk prövning där personer med pankreascancer fick Surufatinib tillsammans med standardkemoterapi före operation. Genom att använda enkelcells-RNA-sekvensering — en teknik som avläser genaktivitet i tusentals enskilda celler — kartlade de alla celltyper i de borttagna tumörerna och jämförde patienter som svarade på behandlingen med dem vars tumörer fortsatte att växa. Icke-responderande patienter hade generellt fler makrofager, och en särskild subtyp dominerade. Dessa celler bar höga nivåer av en receptor kallad GPR34 och visade genprogram förknippade med skaderespons, avfallsrensning och skapandet av en immunsuppressiv miljö. Samtidigt innehöll tumörer från icke-responderare fler utmattade, ”exhausted” mördarceller (CD8 T-celler) som förlorat sin förmåga att effektivt angripa cancerceller.
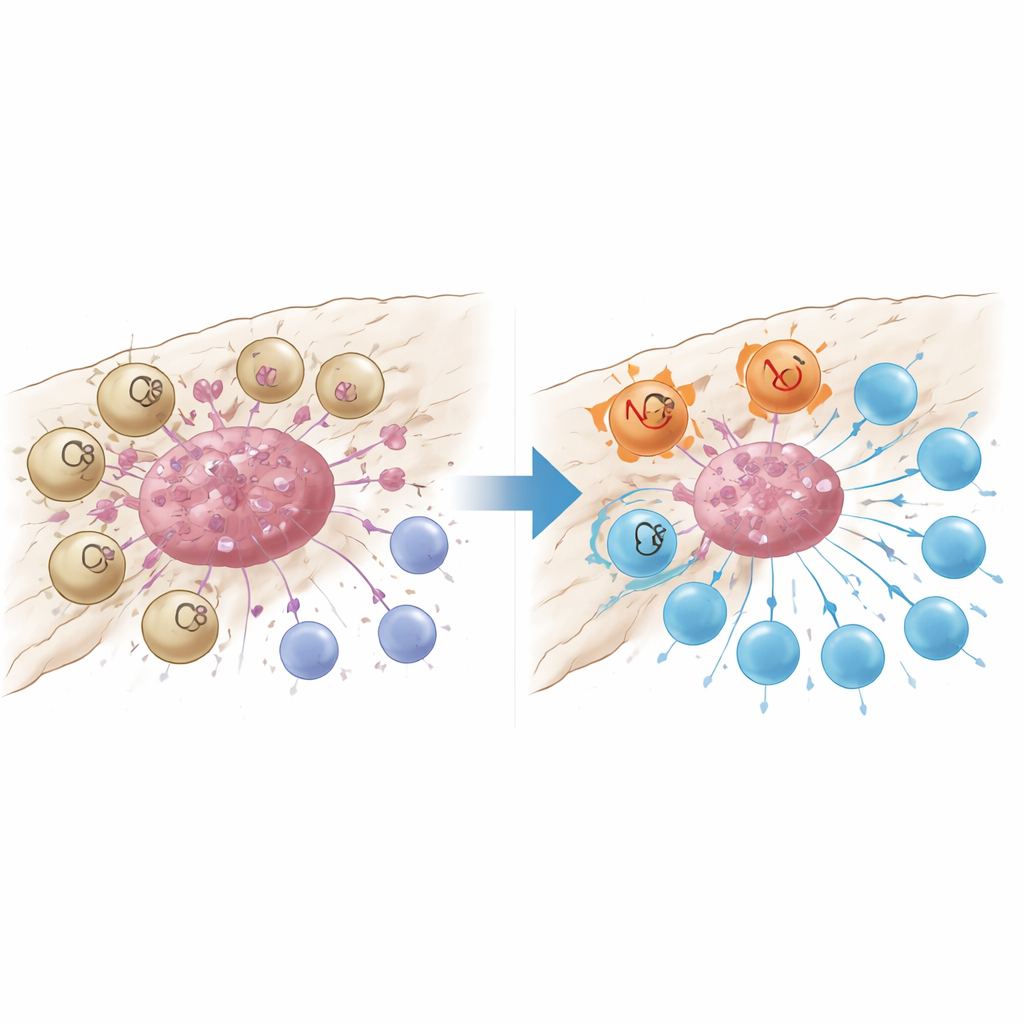
En skadosensor som stänger av T-celler
Närmare analys visade att GPR34-märkta makrofager var tätt samlade inne i tumörnästen och var sällsynta i omgivande normal vävnad eller inflammerad men icke-cancerös pankreas. Patienter vars tumörer innehöll fler av dessa celler hade färre cancerbekämpande CD8 T-celler, fler regulatoriska T-celler som dämpar immuniteten, och kortare överlevnad. I musemodeller där GPR34 saknades enbart i makrofager blev kemoterapi plötsligt mycket mer effektiv: tumörerna krympte mer och T-cellerna inne i tumören var fler och mindre utmattade. Laboratoriestudier med samodling förklarade varför. När makrofager med GPR34 uppfattade molekylära ”fara-signaler” som släpptes ut av döende tumörceller — särskilt ett lipid kallat lysophosphatidylserin — ökade de en process som kallas efferocytos, där de omsluter döda cellfragment. Detta ökade inte bara deras förmåga att ta hand om tumörrester utan aktiverade också lysosomala vägar som bröt ner viktiga molekyler de behöver för att visa tumörantigener för T-celler.
Två sätt att tysta immunsvaret
GPR34-drivna makrofager undergrävde T-celler på ett andra sätt: genom att efter upptag av skadat tumörmaterial frisätta höga nivåer av signalproteinet CXCL16. CXCL16 fungerade som en kronisk stimuleringssignal som pressade CD8 T-celler mot ett utmattat tillstånd där de uttrycker bromsar på ytan och förlorar sin dödande förmåga. Blockering av GPR34 minskade CXCL16-frisättningen, återställde antigenpresentationen på makrofager och återupplivade T-cellernas funktion. Teamet spårade händelsekedjan från signal-lipiden, genom GPR34 och en vanlig tillväxtväg inuti celler, till aktivering av efferocytosmaskineriet och lysosomer. När de farmakologiskt blockerade de nedströms steg som möjliggör upptag eller lysosomal nedbrytning behöll makrofagerna fler av sina antigenvisande molekyler och stödde starkare T-cellsvar, vilket understryker att överaktiv städning paradoxalt kan dölja tumören för immunövervakning.
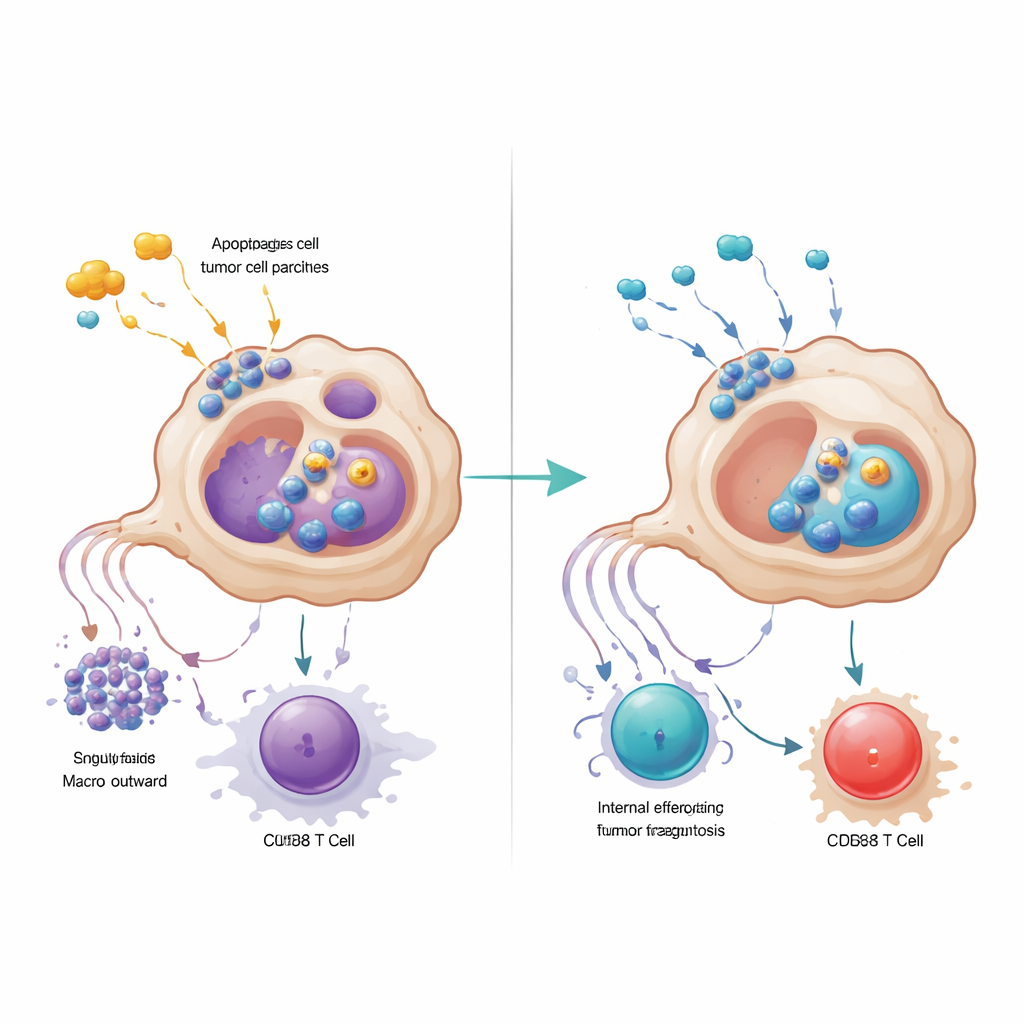
Få befintliga läkemedel att arbeta hårdare
Beväpnade med denna mekanistiska karta testade forskarna en liten molekyl som blockerar GPR34 i flera musemodeller och i patientderiverade tumörorganoider odlade med immunceller. Tillägg av GPR34-antagonisten till kemoterapi och Surufatinib ledde konsekvent till mindre tumörer, mer tumörcelldöd, starkare CD8 T-cellsaktivitet och färre tecken på T-cellsutmattning, utan uppenbar ökad toxicitet i viktiga organ eller i blodvärden. I kontrast reproducerade inte direkt neutralisering av CXCL16 ensam dessa fördelar, vilket betonar att den centrala hävstångspunkten är makrofagens skadosensor och dess påverkan på både efferocytos och antigenpresentation. Enkelt uttryckt antyder studien att vissa makrofager i pankreascancer agerar som överivrade gatustädare som inte bara rensar upp skräp utan också suddar ut de spår immunsystemet behöver. Att stänga av deras GPR34-strömbrytare låter kemoterapiskador exponera tumören istället för att dölja den, och öppnar dörren för mer uthålliga och effektiva behandlingskombinationer.
Citering: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Nyckelord: pankreascancer, tumörmikromiljö, makrofager, immunterapi, Surufatinib