Clear Sky Science · it
Mirare GPR34 nei macrofagi associati al danno potenzia l’immunità anti-tumorale e l’efficacia di Surufatinib nel cancro del pancreas
Perché questo studio è importante
Il cancro del pancreas è uno dei tumori più letali, in parte perché è circondato da una sorta di “campo di forza” immunitario che protegge il tumore dagli attacchi. Questo articolo individua un gruppo chiave di cellule immunitarie che contribuiscono a costruire quella barriera e dimostra che disattivare un singolo interruttore molecolare su queste cellule può rendere molto più efficaci i trattamenti standard. Per i pazienti, questa ricerca indica combinazioni farmacologiche più intelligenti che potrebbero finalmente inclinare la bilancia a favore delle difese dell’organismo.
I collaboratori nascosti intorno al tumore
I tumori del pancreas crescono all’interno di un tessuto affollato di cellule immunitarie e connettivali noto come microambiente tumorale. Tra i residenti più influenti ci sono i macrofagi—globuli bianchi che normalmente rimuovono tessuto morto e aiutano a coordinare la riparazione. Nel cancro del pancreas, questi macrofagi associati al tumore spesso cambiano ruolo, attenuando le risposte immunitarie e contribuendo alla resistenza della neoplasia ai trattamenti. Un farmaco chiamato Surufatinib, già usato in altri tumori, mira a uno dei principali segnali di crescita che mantiene in vita questi macrofagi. Ma il suo impatto nel cancro pancreatico è stato modesto, suggerendo che i macrofagi possono disporre di vie alternative che preservano i loro ruoli protettivi per il tumore.
Seguire singole cellule durante il trattamento
I ricercatori hanno avviato uno studio clinico in cui pazienti con cancro del pancreas hanno ricevuto Surufatinib insieme alla chemioterapia standard prima dell’intervento chirurgico. Utilizzando il sequenziamento dell’RNA a singola cellula—una tecnica che legge l’attività genica in migliaia di singole cellule—hanno mappato tutti i tipi cellulari nei tumori asportati e confrontato i pazienti che rispondevano al trattamento con quelli i cui tumori continuavano a crescere. I non responder presentavano molti più macrofagi in generale, e un sottotipo in particolare dominava. Queste cellule esprimevano alti livelli di un recettore chiamato GPR34 e mostravano programmi genici legati alle risposte al danno tissutale, alla pulizia dei rifiuti e alla creazione di un ambiente immunosoppressivo. Allo stesso tempo, i tumori dei non responder contenevano più cellule T citotossiche “esauste” che avevano perso la capacità di attaccare efficacemente le cellule tumorali.
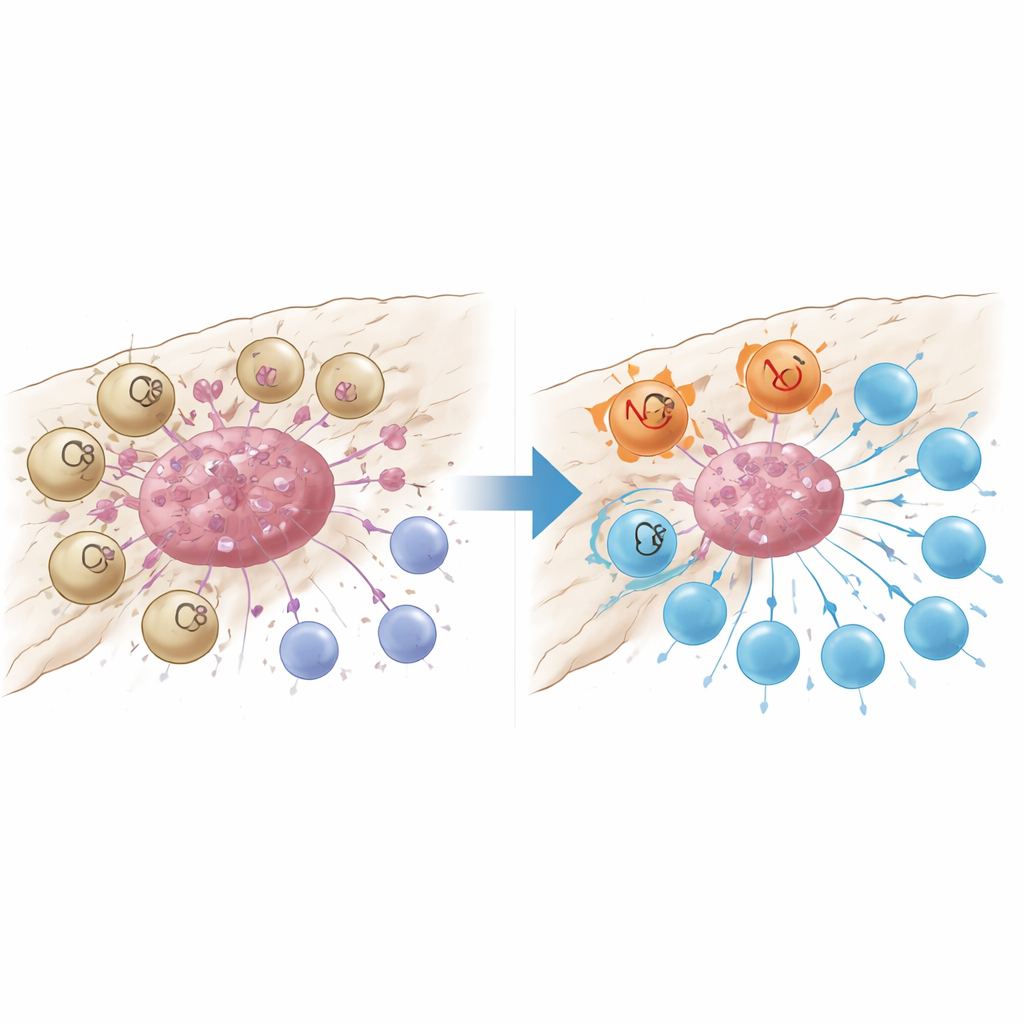
Un sensore del danno che spegne le cellule T
Un’analisi più approfondita ha rivelato che i macrofagi marcati da GPR34 erano strettamente raggruppati all’interno degli agglomerati tumorali e rari nel tessuto normale circostante o nel pancreas infiammato ma non canceroso. I pazienti i cui tumori contenevano più di queste cellule avevano meno cellule CD8 che combattono il cancro, più cellule T regolatorie che limitano l’immunità e tempi di sopravvivenza più brevi. In modelli murini ingegnerizzati per essere privi di GPR34 soltanto nei macrofagi, la chemioterapia è diventata improvvisamente molto più efficace: i tumori si sono ridotti di più e le cellule T all’interno del tumore erano più numerose e meno esauste. Esperimenti in coltura co-cultivando le cellule hanno mostrato il perché. Quando i macrofagi con GPR34 percepivano segnali molecolari di “pericolo” rilasciati dalle cellule tumorali morenti—in particolare un lipide chiamato lisofosfatidilserina—potenziavano un processo chiamato efferocitosi, in cui inglobano i frammenti delle cellule morte. Questo non solo aumentava la loro capacità di eliminare i detriti tumorali ma attivava anche vie lisosomiali interne che degradavano molecole chiave necessarie per presentare gli antigeni tumorali alle cellule T.
Due modi per silenziare l’attacco immunitario
I macrofagi guidati da GPR34 indebolivano le cellule T in un secondo modo: secernendo alti livelli della proteina di segnalazione CXCL16 dopo aver captato materiale tumorale danneggiato. CXCL16 agiva come un segnale di stimolazione cronica, spingendo le cellule CD8 verso uno stato di esaurimento in cui esprimono freni sulla loro superficie e perdono potere citotossico. Bloccare GPR34 riduceva il rilascio di CXCL16, ristabiliva la presentazione degli antigeni sui macrofagi e rivitalizzava la funzione delle cellule T. Il team ha tracciato la catena di eventi dal lipide segnale di danno, attraverso GPR34 e una comune via di crescita intracellulare, fino all’attivazione della macchina dell’efferocitosi e dei lisosomi. Quando hanno bloccato farmacologicamente i passaggi successivi dell’inglobamento o dei lisosomi, i macrofagi mantenevano più molecole di presentazione dell’antigene e favorivano risposte T più potenti, sottolineando che una pulizia eccessiva può paradossalmente nascondere il tumore alla sorveglianza immunitaria.
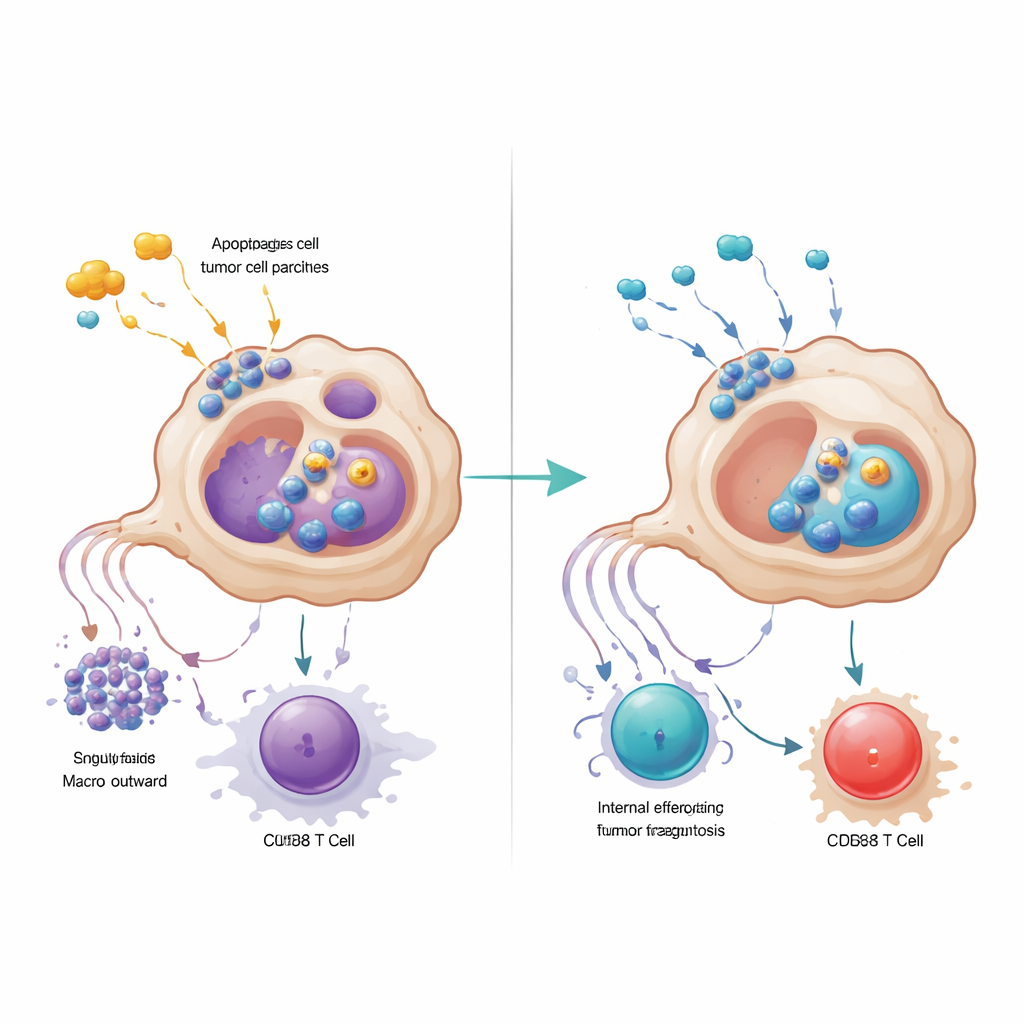
Far lavorare di più i farmaci esistenti
Dotati di questa mappa meccanicistica, i ricercatori hanno testato un piccolo inibitore molecolare di GPR34 in diversi modelli murini e in organoidi tumorali derivati da pazienti coltivati con cellule immunitarie. L’aggiunta dell’antagonista di GPR34 alla chemioterapia e a Surufatinib ha portato costantemente a tumori più piccoli, maggiore morte delle cellule tumorali, attività più forte delle cellule T CD8 e minori segnali di esaurimento delle cellule T, senza tossicità aggiuntiva evidente nei principali organi o nei parametri ematici. Al contrario, neutralizzare direttamente CXCL16 da solo non ha riprodotto questi benefici, evidenziando che il punto di leva centrale è il sensore di danno dei macrofagi e il suo impatto sia sull’efferocitosi sia sulla presentazione dell’antigene. In termini semplici, lo studio suggerisce che alcuni macrofagi nel cancro del pancreas agiscono come zelanti spazzini di strada che non solo rimuovono i detriti ma cancellano anche gli indizi di cui il sistema immunitario ha bisogno. Spegnere il loro interruttore GPR34 permette al danno indotto dalla chemioterapia di esporre il tumore anziché nasconderlo, aprendo la strada a combinazioni di trattamento più durature ed efficaci.
Citazione: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Parole chiave: cancro del pancreas, microambiente tumorale, macrofagi, immunoterapia, Surufatinib