Clear Sky Science · de
Gezielte Abschaltung von GPR34 in schadenassoziierten Makrophagen verstärkt die Anti-Tumor-Immunität und die Wirksamkeit von Surufatinib bei Bauchspeicheldrüsenkrebs
Warum diese Studie wichtig ist
Bauchspeicheldrüsenkrebs gehört zu den tödlichsten Krebserkrankungen, unter anderem weil er von einem immunologischen „Kraftfeld“ umgeben ist, das den Tumor vor Angriffen schützt. Diese Arbeit identifiziert eine entscheidende Gruppe von Immunzellen, die beim Aufbau dieses Schildes helfen, und zeigt, dass das Deaktivieren eines einzelnen molekularen Schalters auf diesen Zellen Standardtherapien deutlich wirksamer machen kann. Für Patientinnen und Patienten weist die Forschung auf intelligentere Wirkstoffkombinationen hin, die letztlich das Gleichgewicht zugunsten der körpereigenen Abwehr verschieben könnten.
Die verborgenen Helfer rund um den Tumor
Bauchspeicheldrüsentumoren wachsen in einer dicht besiedelten Nachbarschaft aus Immun- und Bindegewebe, dem tumorösen Mikroumfeld. Zu den einflussreichsten Bewohnern gehören Makrophagen – weiße Blutkörperchen, die normalerweise abgestorbenes Gewebe beseitigen und die Reparatur koordinieren. Bei Bauchspeicheldrüsenkrebs wechseln diese tumorassoziierten Makrophagen häufig die Seiten, dämpfen Immunantworten und helfen dem Krebs, Therapien zu widerstehen. Ein Wirkstoff namens Surufatinib, der bereits bei anderen Krebsarten eingesetzt wird, zielt auf eines der Hauptwachstumssignale, das diese Makrophagen am Leben erhält. Seine Wirkung beim Bauchspeicheldrüsenkrebs war jedoch verhalten, was darauf hindeutet, dass Makrophagen Ausweichwege besitzen, die ihre tumorschützenden Funktionen bewahren.
Einzelzellenverfolgung während der Therapie
Die Forschenden starteten eine klinische Studie, in der Menschen mit Bauchspeicheldrüsenkrebs vor der Operation Surufatinib zusammen mit Standardchemotherapie erhielten. Mithilfe der Einzelzell-RNA-Sequenzierung – einer Methode, die die Genaktivität von Tausenden einzelner Zellen liest – kartierten sie alle Zelltypen in den entfernten Tumoren und verglichen Patientinnen und Patienten, die auf die Behandlung ansprachen, mit denen, deren Tumoren weiter wuchsen. Nichtansprechende Tumoren wiesen insgesamt deutlich mehr Makrophagen auf, und ein Subtyp dominierte besonders. Diese Zellen trugen hohe Mengen eines Rezeptors namens GPR34 und zeigten Genprogramme, die mit Gewebeschadensantworten, Abfallbeseitigung und der Schaffung eines immunsuppressiven Umfelds verknüpft sind. Gleichzeitig enthielten Tumoren von Nichtansprechern mehr erschöpfte, „ausgebrannte“ T-Killerzellen, die ihre Fähigkeit verloren hatten, Krebszellen effizient anzugreifen.
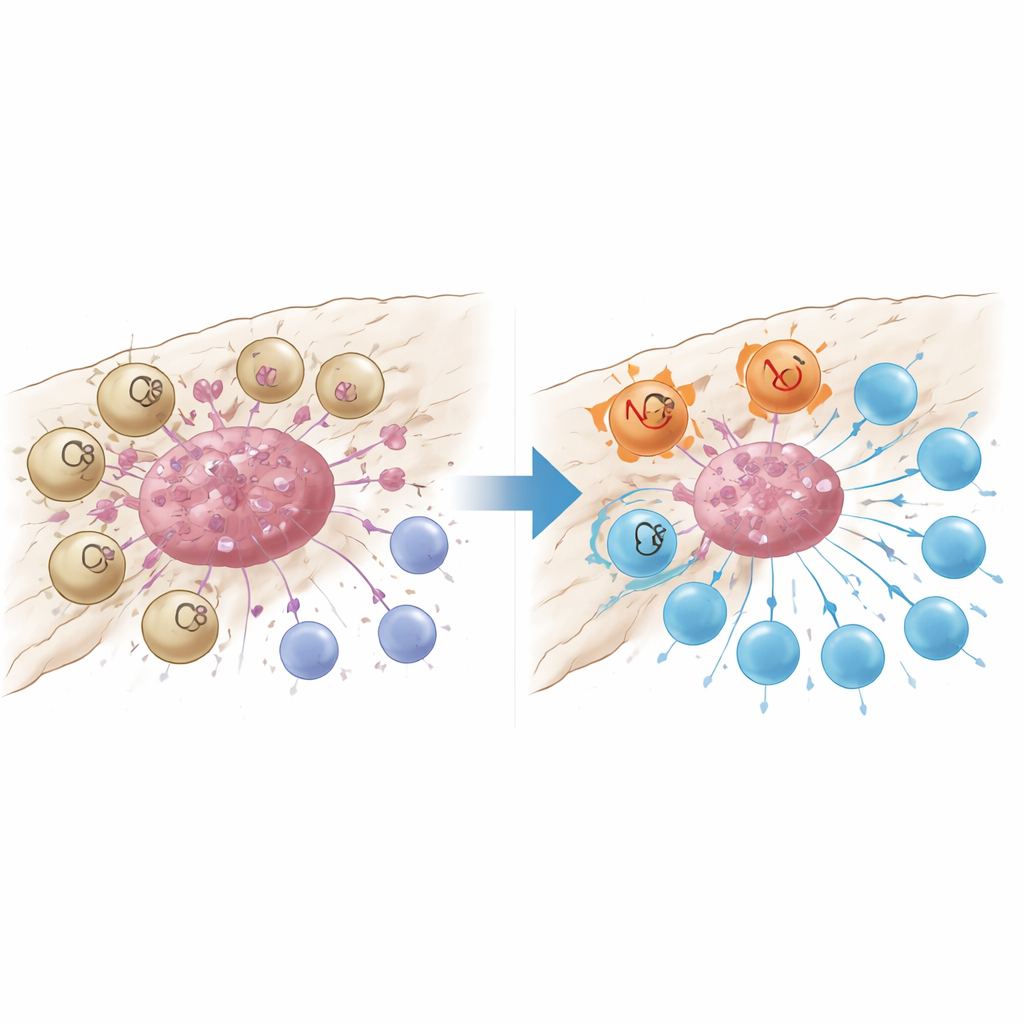
Ein Schadenssensor, der T‑Zellen ausschaltet
Genauere Analysen zeigten, dass GPR34-markierte Makrophagen dicht in Tumornestern konzentriert waren und in angrenzendem normalem Gewebe oder entzündetem, aber nicht krebsigem Pankreas selten vorkamen. Patientinnen und Patienten, deren Tumoren mehr dieser Zellen enthielten, hatten weniger krebsbekämpfende CD8-T-Zellen, mehr regulatorische T-Zellen, die die Immunantwort dämpfen, und kürzere Überlebenszeiten. In Mausmodellen, die so gezüchtet wurden, dass GPR34 nur in Makrophagen fehlte, wurde Chemotherapie plötzlich deutlich wirksamer: Die Tumoren schrumpften stärker, und im Tumor waren mehr T-Zellen zu finden, die weniger erschöpft waren. Zellkultur-Co-Kultur-Experimente erklärten das Warum: Wenn GPR34-exprimierende Makrophagen molekulare „Gefahrensignale“ aus sterbenden Tumorzellen wahrnahmen – insbesondere ein Lipid namens Lysophosphatidylserin – erhöhten sie einen Prozess namens Efferocytose, bei dem sie tote Zellfragmente aufnehmen. Das steigerte nicht nur ihre Fähigkeit, Tumorreste zu verschlingen, sondern löste auch lysosomale Abbauwege aus, die zentrale Moleküle zerstörten, die sie benötigen, um Tumorantigene T‑Zellen zu präsentieren.
Zwei Wege, die Immunattacke stummzuschalten
GPR34-getriebene Makrophagen untergruben T‑Zellen auf eine zweite Weise: Sie schütteten nach der Aufnahme von beschädigtem Tumormaterial hohe Mengen des Signalproteins CXCL16 aus. CXCL16 wirkte als chronisches Stimulationssignal und trieb CD8-T-Zellen in einen erschöpften Zustand, in dem sie Bremsen auf ihrer Oberfläche exprimieren und ihre Tötungskraft verlieren. Die Blockade von GPR34 reduzierte die Freisetzung von CXCL16, stellte die Antigenpräsentation auf Makrophagen wieder her und belebte die T‑Zellfunktionen. Das Team verfolgte die Ereigniskette vom Schadenssignal-Lipid über GPR34 und einen häufigen Wachstumsweg innerhalb der Zelle bis zur Aktivierung der Efferocytose-Maschinerie und der Lysosomen. Wenn sie pharmakologisch die nachgeschalteten Schritte der Aufnahme oder der lysosomalen Verarbeitung hemmten, behielten Makrophagen mehr ihrer antigenpräsentierenden Moleküle und unterstützten kräftigere T‑Zellantworten, was verdeutlicht, dass übertriebene Aufräumaktivität paradoxerweise den Tumor vor der immunologischen Überwachung verbergen kann.
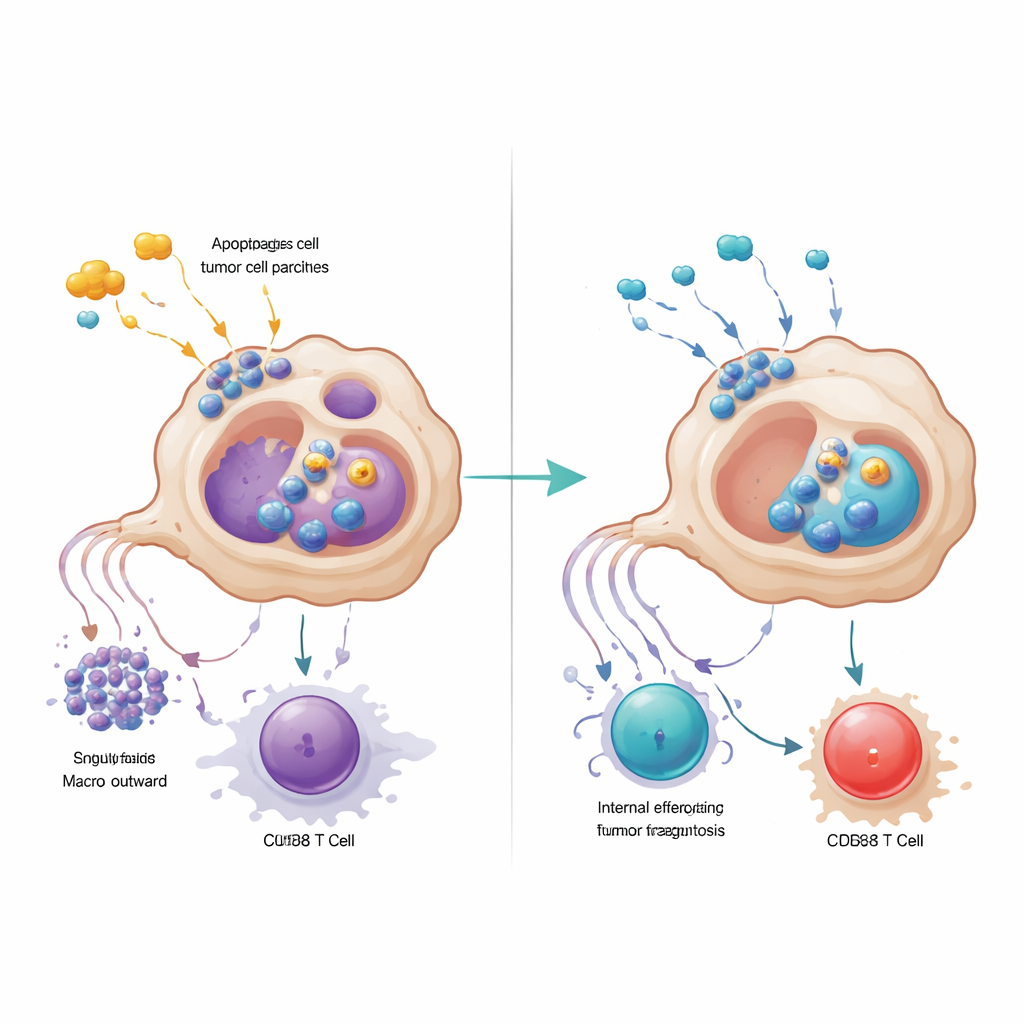
Bestehende Medikamente wirksamer machen
Mit dieser mechanistischen Karte testeten die Forschenden einen kleinen GPR34‑Inhibitor in mehreren Mausmodellen und in patientenabgeleiteten Tumororganoiden, die mit Immunzellen kultiviert wurden. Das Hinzufügen des GPR34‑Antagonisten zur Chemotherapie und zu Surufatinib führte durchgängig zu kleineren Tumoren, mehr Tumorzellsterben, stärkerer CD8-T‑Zell‑Aktivität und weniger Anzeichen von T‑Zell‑Erschöpfung, ohne offensichtliche zusätzliche Toxizität in wichtigen Organen oder Blutbildern. Dagegen reproduzierte die direkte Neutralisierung von CXCL16 allein diese Vorteile nicht, was hervorhebt, dass der zentrale Hebel der Schadenssensor der Makrophagen und sein Einfluss auf sowohl Efferocytose als auch Antigenpräsentation ist. Einfach ausgedrückt legt die Studie nahe, dass einige Makrophagen bei Bauchspeicheldrüsenkrebs wie übermotivierte Straßenreiniger agieren, die nicht nur Schutt beseitigen, sondern auch die Hinweise tilgen, die das Immunsystem benötigt. Das Abschalten ihres GPR34‑Schalters lässt zu, dass durch Chemotherapie verursachter Schaden den Tumor offenlegt statt ihn zu verbergen, und ebnet den Weg für dauerhaftere und effektivere Behandlungskombinationen.
Zitation: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Schlüsselwörter: Bauchspeicheldrüsenkrebs, tumoröses Mikroumfeld, Makrophagen, Immuntherapie, Surufatinib