Clear Sky Science · ja
損傷関連マクロファージのGPR34を標的にすることが膵臓がんにおける抗腫瘍免疫とスルファチニブの有効性を高める
この研究が重要な理由
膵臓がんは最も致死率の高いがんのひとつであり、その一因は腫瘍を外敵から遮断する免疫の「防護膜」に包まれていることにあります。本論文はその防護膜を形成する重要な免疫細胞群を明らかにし、これらの細胞上の単一の分子スイッチを無効化することで標準治療の効果が大幅に改善することを示しています。患者にとっては、これが体自身の防御力を有利に傾けるより賢い薬剤併用戦略への道を示唆します。
腫瘍の周囲にいる隠れた助っ人たち
膵臓腫瘍は、免疫細胞や結合組織細胞が密に詰まった腫瘍微小環境の中で成長します。そこでもっとも影響力のある住人の一つがマクロファージです。マクロファージは通常、死んだ組織の掃除や修復の調整を行いますが、膵臓がんでは腫瘍関連マクロファージがしばしば役割を変え、免疫応答を抑制しがんの治療抵抗性に寄与します。スルファチニブという薬は、これらマクロファージの生存を支える主要な成長シグナルの一つを標的とする既存薬ですが、膵臓がんでの効果は限定的であり、マクロファージには腫瘍保護的役割を維持する代替経路が存在することが示唆されます。
治療中の個々の細胞を追う
研究者たちは、膵臓がん患者に術前化学療法とともにスルファチニブを投与する臨床試験を行いました。単一細胞RNAシーケンシング──数千個の個々の細胞の遺伝子発現を読む手法──を用いて摘出された腫瘍内の全細胞種をマッピングし、治療に反応した患者と腫瘍が増悪し続けた患者とを比較しました。非応答者ではマクロファージの総数が多く、特にあるサブタイプが優勢でした。これらの細胞はGPR34という受容体を高発現し、組織損傷応答、廃棄物処理、免疫抑制環境の形成に関連する遺伝子プログラムを示していました。同時に、非応答腫瘍は効率的にがん細胞を攻撃する能力を失った“疲弊”した細胞傷害性T細胞をより多く含んでいました。
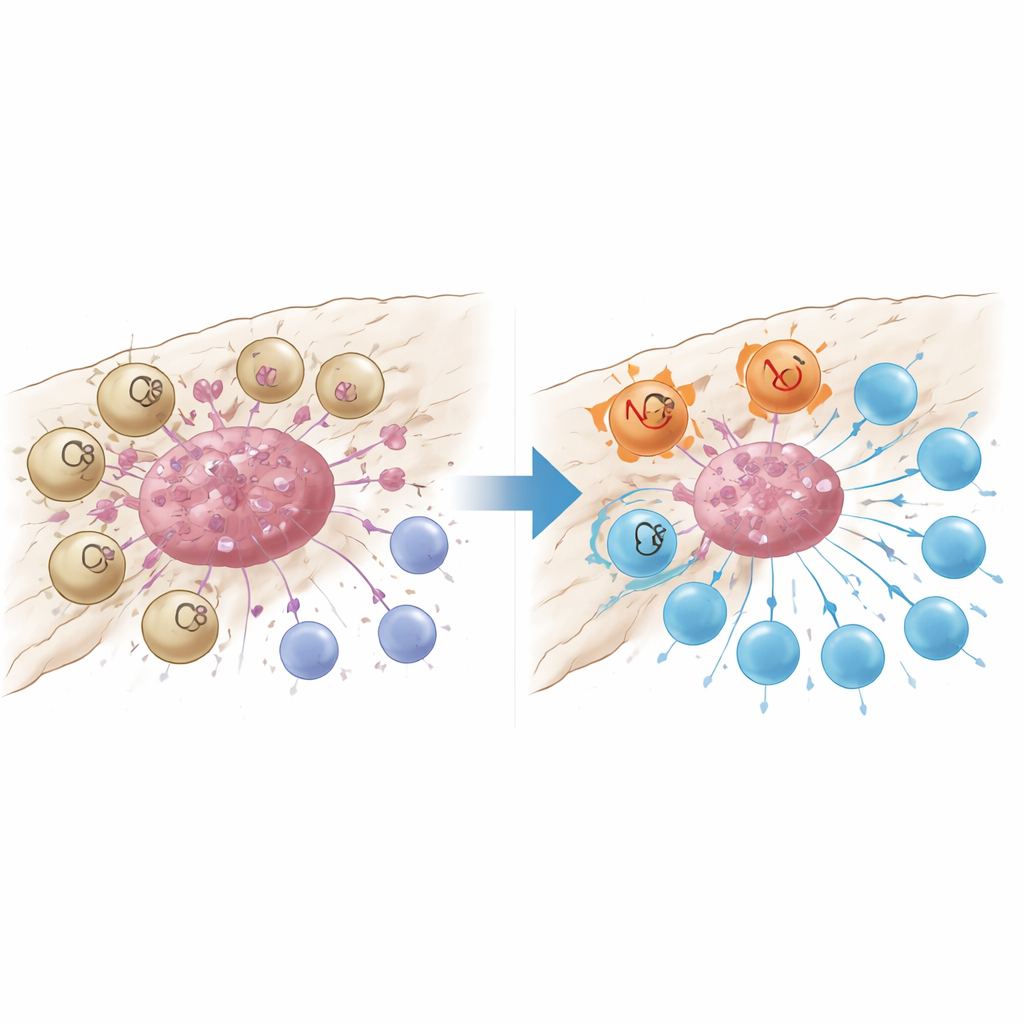
T細胞をオフにする損傷センサー
詳細解析により、GPR34で標識されるマクロファージは腫瘍巣内に密集しており、周囲の正常組織や炎症のある非がん性膵臓にはほとんど見られないことが明らかになりました。これらの細胞が多い患者はがんと闘うCD8陽性T細胞が少なく、免疫を抑える制御性T細胞が多く、予後も短い傾向がありました。マクロファージでのみGPR34が欠損するように設計したマウスモデルでは、化学療法の効果が突然大きく向上しました:腫瘍はより縮小し、腫瘍内のT細胞は数が増え疲弊が減りました。培養での共培養実験はその理由を示します。GPR34を持つマクロファージが、特にリゾホスファチジルセリンという脂質など死にゆく腫瘍細胞から放出される“危険信号”を感知すると、エフェロサイトーシスと呼ばれる死細胞断片の貪食プロセスを活性化します。これにより腫瘍残骸を取り込む能力が高まるだけでなく、腫内で抗原をT細胞に提示するために必要な主要な分子を分解するリソソーム経路が内部で作動します。
免疫攻撃を沈黙させる2つの方法
GPR34駆動のマクロファージは、ダメージを取り込むことでもう一つの方法でもT細胞を弱めました:損傷腫瘍物質を取り込んだ後にシグナル蛋白質CXCL16を高レベルで分泌することです。CXCL16は持続的な刺激シグナルとして働き、CD8 T細胞を表面にブレーキ分子を発現し殺傷力を失った疲弊状態へ押し込んでしまいます。GPR34を遮断するとCXCL16放出が減り、マクロファージの抗原提示が回復し、T細胞機能が再活性化されました。研究チームは、損傷信号脂質からGPR34、細胞内の共通の増殖経路を経てエフェロサイトーシス装置とリソソームの活性化に至るまでの一連の出来事をたどりました。下流の貪食やリソソーム工程を薬理学的に阻害すると、マクロファージは抗原提示分子をより多く保持し、より強力なT細胞応答を支持し続けました。これは過剰な掃除が逆に腫瘍を免疫監視から隠してしまうことを強調する結果です。
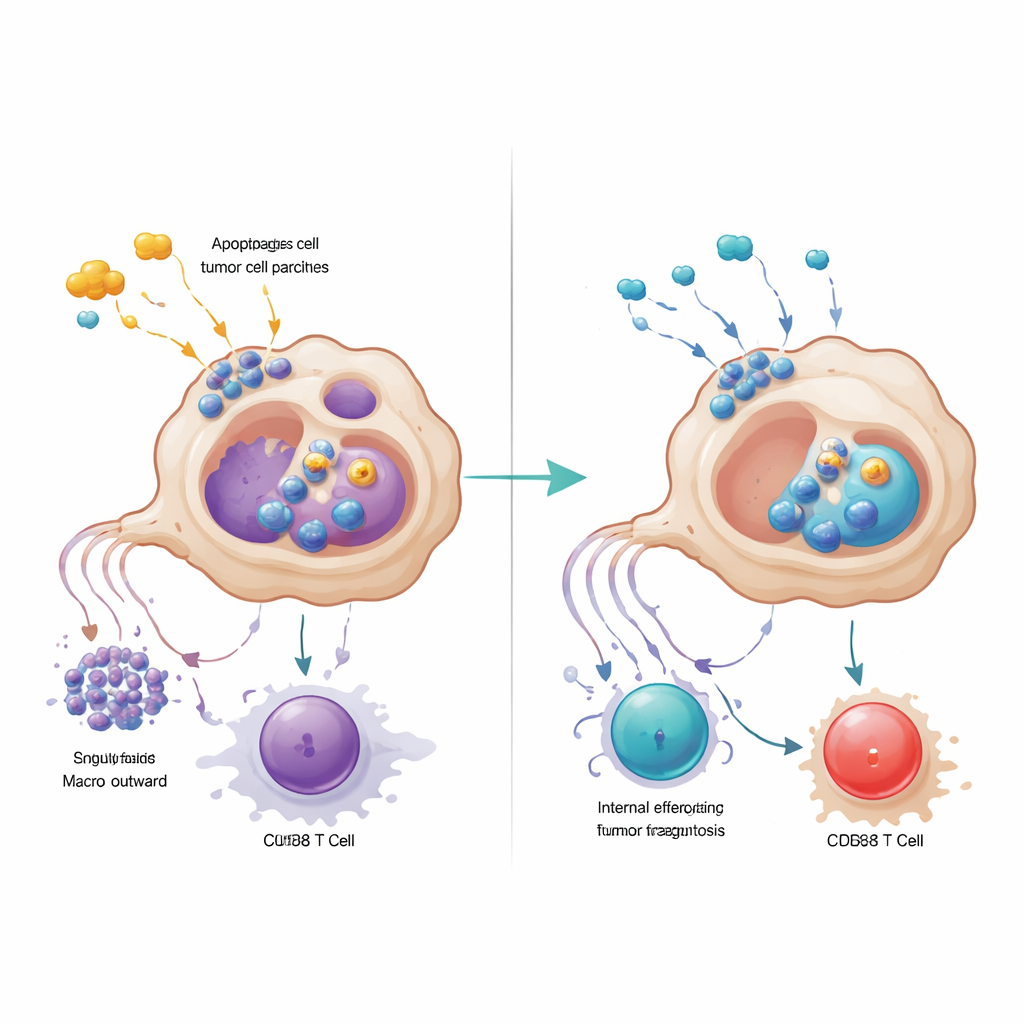
既存薬の効果を高める
この機序地図を基に、研究者たちは小分子のGPR34阻害剤を複数のマウスモデルと免疫細胞を伴って培養した患者由来腫瘍オルガノイドで試験しました。GPR34拮抗薬を化学療法およびスルファチニブに加えると、一貫して腫瘍が小さくなり、腫瘍細胞死が増え、CD8 T細胞活性が強まり、T細胞疲弊の兆候が減少しました。主要な臓器や血算で明白な追加毒性は観察されませんでした。対照的にCXCL16を単独で中和してもこれらの利益は再現されず、中心的なテコはマクロファージの損傷センサーとそれがエフェロサイトーシスと抗原提示の両方に及ぼす影響であることが示されました。平たく言えば、本研究は膵臓がんの一部のマクロファージが過熱した街頭掃除係のように働き、残骸を除去するだけでなく免疫が必要とする手がかりも消してしまうことを示しています。彼らのGPR34スイッチを切ることで、化学療法による損傷は腫瘍を隠すのではなく露出させるようになり、より持続的で効果的な治療の組み合わせへの道が開かれます。
引用: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
キーワード: 膵臓がん, 腫瘍微小環境, マクロファージ, 免疫療法, スルファチニブ