Clear Sky Science · tr
Hasarla ilişkili makrofajlarda GPR34 hedeflenmesi pankreas kanserinde anti-tümör bağışıklığını ve Surufatinib etkinliğini artırır
Bu çalışma neden önemli
Pankreas kanseri, kısmen tümörü saldırılardan koruyan bir bağışıklık “kalkanı” ile çevrili olması nedeniyle en ölümcül kanserlerden biridir. Bu makale, o kalkanın inşasına yardımcı olan önemli bir bağışıklık hücresi grubunu ortaya koyuyor ve bu hücrelerdeki tek bir moleküler anahtarı devre dışı bırakmanın standart tedavilerin etkinliğini önemli ölçüde artırabileceğini gösteriyor. Hastalar açısından bu araştırma, nihayetinde vücudun kendi savunma mekanizmalarının lehine dengeyi değiştirebilecek daha akıllı ilaç kombinasyonlarına işaret ediyor.
Tümör çevresindeki görünmez yardımcılar
Pankreas tümörleri, tümör mikroçevresi olarak bilinen, bağışıklık ve bağ dokusu hücreleriyle dolu bir ortam içinde büyür. En etkili sakinlerden biri makrofajlardır—normalde ölü dokuyu temizleyen ve onarıma yardımcı olan beyaz kan hücreleri. Pankreas kanserinde, tümör ilişkili makrofajlar sıklıkla tavır değiştirir, bağışıklık yanıtlarını zayıflatır ve kanserin tedaviye direnmesine yardımcı olurlar. Halihazırda diğer kanserlerde kullanılan Surufatinib adlı bir ilaç, bu makrofajları canlı tutan ana büyüme sinyallerinden birini hedefler. Ancak pankreas kanserindeki etkisi sınırlı kaldı; bu da makrofajların tümörü koruyucu rollerini sürdürebilmek için yedek yolları olabileceğini düşündürüyor.
Tedavi sırasında tek tek hücreleri izlemek
Araştırmacılar, pankreas kanserli kişilere cerrahi öncesi standart kemoterapi ile birlikte Surufatinib verildiği bir klinik çalışma başlattılar. Tek hücre RNA dizileme—binlerce bireysel hücredeki gen aktivitesini okuyan bir teknik—kullanarak çıkarılan tümörlerdeki tüm hücre tiplerini haritaladılar ve tedaviye yanıt veren hastaları tümörleri büyümeye devam edenlerle karşılaştırdılar. Yanıt vermeyenlerde genel olarak çok daha fazla makrofaj vardı ve özellikle bir alt tip baskındı. Bu hücreler GPR34 adlı bir reseptörü yüksek düzeyde taşıyor ve doku hasarı yanıtları, atık temizleme ve immün-supresif bir ortam yaratma ile ilişkili gen programlarını gösteriyordu. Aynı zamanda, yanıt vermeyen hastaların tümörlerinde verimli bir şekilde kanseri hedefleme yeteneğini kaybetmiş tükenmiş “exhausted” öldürücü T hücreleri daha fazlaydı.
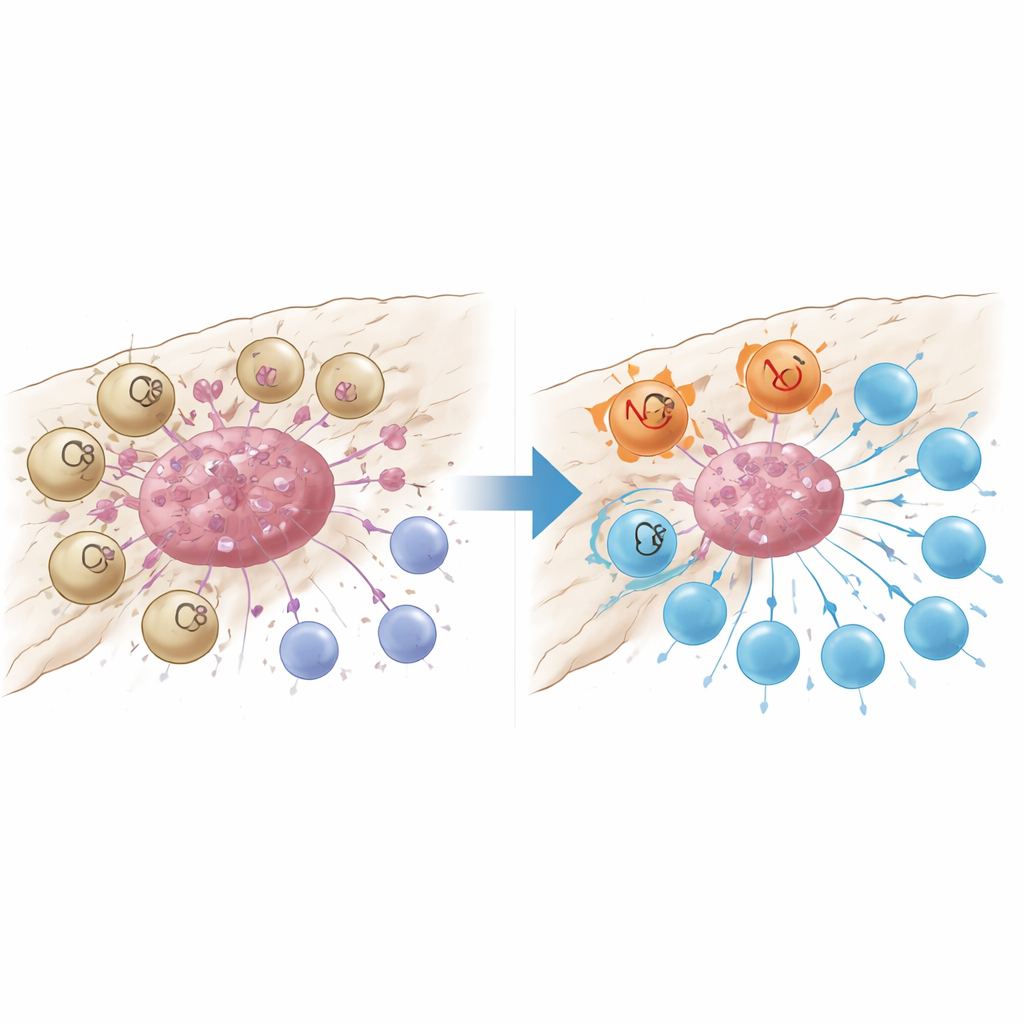
T hücrelerini kapatan bir hasar sensörü
Daha ayrıntılı analiz, GPR34 ile işaretlenmiş makrofajların tümör yuvaları içinde sıkı kümeler halinde olduğunu ve çevreleyen normal dokuda veya iltihaplı fakat kansersiz pankreasta nadir bulunduğunu ortaya koydu. Tümörlerinde daha fazla bu hücreye sahip hastalarda, daha az kanserle savaşan CD8 T hücresi, bağışıklığı sınırlayan daha fazla düzenleyici T hücresi ve daha kısa sağkalım süreleri izlendi. Makrofajlarda yalnızca GPR34 eksik olacak şekilde tasarlanmış fare modellerinde kemoterapi aniden çok daha etkili hale geldi: tümörler daha fazla küçüldü ve tümör içindeki T hücreleri daha çok sayıda ve daha az tükenmiş oldu. Laboratuvar eş-kültür deneyleri nedenini gösterdi. GPR34 taşıyan makrofajlar, özellikle lizofosfatidilserin adı verilen bir lipid olmak üzere ölen tümör hücreleri tarafından salınan moleküler “tehlike sinyallerini” algıladıklarında, artıkları yutan efferocytosis adı verilen bir süreci artırdılar. Bu sadece tümör artıklarını yutma yeteneklerini artırmakla kalmadı, aynı zamanda T hücrelerine sunacakları tümör antijenlerini göstermek için ihtiyaç duydukları bazı anahtar molekülleri parçalayan lizozomal yolları da tetikledi.
Bağışıklık saldırısını susturmanın iki yolu
GPR34 kaynaklı makrofajlar T hücrelerini ikinci bir yolla da zayıflattı: hasarlı tümör materyalini aldıktan sonra yüksek düzeyde CXCL16 adlı sinyal proteini salgılıyordu. CXCL16, CD8 T hücrelerini yüzeylerinde frenler (inhibitörler) ifade eden ve öldürme gücünü kaybettiren bir tükenmişlik durumuna iten kronik bir uyarı sinyali olarak işledi. GPR34'ü bloke etmek CXCL16 salınımını azaltıyor, makrofajlardaki antijen sunumunu geri getiriyor ve T hücre fonksiyonunu canlandırıyordu. Ekip, hasar sinyali lipidinden GPR34 ve hücre içindeki yaygın bir büyüme yoluna, oradan da efferocytosis mekanizması ve lizozom aktivasyonuna kadar olay zincirini izledi. Aşağı akıştaki yutma ya da lizozomal adımları farmakolojik olarak bloke ettiklerinde, makrofajlar daha fazla antijen gösteren molekülünü korudu ve daha güçlü T hücre yanıtlarını destekledi; bu da aşırı temizlik aktivitesinin paradoksal olarak tümörü bağışıklık gözetiminden gizleyebileceğini vurguladı.
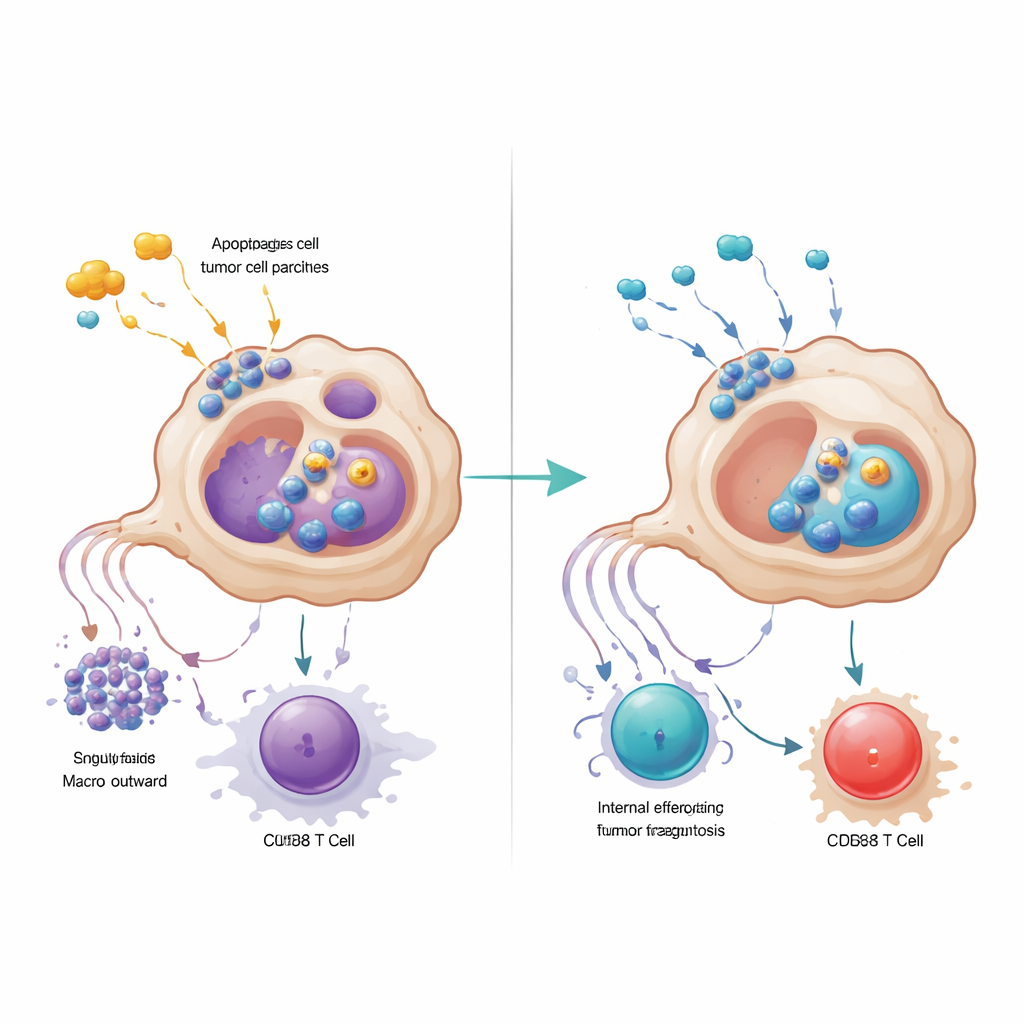
Mevcut ilaçların etkinliğini artırmak
Bu mekanistik harita ile donanmış olarak araştırmacılar, birkaç fare modelinde ve bağışıklık hücreleri ile birlikte yetiştirilen hasta kaynaklı tümör organoidlerinde küçük moleküllü bir GPR34 blokerini test ettiler. GPR34 antagonisti kemoterapi ve Surufatinib ile birlikte eklendiğinde, tutarlı şekilde daha küçük tümörler, daha fazla tümör hücresi ölümü, daha güçlü CD8 T hücre aktivitesi ve T hücre tükenmişliğine dair daha az belirti görüldü; ana organlarda veya kan sayımlarında belirgin ek toksisite gözlemlenmedi. Buna karşılık, yalnızca CXCL16’yı doğrudan nötralize etmek bu faydaları tekrarlamadı; bu da merkezi kaldıraç noktasının makrofaj hasar sensörü ve bunun hem efferocytosis hem de antijen sunumu üzerindeki etkisi olduğunu gösteriyor. Basitçe söylemek gerekirse, çalışma pankreas kanserindeki bazı makrofajların sadece döküntüleri temizlemekle kalmayıp bağışıklık sisteminin ihtiyaç duyduğu ipuçlarını da silen aşırı hevesli sokak süpürücüler gibi davrandığını öne sürüyor. Onların GPR34 anahtarını kapatmak, kemoterapinin yol açtığı hasarın tümörü gizlemek yerine açığa çıkarmasına izin veriyor ve daha kalıcı ve etkili tedavi kombinasyonlarına kapı aralıyor.
Atıf: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Anahtar kelimeler: pankreas kanseri, tümör mikroçevresi, makrofajlar, immünoterapi, Surufatinib