Clear Sky Science · nl
Het richten op GPR34 in schade-geassocieerde macrofagen versterkt anti-tumorimmuniteit en de werkzaamheid van Surufatinib bij alvleesklierkanker
Waarom deze studie ertoe doet
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker, deels omdat de tumor omgeven is door een immuun "krachtveld" dat de kanker beschermt tegen aanvallen. Dit artikel onthult een belangrijke groep immuuncellen die helpen dit schild op te bouwen en toont aan dat het uitschakelen van één moleculaire schakelaar op die cellen standaardtherapieën veel effectiever kan maken. Voor patiënten wijst dit onderzoek op slimere medicijncombinaties die uiteindelijk het tij in het voordeel van het eigen afweersysteem kunnen doen keren.
De verborgen helpers rond de tumor
Alvleeskliertumoren groeien in een dichtbevolkte omgeving van immuun- en bindweefselcellen, bekend als de tumormicro-omgeving. Een van de meest invloedrijke bewoners zijn macrofagen—witte bloedcellen die normaal gesproken dode weefsels opruimen en helpen bij herstel. Bij alvleesklierkanker slaan tumorgeassocieerde macrofagen vaak om naar de andere kant: ze dempen immuunreacties en helpen de tumor resistent te zijn tegen behandeling. Een medicijn genaamd Surufatinib, dat al gebruikt wordt bij andere kankers, richt zich op één van de belangrijkste groeisignalen die deze macrofagen in leven houdt. Maar het effect bij alvleesklierkanker is tot nu toe bescheiden, wat suggereert dat macrofagen alternatieve routes hebben die hun tumorbeschermende rol in stand houden.
Individuele cellen volgen tijdens behandeling
De onderzoekers startten een klinische proef waarin mensen met alvleesklierkanker Surufatinib kregen samen met standaard chemotherapie vóór de operatie. Met single-cell RNA-sequencing—een techniek die genactiviteit leest in duizenden individuele cellen—braken ze alle celtypen in de verwijderde tumoren in kaart en vergeleken patiënten die op de behandeling reageerden met patiënten van wie de tumor bleef groeien. Niet-responderende patiënten hadden over het geheel genomen veel meer macrofagen, en één subtyp domineerde in het bijzonder. Deze cellen droegen hoge niveaus van een receptor genaamd GPR34 en lieten genprogramma’s zien die gekoppeld zijn aan weefselschade, afvalopruiming en het creëren van een immuunsuppressieve omgeving. Tegelijkertijd bevatten tumoren van niet-responders meer uitgeputte, "exhausted" cytotoxische T-cellen (killer T-cellen) die hun vermogen om efficiënt kankercellen aan te vallen hadden verloren.
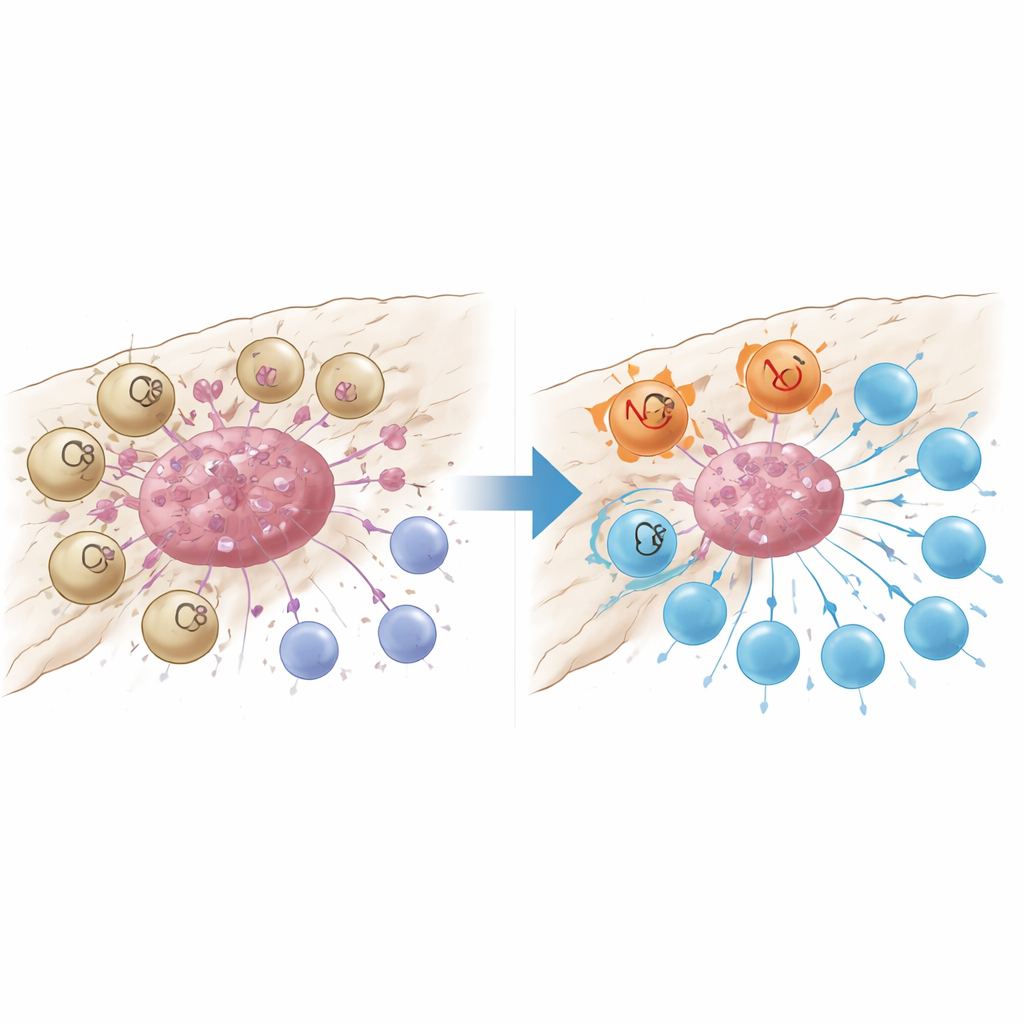
Een schade-sensor die T-cellen uitschakelt
Nadere analyse toonde aan dat GPR34-gemarkeerde macrofagen dicht gegroepeerd zaten binnen tumorclusters en zeldzaam waren in omliggend normaal weefsel of in ontstoken maar niet-kankerrijk pancreasweefsel. Patiënten met meer van deze cellen in hun tumor hadden minder kankervijandige CD8-T-cellen, meer regulerende T-cellen die de immuniteit remmen, en een kortere overleving. In muismodellen die zo werden gefokt dat GPR34 alleen in macrofagen ontbrak, werd chemotherapie plots veel effectiever: tumoren krimpten sterker en er waren meer, minder uitgeputte T-cellen in de tumor. Laboratorium co-cultuurexperimenten lieten zien waarom. Wanneer macrofagen met GPR34 moleculaire "gevaarssignalen" voelden die vrijkomen uit stervende tumorcellen—vooral een vetmolecuul genoemd lysophosphatidylserine—zetten ze een proces hoger genaamd efferocytose, waarbij ze fragmenten van dode cellen opnemen. Dit vergrootte niet alleen hun vermogen om tumorresten te verteren, maar activeerde ook lysosomale paden die belangrijke moleculen afbreken die ze nodig hebben om tumorantigenen aan T-cellen te presenteren.
Twee manieren om immuunaanval te verzwakken
Door GPR34 aangedreven macrofagen ondermijnden T-cellen op een tweede manier: door na opname van beschadigd tumormateriaal hoge niveaus van het signaalproteïne CXCL16 uit te scheiden. CXCL16 fungeerde als een chronisch stimulatiesignaal dat CD8-T-cellen duwde richting een uitgeputte staat, waarbij ze remmende eiwitten op hun oppervlakte tot expressie brengen en hun dodelijke capaciteit verliezen. Het blokkeren van GPR34 verminderde de afgifte van CXCL16, herstelde de antigeenpresentatie door macrofagen en revitaliseerde T-celfunctie. Het team volgde de keten van gebeurtenissen van het schade-lipide, via GPR34 en een gemeenschappelijk groeipad binnen cellen, tot de activering van efferocytose-machinerie en lysosomen. Wanneer ze farmacologisch de downstream stappen van opname of lysosomale verwerking blokkeerden, behielden macrofagen meer van hun antigeen-presenterende moleculen en ondersteunden ze krachtigere T-celreacties, wat benadrukt dat overactieve opruiming paradoxaal genoeg de tumor kan verbergen voor immuunsurveillance.
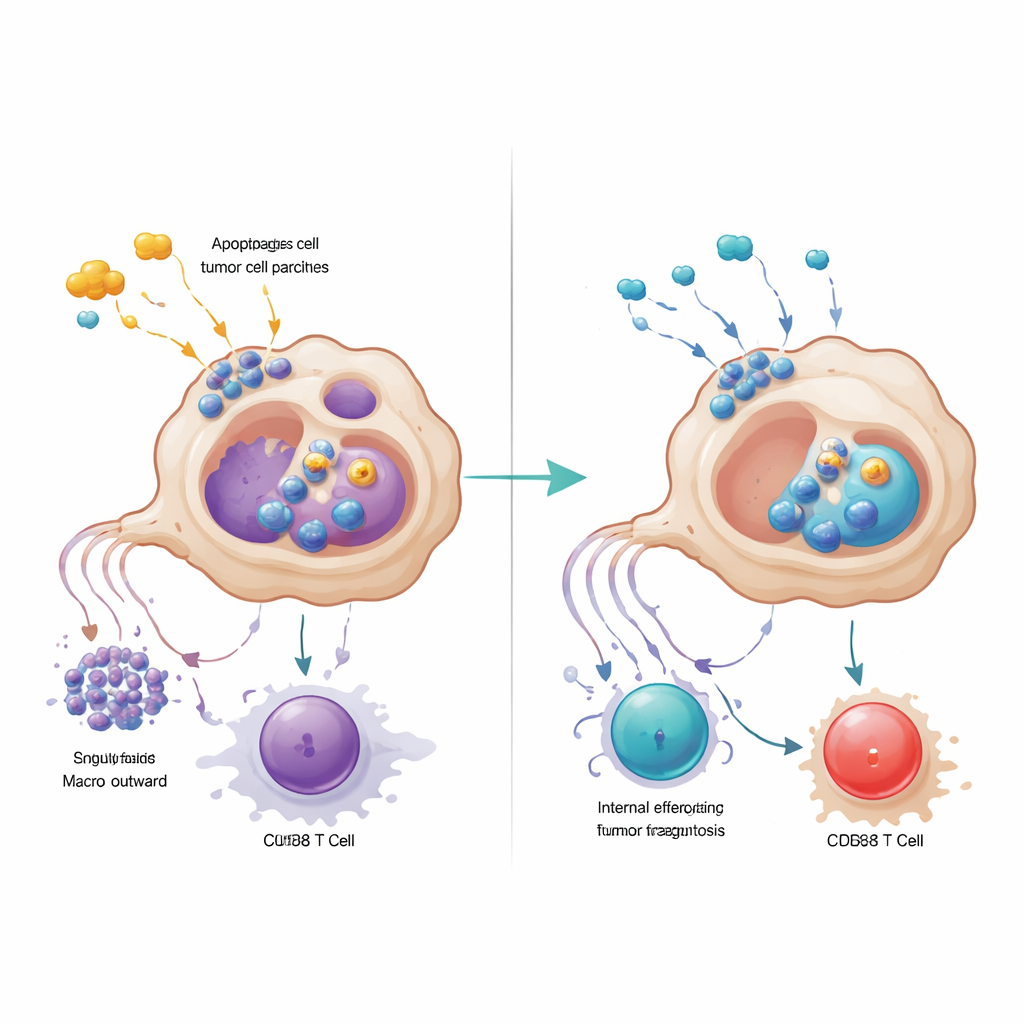
Bestaande medicijnen harder laten werken
Gewapend met dit mechanistische kaartwerk testten de onderzoekers een kleine-molecuul GPR34-remmer in verschillende muismodellen en in patiënt-afgeleide tumoroïden die met immuuncellen werden gekweekt. Het toevoegen van de GPR34-antagonist aan chemotherapie en Surufatinib leidde consequent tot kleinere tumoren, meer tumorcelsterfte, sterkere CD8-T-celactiviteit en minder tekenen van T-celuitputting, zonder duidelijke extra toxiciteit in belangrijke organen of in bloedwaarden. Ter vergelijking: het direct neutraliseren van CXCL16 alleen reproduceerde deze voordelen niet, wat benadrukt dat het centrale hefboompunt de schade-sensor in macrofagen is en diens invloed op zowel efferocytose als antigeenpresentatie. Simpel gezegd suggereert de studie dat sommige macrofagen in alvleesklierkanker zich gedragen als overijverige straatvegers die niet alleen puin opruimen maar ook de aanwijzingen uitwissen die het immuunsysteem nodig heeft. Het uitschakelen van hun GPR34-schakelaar laat chemotherapieschade de tumor blootleggen in plaats van verbergen, en opent de deur naar duurzamere en effectievere behandelingscombinaties.
Bronvermelding: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Trefwoorden: alvleesklierkanker, tumormicro-omgeving, macrofagen, immunotherapie, Surufatinib