Clear Sky Science · pl
Celowanie w GPR34 w makrofagach reagujących na uszkodzenie wzmacnia odporność przeciwnowotworową i skuteczność Surufatinibu w raku trzustki
Dlaczego to badanie ma znaczenie
Rak trzustki jest jednym z najbardziej śmiertelnych nowotworów, częściowo dlatego, że jest otoczony przez immunologiczną „tarcę”, która chroni guz przed atakiem. Artykuł ten ujawnia kluczową grupę komórek układu odpornościowego, które pomagają budować tę tarczę, i pokazuje, że wyłączenie pojedynczego molekularnego przełącznika na tych komórkach może znacząco poprawić działanie standardowych terapii. Dla pacjentów badanie to wskazuje na inteligentniejsze kombinacje leków, które mogłyby wreszcie przechylić szalę na korzyść własnej obrony organizmu.
Ukryci pomocnicy wokół guza
Guzy trzustki rosną w zatłoczonym sąsiedztwie komórek odpornościowych i tkanki łącznej, zwanym mikrośrodowiskiem guza. Jednymi z najbardziej wpływowych mieszkańców są makrofagi — białe krwinki, które zwykle usuwają martwą tkankę i koordynują naprawę. W raku trzustki makrofagi związane z guzem często zmieniają stronę, tłumiąc odpowiedzi immunologiczne i pomagając nowotworowi opierać się leczeniu. Lek o nazwie Surufatinib, stosowany już w innych nowotworach, celuje w jeden z głównych sygnałów wzrostu, który utrzymuje te makrofagi przy życiu. Jednak jego wpływ w raku trzustki był umiarkowany, co sugeruje, że makrofagi mogą mieć zapasowe ścieżki zachowujące ich ochronne role wobec guza.
Śledzenie pojedynczych komórek podczas leczenia
Naukowcy rozpoczęli badanie kliniczne, w którym osoby z rakiem trzustki otrzymały Surufatinib wraz ze standardową chemioterapią przed operacją. Za pomocą analizy pojedynczych komórek RNA — techniki odczytującej aktywność genów w tysiącach indywidualnych komórek — zmapowali wszystkie typy komórek w usuniętych guzach i porównali pacjentów, którzy odpowiedzieli na leczenie, z tymi, u których guzy nadal rosły. U osób niereagujących ogółem było znacznie więcej makrofagów, a jeden podtyp dominował szczególnie. Komórki te miały wysokie poziomy receptora zwanego GPR34 i wykazywały programy genowe powiązane z reakcją na uszkodzenie tkanek, usuwaniem odpadów i tworzeniem środowiska supresyjnego dla odporności. Jednocześnie guzy u niereagujących zawierały więcej wypalonych („wyczerpanych”) komórek zabójczych T, które utraciły zdolność do efektywnego atakowania komórek nowotworowych.
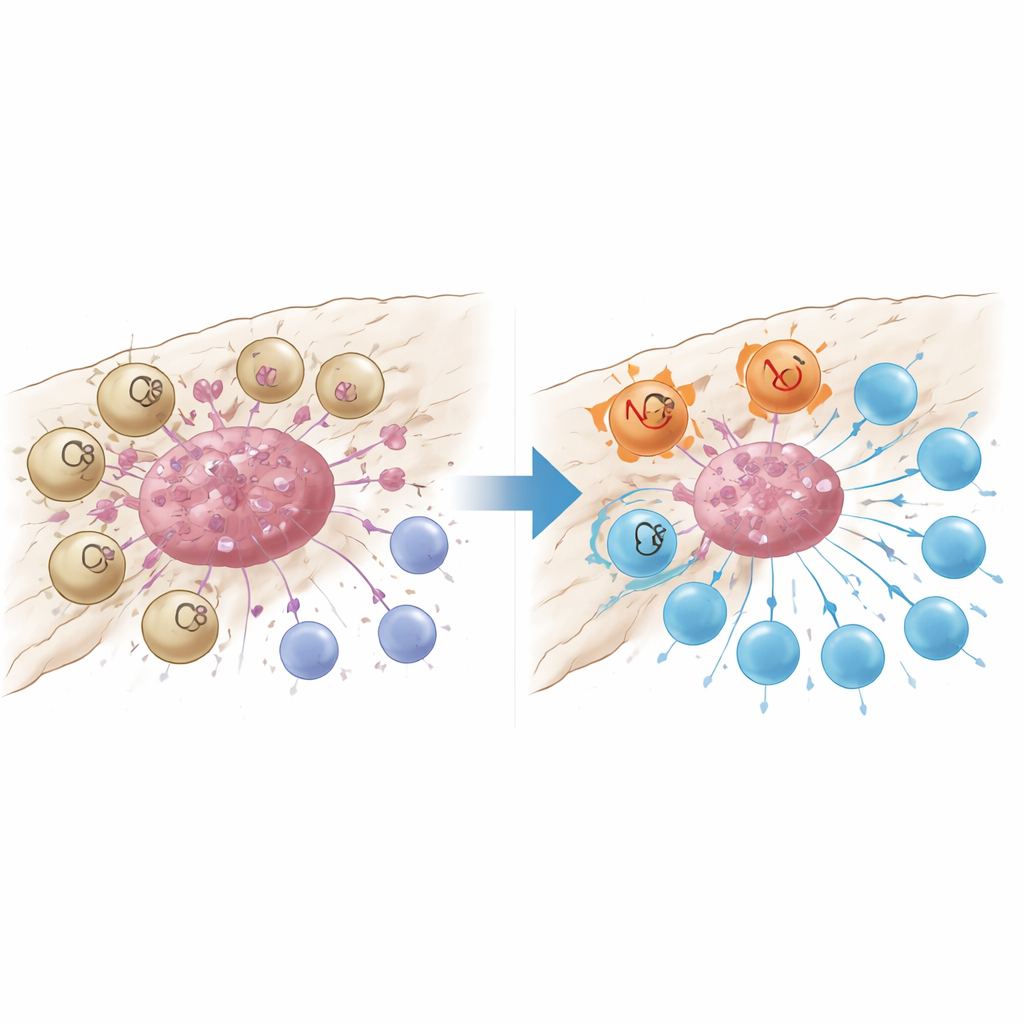
Czujnik uszkodzenia, który wyłącza limfocyty T
Dokładniejsza analiza wykazała, że makrofagi oznaczone GPR34 były ciasno skupione wewnątrz gniazd guza i rzadkie w otaczającej normalnej tkance lub w zapalnej, ale nienowotworowej trzustce. Pacjenci, których guzy zawierały więcej tych komórek, mieli mniej komórek CD8 walczących z rakiem, więcej regulacyjnych komórek T hamujących odporność oraz krótszy czas przeżycia. W modelach mysich, w których GPR34 został usunięty tylko w makrofagach, chemioterapia stała się nagle znacznie skuteczniejsza: guzy kurczyły się bardziej, a wewnątrz guza było więcej limfocytów T o mniejszym stopniu wyczerpania. Eksperymenty in vitro w układach współhodowli wyjaśniły dlaczego. Kiedy makrofagi z GPR34 wykrywały molekularne „sygnały niebezpieczeństwa” uwalniane przez umierające komórki guza — szczególnie lipid zwany lizofosfatydyloseryną — zwiększały proces zwany efferocytozą, podczas którego pochłaniają fragmenty martwych komórek. To nie tylko zwiększało ich zdolność do usuwania szczątków guza, ale także aktywowało wewnętrzne szlaki lizosomalne, które rozkładały kluczowe cząsteczki niezbędne do prezentacji antygenów guza limfocytom T.
Dwa sposoby wyciszania ataku immunologicznego
Makrofagi napędzane przez GPR34 podkopywały limfocyty T także w drugi sposób: wydzielając wysokie poziomy białka sygnałowego CXCL16 po przejęciu uszkodzonego materiału nowotworowego. CXCL16 działał jako chroniczny sygnał stymulujący, popychając komórki CD8 w kierunku stanu wyczerpania, w którym na ich powierzchni pojawiały się hamulce i traciły zdolność do zabijania. Blokada GPR34 zmniejszała uwalnianie CXCL16, przywracała prezentację antygenów przez makrofagi i ożywiała funkcję limfocytów T. Zespół prześledził łańcuch zdarzeń od lipidowego sygnału uszkodzenia, przez GPR34 i powszechną wewnątrzkomórkową ścieżkę wzrostu, do aktywacji mechanizmów efferocytozy i lizosomów. Gdy farmakologicznie zablokowali dalsze etapy pochłaniania lub lizosomalne, makrofagi zachowywały więcej cząsteczek prezentujących antygeny i wspierały silniejsze odpowiedzi T, co podkreśla, że nadmierne sprzątanie paradoksalnie może ukrywać guz przed nadzorem immunologicznym.
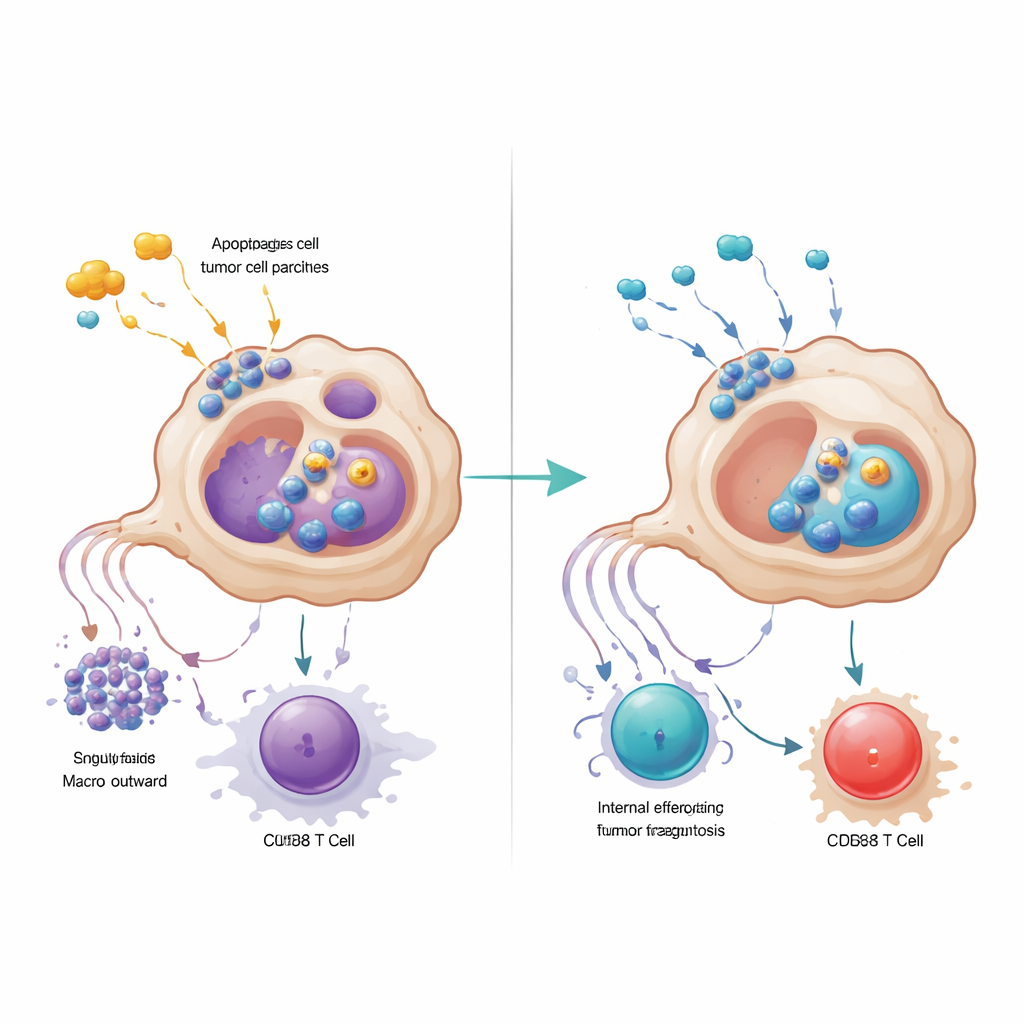
Sprawienie, by istniejące leki działały silniej
Uzbrojeni w tę mapę mechanistyczną, badacze przetestowali małocząsteczkowy bloker GPR34 w kilku modelach mysich i w organoidach pochodzących od pacjentów hodowanych z komórkami odpornościowymi. Dodanie antagonisty GPR34 do chemioterapii i Surufatinibu konsekwentnie prowadziło do mniejszych guzów, większej śmierci komórek nowotworowych, silniejszej aktywności komórek CD8 i mniejszych oznak wyczerpania T, bez widocznej dodatkowej toksyczności w głównych narządach czy we krwi. W przeciwieństwie do tego, bezpośrednie unieszkodliwienie samego CXCL16 nie odtworzyło tych korzyści, co podkreśla, że centralnym punktem dźwigni jest czujnik uszkodzenia makrofagów i jego wpływ zarówno na efferocytozę, jak i prezentację antygenów. Mówiąc prościej, badanie sugeruje, że pewne makrofagi w raku trzustki działają jak nadgorliwe zamiatacze uliczne, które nie tylko usuwają szczątki, ale także zacierają wskazówki potrzebne układowi odpornościowemu. Wyłączenie ich przełącznika GPR34 pozwala, by uszkodzenia wywołane chemioterapią ujawniły guz zamiast go ukrywać, otwierając drogę do trwalszych i skuteczniejszych kombinacji terapeutycznych.
Cytowanie: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Słowa kluczowe: rak trzustki, mikrośrodowisko guza, makrofagi, immunoterapia, Surufatinib