Clear Sky Science · ru
Нацеливание на GPR34 в макрофагах, реагирующих на повреждения, усиливает противоопухолевый иммунитет и эффективность Суруфатиниба при раке поджелудочной железы
Почему это исследование важно
Рак поджелудочной железы — один из самых смертельных видов рака, частично из‑за того, что опухоль окружена иммунной «силовой оболочкой», которая защищает её от атаки. В этой статье выявлена ключевая группа иммунных клеток, помогающая строить эту оболочку, и показано, что отключение одного молекулярного переключателя в этих клетках может заметно повысить эффективность стандартных методов лечения. Для пациентов это исследование указывает на более разумные комбинации препаратов, которые могли бы наконец склонить чашу весов в пользу собственных защитных сил организма.
Скрытые помощники вокруг опухоли
Опухоли поджелудочной железы растут в плотном окружении иммунных и соединительных клеток, известном как опухолевое микроокружение. Одними из самых влиятельных обитателей являются макрофаги — лейкоциты, которые обычно очищают мёртвые участки ткани и координируют восстановление. При раке поджелудочной железы эти опухолево‑ассоциированные макрофаги часто «переходят на сторону врага», подавляя иммунные ответы и помогая опухоли сопротивляться лечению. Препарат Суруфатиниб, уже применяемый при других раках, нацелен на один из главных сигнальных путей, поддерживающих выживание этих макрофагов. Но его эффект при раке поджелудочной был умеренным, что наводит на мысль о наличии у макрофагов запасных маршрутов, сохраняющих их опухле‑защитные функции.
Отслеживание отдельных клеток во время лечения
Исследователи провели клиническое исследование, в котором пациенты с раком поджелудочной получали Суруфатиниб вместе со стандартной химиотерапией перед операцией. С помощью одно‑клеточного секвенирования РНК — метода, считывающего активность генов в тысячах отдельных клеток — они картировали все типы клеток в удалённых опухолях и сравнивали пациентов, ответивших на лечение, с теми, у кого опухоль продолжала расти. У неответивших было значительно больше макрофагов в целом, и один подтип особенно доминировал. Эти клетки выражали высокие уровни рецептора GPR34 и имели генетические программы, связанные с реакциями на повреждение ткани, утилизацией отходов и созданием иммуноподавляющей среды. Одновременно в опухолях неответивших наблюдалось больше «истощённых» киллерных T-клеток, утративших способность эффективно убивать раковые клетки.
Датчик повреждений, который выключает T‑клетки
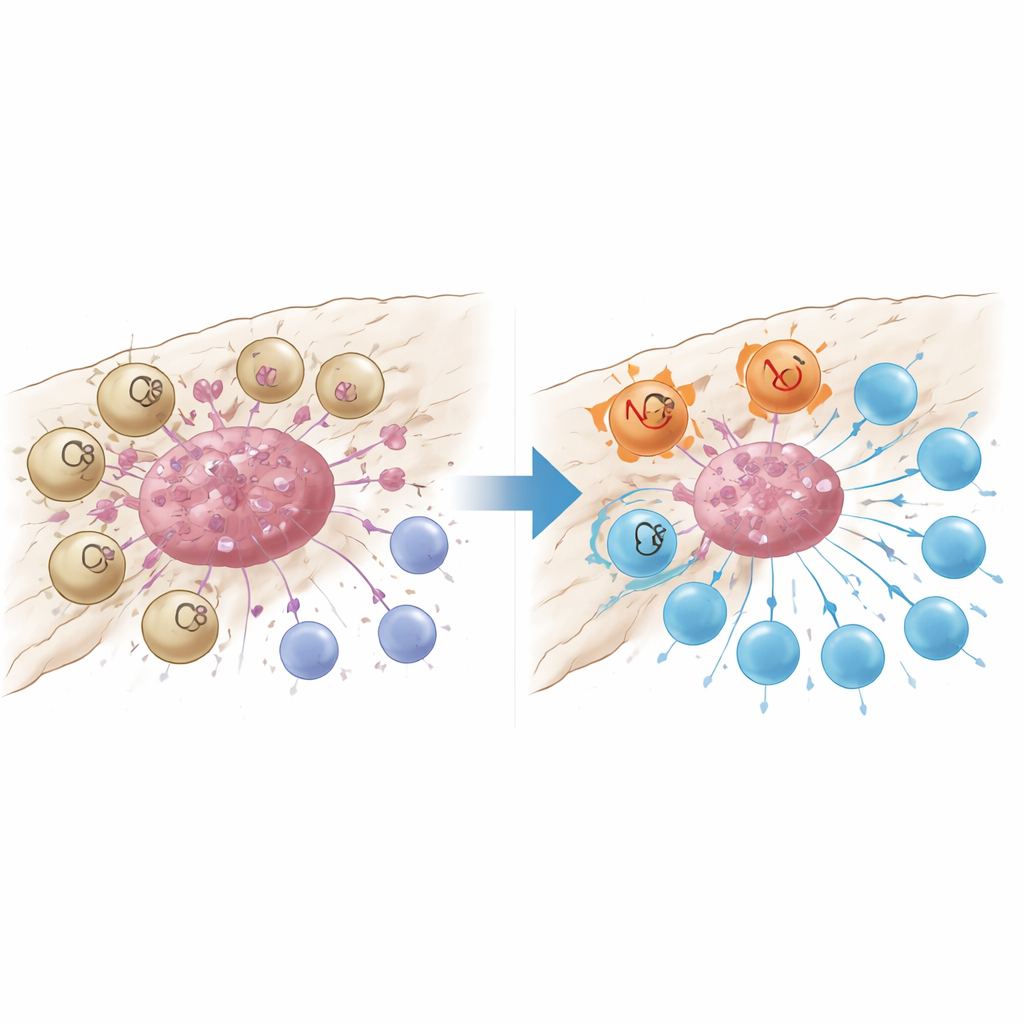
Более детальный анализ показал, что макрофаги, помеченные GPR34, были сконцентрированы внутри опухолевых гнёзд и редко встречались в окружающей нормальной ткани или в воспалённой, но некопущённой поджелудочной. У пациентов с большим числом таких клеток было меньше CD8+ T‑клеток‑киллеров, больше регуляторных T‑клеток, сдерживающих иммунитет, и более короткое выживание. В модельных мышах, у которых GPR34 удалили только в макрофагах, химиотерапия внезапно стала значительно эффективнее: опухоли уменьшались больше, а внутри опухолей T‑клеток было больше и они были менее «истощёнными». Лабораторные совместные культивирования объяснили, почему. Когда макрофаги с GPR34 ощущали молекулярные «сигналы опасности», высвобождаемые гибнущими опухолевыми клетками — особенно липид лизофосфатидилсерин — они усиливали процесс, называемый эффероцитозом, при котором поглощают фрагменты мёртвых клеток. Это не только увеличивало их способность убирать погибшие клетки опухоли, но и запускало внутриклеточные лизосомные пути, разрушающие ключевые молекулы, необходимые для презентации опухолевых антигенов T‑клеткам.
Два способа подавления иммунной атаки
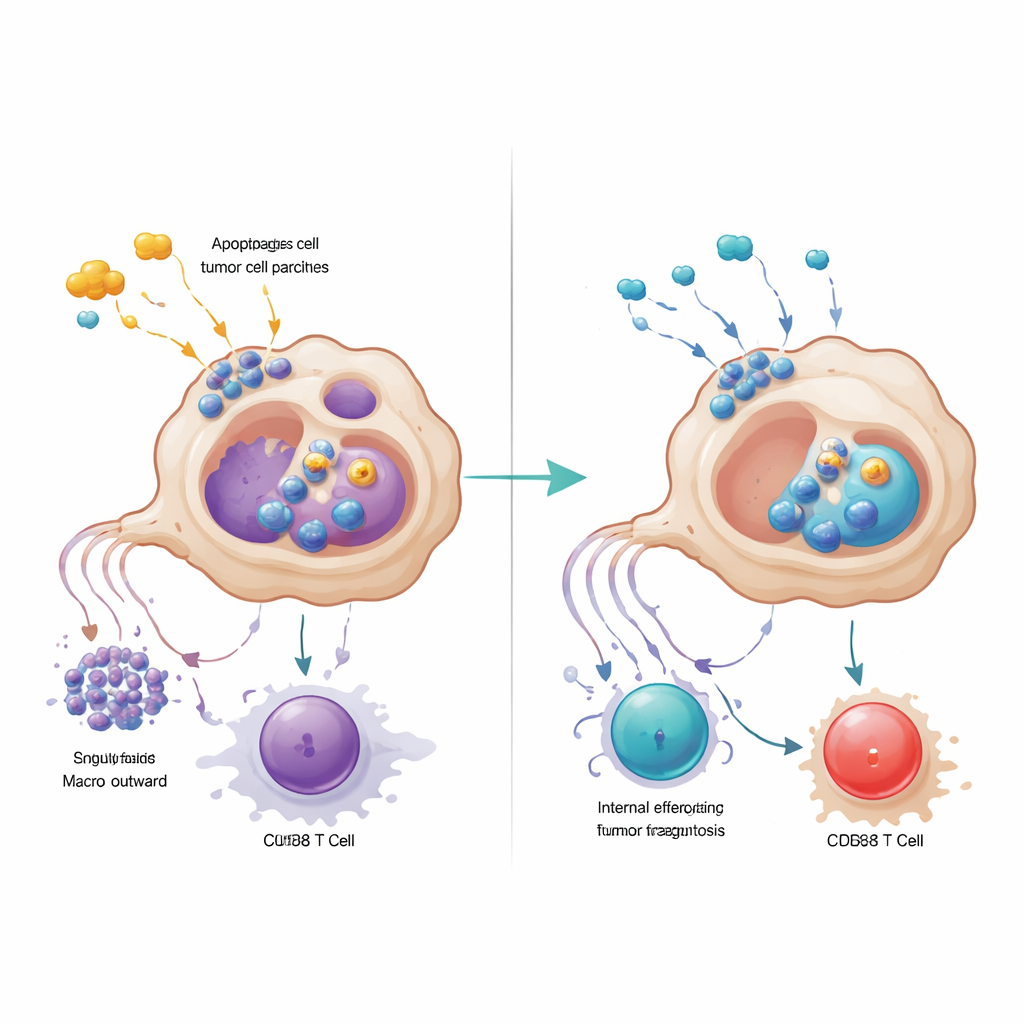
Макрофаги, активируемые через GPR34, подрывали T‑клетки и вторым способом: выделением высоких уровней сигнального белка CXCL16 после захвата повреждённого опухолевого материала. CXCL16 действовал как хронический стимул, толкая CD8+ T‑клетки в состояние истощения, при котором они экспрессируют тормозящие молекулы на своей поверхности и теряют цитотоксическую функцию. Блокирование GPR34 снижало выброс CXCL16, восстанавливало презентацию антигенов макрофагами и ревитализировало функцию T‑клеток. Команда проследила цепочку событий от липида‑сигнала повреждения через GPR34 и общий ростовой путь внутри клетки до активации механизмов эффероцитоза и лизосом. Когда они фармакологически блокировали последующие шаги захвата или лизосомную активность, макрофаги сохраняли больше молекул для презентации антигенов и поддерживали более мощные T‑клеточные ответы, подчёркивая, что чрезмерная уборка парадоксально может скрывать опухоль от иммунного надзора.
Усиление эффективности существующих препаратов
Вооружившись этой механистической схемой, исследователи испытали маломолекулярный блокатор GPR34 в нескольких мышиных моделях и в органоидах опухолей, полученных от пациентов и выращенных вместе с иммунными клетками. Добавление антагониста GPR34 к химиотерапии и Суруфатинибу последовательно приводило к уменьшению размеров опухолей, большему числу погибших опухолевых клеток, усилению активности CD8+ T‑клеток и снижению признаков их истощения, без явной дополнительной токсичности для основных органов или показателей крови. Напротив, прямое нейтрализующее действие на CXCL16 само по себе не воспроизводило этих выгод, что подчёркивает: центральной точкой воздействия является датчик повреждений в макрофагах и его влияние как на эффероцитоз, так и на презентацию антигенов. Проще говоря, исследование показывает, что некоторые макрофаги при раке поджелудочной выступают как чрезмерно рьяные уличные дворники, которые не только убирают мусор, но и стирают следы, нужные иммунной системе. Отключение их переключателя GPR34 позволяет повреждению, вызванному химиотерапией, обнажить опухоль, а не скрыть её, открывая путь к более длительным и эффективным комбинациям лечения.
Цитирование: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Ключевые слова: рак поджелудочной железы, опухолевый микроокружение, макрофаги, иммунотерапия, Суруфатиниб