Clear Sky Science · es
Apuntar a GPR34 en macrófagos asociados al daño potencia la inmunidad antitumoral y la eficacia de Surufatinib en el cáncer de páncreas
Por qué importa este estudio
El cáncer de páncreas es uno de los más letales, en parte porque está rodeado por un “campo de fuerza” inmunitario que protege el tumor del ataque. Este artículo revela un grupo clave de células inmunitarias que contribuyen a construir ese escudo y muestra que desactivar un único interruptor molecular en esas células puede mejorar considerablemente los tratamientos estándar. Para los pacientes, esta investigación apunta hacia combinaciones de fármacos más inteligentes que podrían, por fin, inclinar la balanza a favor de las defensas del propio organismo.
Los ayudantes ocultos alrededor del tumor
Los tumores pancreáticos crecen dentro de un vecindario denso de células inmunitarias y conectivas conocido como microambiente tumoral. Entre los residentes más influyentes están los macrófagos: glóbulos blancos que normalmente limpian tejido muerto y ayudan a coordinar la reparación. En el cáncer de páncreas, estos macrófagos asociados al tumor a menudo cambian de bando, atenuando las respuestas inmunitarias y ayudando al cáncer a resistir el tratamiento. Un fármaco llamado Surufatinib, ya usado en otros cánceres, apunta a una de las señales de crecimiento principales que mantiene vivos a estos macrófagos. Pero su impacto en el cáncer de páncreas ha sido modesto, lo que sugiere que los macrófagos pueden disponer de vías alternativas que preservan sus roles protectores del tumor.
Rastreando células individuales durante el tratamiento
Los investigadores pusieron en marcha un ensayo clínico en el que personas con cáncer de páncreas recibieron Surufatinib junto con quimioterapia estándar antes de la cirugía. Usando secuenciación de ARN de célula única—una técnica que lee la actividad génica en miles de células individuales—mapearon todos los tipos celulares en los tumores extirpados y compararon a los pacientes que respondieron al tratamiento con aquellos cuyos tumores siguieron creciendo. Los no respondedores tenían muchos más macrófagos en general, y un subtipo en particular dominaba. Estas células presentaban altos niveles de un receptor llamado GPR34 y mostraban programas génicos vinculados a respuestas al daño tisular, limpieza de desechos y creación de un entorno inmunosupresor. Al mismo tiempo, los tumores de los no respondedores contenían más células T citotóxicas “agotadas” que habían perdido su capacidad de atacar eficazmente a las células cancerosas.
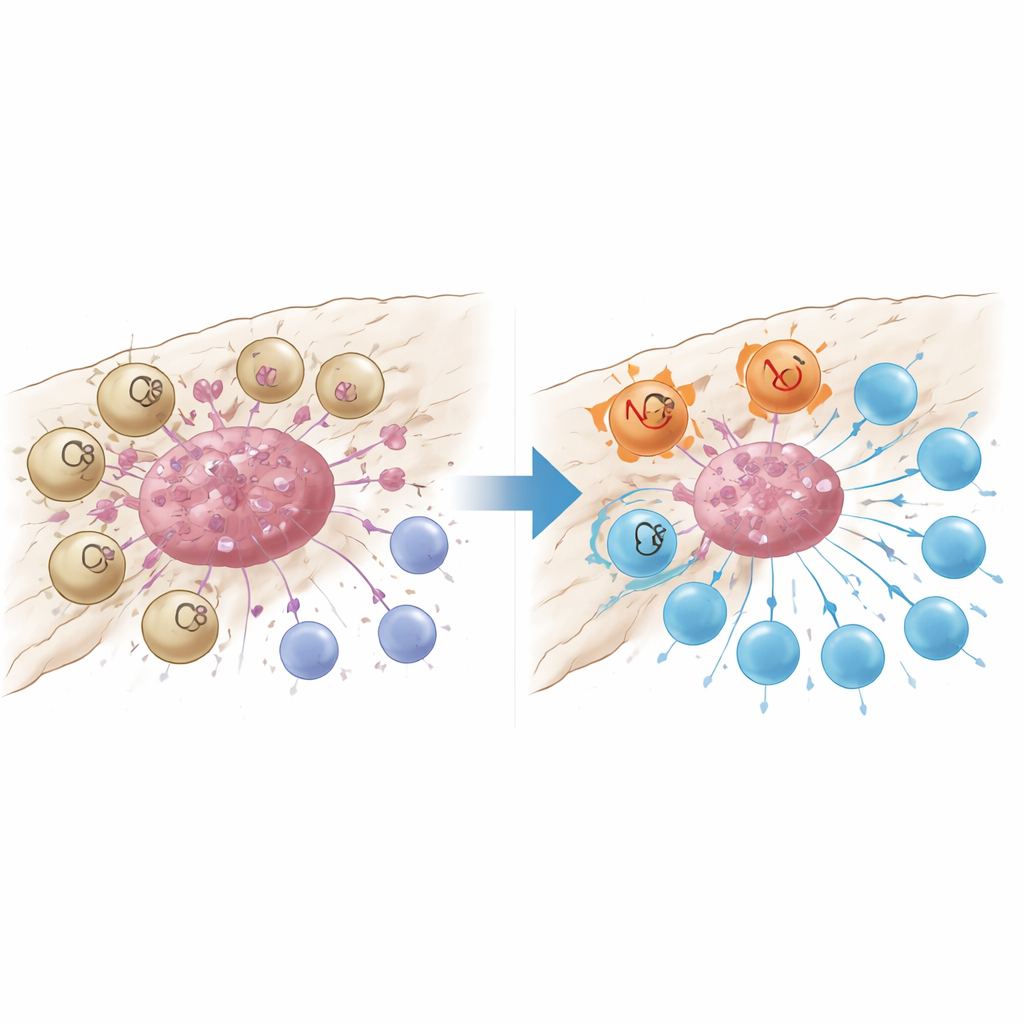
Un sensor de daño que apaga a las células T
Un análisis más detallado reveló que los macrófagos marcados por GPR34 se agrupaban de forma compacta dentro de los nidos tumorales y eran raros en el tejido normal circundante o en el páncreas inflamado pero no canceroso. Los pacientes cuyos tumores contenían más de estas células tenían menos células T CD8 que combaten el cáncer, más células T reguladoras que restringen la inmunidad y tiempos de supervivencia más cortos. En modelos de ratón diseñados para carecer de GPR34 solo en macrófagos, la quimioterapia se volvió de repente mucho más efectiva: los tumores se encogieron más y las células T dentro del tumor eran más numerosas y menos agotadas. Experimentos de cocultivo en el laboratorio explicaron por qué. Cuando los macrófagos con GPR34 detectaban señales moleculares de “peligro” liberadas por células tumorales moribundas—especialmente un lípido llamado lisofosfatidilserina—aumentaban un proceso llamado eférofagocitosis, en el que engullen fragmentos de células muertas. Esto no solo incrementó su capacidad para devorar los restos tumorales, sino que también activó vías lisosomales internas que degradaban moléculas clave necesarias para presentar antígenos tumorales a las células T.
Dos maneras de silenciar el ataque inmunitario
Los macrófagos impulsados por GPR34 minaron a las células T de una segunda forma: secretando altos niveles de la proteína señalizadora CXCL16 tras incorporar material tumoral dañado. CXCL16 actuó como una señal de estimulación crónica, empujando a las células T CD8 hacia un estado de agotamiento donde expresan frenos en su superficie y pierden poder citotóxico. Bloquear GPR34 redujo la liberación de CXCL16, restauró la presentación de antígenos en los macrófagos y revitalizó la función de las células T. El equipo trazó la cadena de eventos desde el lípido señal de daño, a través de GPR34 y una vía de crecimiento común dentro de la célula, hasta la activación de la maquinaria de eférofagocitosis y los lisosomas. Cuando bloquearon farmacológicamente los pasos posteriores de ingestión o lisosomales, los macrófagos conservaron más de sus moléculas presentadoras de antígenos y apoyaron respuestas T más potentes, subrayando que una limpieza demasiado activa puede, paradójicamente, ocultar el tumor a la vigilancia inmunitaria.
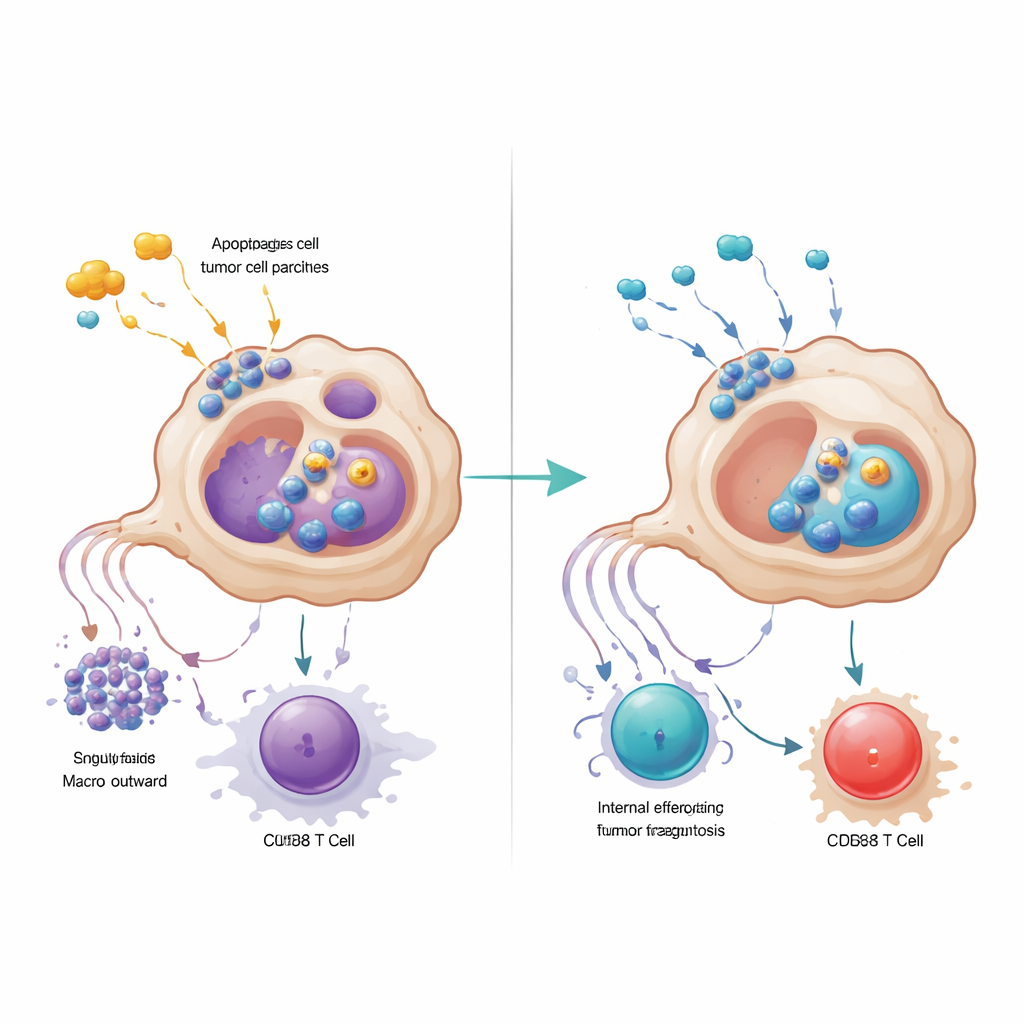
Hacer que los fármacos existentes funcionen mejor
Armados con este mapa mecanicista, los investigadores probaron un bloqueador de pequeña molécula de GPR34 en varios modelos de ratón y en organoides tumorales derivados de pacientes cultivados con células inmunitarias. Añadir el antagonista de GPR34 a la quimioterapia y a Surufatinib condujo de forma consistente a tumores más pequeños, más muerte de células tumorales, mayor actividad de las células T CD8 y menos signos de agotamiento T, sin toxicidad añadida aparente en órganos principales o en los recuentos sanguíneos. En contraste, neutralizar directamente CXCL16 por sí solo no reprodujo estos beneficios, lo que pone de relieve que el punto de palanca central es el sensor de daño de los macrófagos y su impacto tanto en la eférofagocitosis como en la presentación de antígenos. En términos sencillos, el estudio sugiere que algunos macrófagos en el cáncer de páncreas actúan como barrenderos demasiado entusiastas que no solo eliminan los restos, sino que también borran las pistas que el sistema inmunitario necesita. Apagar su interruptor GPR34 permite que el daño causado por la quimioterapia exponga el tumor en lugar de ocultarlo, abriendo la puerta a combinaciones de tratamiento más duraderas y efectivas.
Cita: Guo, X., Liu, Y., Li, T. et al. Targeting GPR34 in damage-associated macrophages enhances anti-tumor immunity and the efficacy of Surufatinib in pancreatic cancer. Sig Transduct Target Ther 11, 156 (2026). https://doi.org/10.1038/s41392-026-02641-4
Palabras clave: cáncer de páncreas, microambiente tumoral, macrófagos, inmunoterapia, Surufatinib