Clear Sky Science · zh
p53:从理解其结构到治疗靶向的进展
为何这位“守护蛋白”至关重要
蛋白 p53 常被称为“基因组的守护者”,因为它帮助健康细胞修复损伤,并阻止受损细胞演变为癌细胞。本文综述阐述了 p53 的工作机制、它为何在癌症中频繁失灵,以及科学家如何开始设计针对长期被认为“不可成药”的目标的药物。文章还探讨了 p53 与阿尔茨海默病、糖尿病和心脏病等疾病之间令人意外的联系,并概述了旨在修复或绕过 p53 功能缺陷的新治疗方法。
细胞内部的安全检查员
在正常情况下,细胞通过内置的回收系统保持 p53 水平较低。当细胞受到压力——例如 DNA 损伤、缺氧或促癌信号——p53 会迅速积累并启动大量基因。这些基因可以暂停细胞分裂、触发 DNA 修复、调整代谢,或者在损伤不可逆时促使细胞进入永久退休状态(衰老)或受控死亡(凋亡)。通过这些机制,p53 保持遗传密码的稳定并防止受损细胞增殖。它还影响诸如铁死亡等较新的细胞死亡形式,并塑造肿瘤周围的免疫环境,帮助免疫细胞识别并攻击癌变细胞。
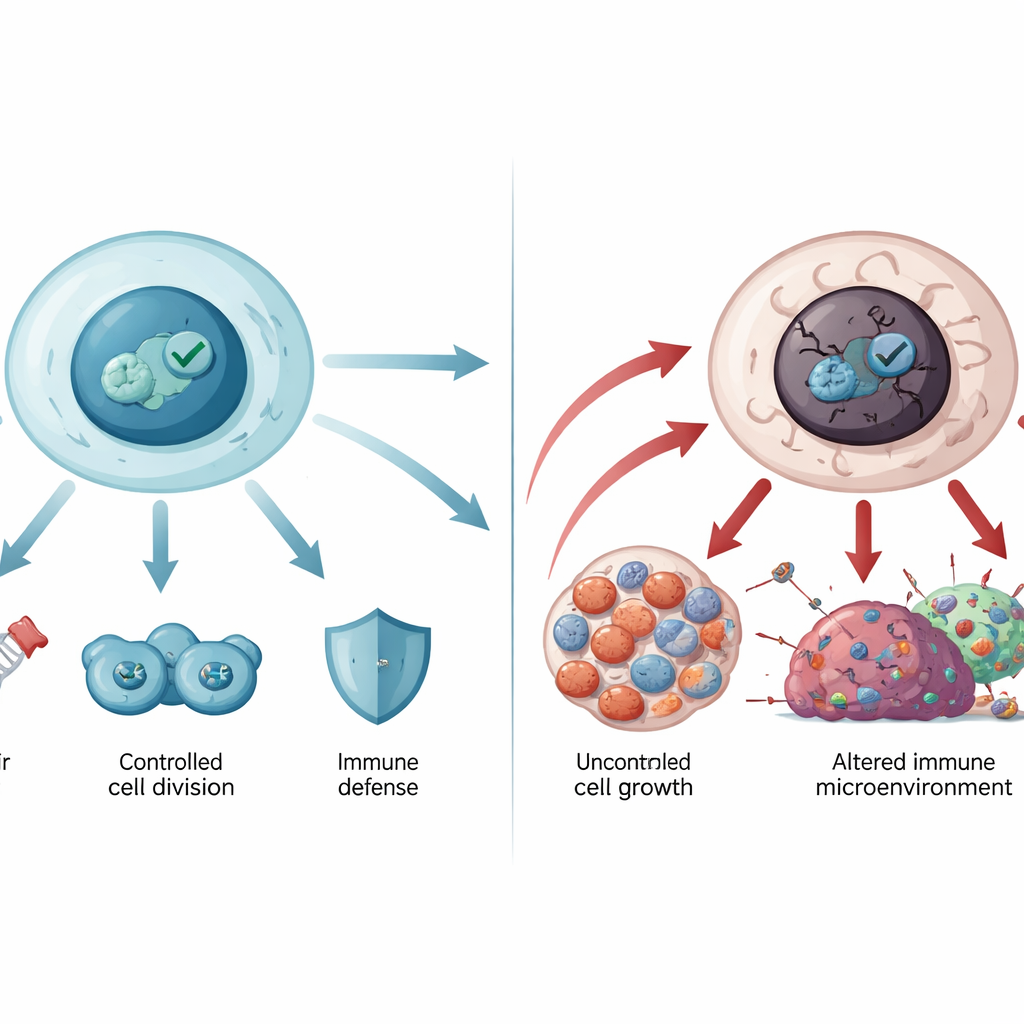
当守护者失控时
编码 p53 的基因 TP53 是人类癌症中突变最频繁的基因。大多数这些突变是发生在蛋白中心 DNA 结合区域的单个氨基酸替换。有些突变削弱了 p53 与 DNA 的结合能力,而另一些则使其结构不稳定,导致展开并凝聚成类似淀粉样的聚集体,这一点在神经退行性疾病中也有所见到。突变的 p53 不仅失去保护功能,还可能获得新的促癌活性:它可以促进不受控的生长、帮助肿瘤细胞抵抗细胞死亡和化疗、重塑代谢以供肿瘤所需,并削弱抗肿瘤免疫。生殖系 TP53 突变造成的 Li–Fraumeni 综合征及其他罕见的遗传性疾病显示出该通路对终生防护的重要性。
超越癌症:与大脑、代谢和心脏的联系
由于 p53 控制细胞死亡、应激反应和能量利用,其影响超出癌症范畴。在大脑中,异常的 p53 活性已与阿尔茨海默病、帕金森病、亨廷顿病、肌萎缩侧索硬化和多发性硬化症相关,常通过与疾病相关蛋白相互作用并促进脆弱神经元过度丧失来发挥作用。在代谢方面,p53 帮助调节脂肪储存、血糖和肝脏脂肪;其作用取决于具体情境,既可以保护机体免受肥胖和糖尿病,也可能促成胰岛素抵抗和脂肪肝。在心脏和血管中,p53 影响细胞存活、瘢痕形成和动脉粥样斑块的形成,在心力衰竭、糖尿病相关心脏损伤和动脉粥样硬化中扮演复杂角色。这些广泛的效应意味着任何增强或抑制 p53 的尝试都必须在抗癌益处与对正常组织潜在伤害之间找到平衡。
为“不可成药”寻找新打法
数十年来,人们认为 p53 过于复杂且过于关键,难以安全地作为药物靶点。但这一观点正在改变。一种主要策略旨在“拯救”突变 p53,通过稳定其构象使其行为更接近正常蛋白;相关例子包括 PRIMA‑1/APR‑246、三氧化二砷,以及针对特定热点突变(如 Y220C 或 R175H)的定制分子。另一种方法是在肿瘤仍保有完整 TP53 基因的情况下,通过阻断其负调控因子 MDM2 和 MDM4 提高正常 p53 的水平;这些蛋白的多种口服抑制剂正在进行临床试验。第三种策略试图通过促进突变 p53 的降解来切断肿瘤细胞对其的依赖,手段包括热休克抑制剂、组蛋白去乙酰化酶抑制剂或常用的他汀类药物。同时,疫苗、工程化树突状细胞和高度特异性的抗体也在开发中,以帮助免疫系统识别和清除积累异常 p53 的细胞。
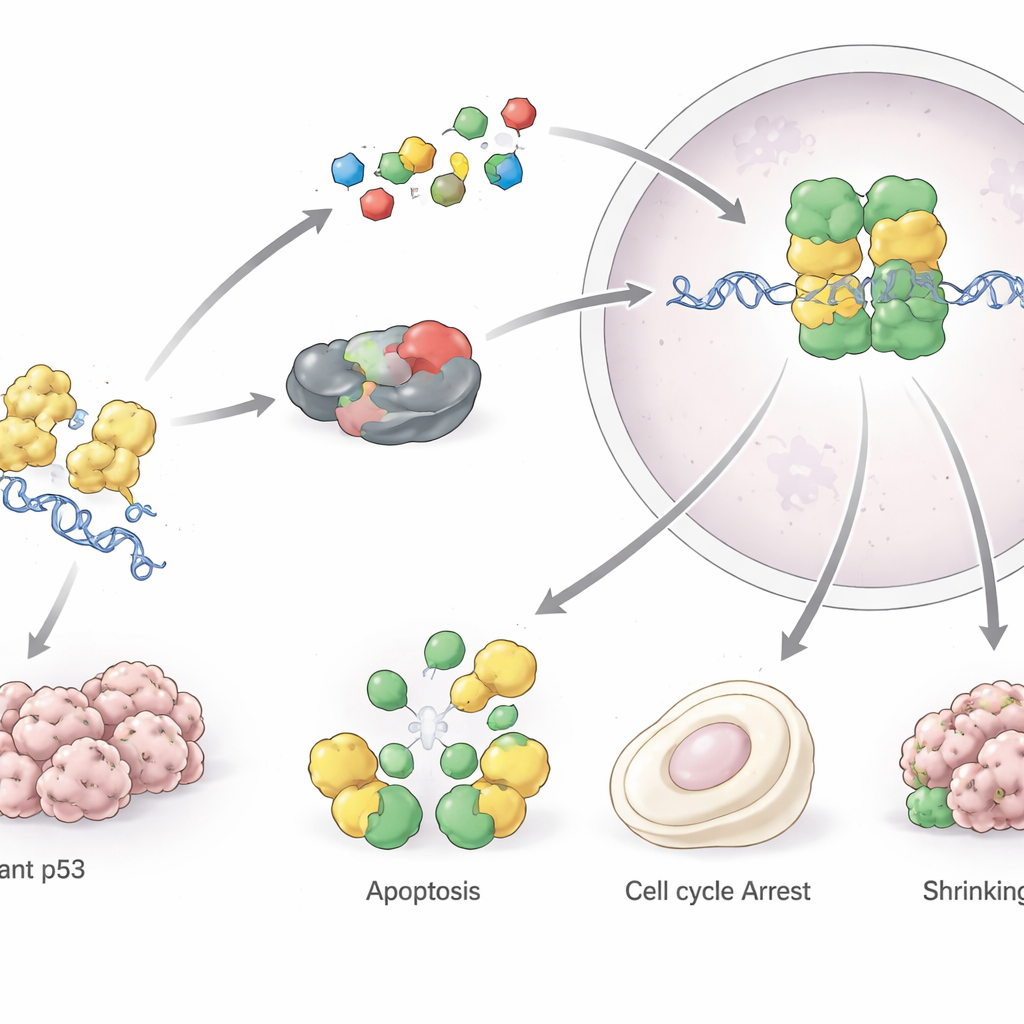
展望:从地图到药物
文章总结道,p53 已从一种纯粹的生物学兴趣对象转变为一个现实可及的治疗靶点,但这需要高度精确的策略。TP53 突变的多样性和 p53 在正常组织中双刃剑式的作用使得一刀切的治疗方案不太可能。相反,作者设想将小分子、免疫疗法和基因编辑工具与系统生物学和机器学习相结合,以根据每个肿瘤的线路图匹配最合适的 p53 靶向策略。如果这些努力成功,恢复或补偿 p53 功能的药物不仅可能改变多种癌症的治疗,还可能惠及某些与该守护蛋白相关的非癌症疾病。
引用: Wang, W., Liu, X., Liu, H. et al. p53: from understanding its structure to advances in therapeutic targeting. Sig Transduct Target Ther 11, 121 (2026). https://doi.org/10.1038/s41392-025-02549-5
关键词: p53, TP53 突变, 癌症治疗, 抑癌通路, 靶向 p53 的药物